Папілярний рак щитоподібної залози
| Папілярний рак щитоподібної залози | |
|---|---|
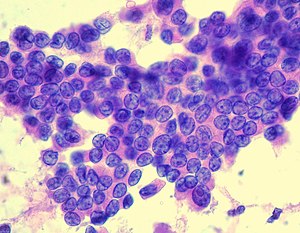 Цитологічна картина папілярного раку щитоподібної залози (посилення х1000, фарбування г-е). | |
| Спеціальність | онкологія |
| Симптоми | thyroid noduled[1][2] |
| Класифікація та зовнішні ресурси | |
| МКХ-11 | 2D10.1 |
| МКХ-10 | C73 |
| МКХ-9 | 193 |
| МКХ-О | M8140/3 |
| OMIM | 603744 |
| eMedicine | med/2464 |
| MeSH | D013964 |
| | |
Папілярний рак щитоподібної залози або папілярна карцинома щитоподібної залози — найпоширеніше злоякісне новоутворення щитоподібної залози у дітей та дорослих, що становить до 80% всіх злоякісних новоутворень щитоподібної залози.[3][4][5][6][7] Як правило, папілярний рак щитоподібної залози уражає жінок та пацієнтів, що зазнали раідоактивного опромінення ділянок голови та шиї у зв'язку з медичними показанями або внаслідок аварії на Чорнобильській АЕС.[4]
Маркери карциноми[ред. | ред. код]
- Тиреоглобулін використовують як маркер раку для диференційованих форм раку щитоподібної залози, до яких також належить папілярний.[8][9]
- Імуногістохімічне визначення експресії протеїнів HBME-1 та цитокератину 19 (СК-19) також має певне діагностичне значення для диференційованого діагнозу між папілярною та фолікулярною карциномами щитоподібної залози, оскільки експресія цих протеїнів спостерігається переважно в папілярному раку.[10]
- Визначення мутації в 15 екзоні гену BRAF або експресії різноманітних протеїнів також може мати діагностичне значення.[11][12]
Патогістологічна характеристика[ред. | ред. код]


За гістологічними характеристиками визначають класичний папілярний рак, фолікулярний варіант папілярного раку, дифузносклеротичний варіант, веретеноклітинний варіант, інкапсульований неінвазивний варіант папілярного раку.
- Характерним для папілярного раку є наявність нуклеарних включень (ядро клітини, при фарбуванні гематоксиліном-еозином, містить порожні ділянки)[13] та псамомних тілець при світловій мікроскопії. Ці ознаки використовують при ідентифікації фолікулярного варіанту папілярного раку, при якому клітини не утворюють характерних папілярних структур.[14]
- Метастази в лімфатичні вузли шиї внаслідок переважно лімфогенного метастазування
- Мультифокальність
Папілярний рак щитоподібної залози іноді характеризується високою інвазивною активністю, що проявляється метастазуванням переважно лімфогенним шляхом, хоча інвазія кровоносних судин теж виникає.[15] Внаслідок цих властивостей рідко зустрічається інкапсуляція папілярного раку, а інвазія за межі капсули щитоподібної залози сягає 40 %.[16] Віддалені метастази найчастіше уражають легені, але кількість таких випадків менше 10 %.
Папілярна мікрокарцинома щитоподібної залози[ред. | ред. код]
Папілярний рак, розміри якого менше 1 см в найбільшому діаметрі.[5] Поширеність мікрокарциноми може сягати 30 %, про що свідчать дослідження аутопсійного матеріалу,[17] та до 50 % згідно з даними ретроспективних досліджень.[18] Лікувальна стратегія щодо інсидентальної мікрокарциноми варіює, незважаючи на верифікованість діагнозу за даними ультразвукового дослідження, які підтверджені даними цитологічного аналізу аспіратів тонкоголкової аспіраційної пункційної біопсії (ТАПБ). Переважно пацієнтам виконується тотальна тиреоїдектомія з послідуючою абляцією радіокативним йодом (І-131).
Оккультна папілярна карцинома[ред. | ред. код]
Цим терміном описують метастаз папілярного рака щитоподібної залози при відсутності клінічної картини первинної пухлини в самій щитоподібній залозі. Вперше описано в дослідженні Woolner et al. в 1960 році.[19]
Кістозний тип папілярного раку[ред. | ред. код]
Кістозний тип папілярної карциноми являє собою класичний за патогістологічною будовою ПРЩ, що визначається у вигляді новоутворення стінки кістозного утворення щитоподібної залози. Клінічний перебіг кістозного ПРЩ схожий з класичним ПРЩ.[20] Проте виявлення даного виду карциноми може бути складним внаслідок малоінфомативної ТАПБ, що може містити переважно кістозну рідину та недостатню для патоцитологічного висновку кількість фолікулярних клітин.
Інкапсульований неінвазивний варіант папілярного раку[ред. | ред. код]
B 2016 році в США це новоутворення було рекласифіковано. Згідно рішення групи експертів, цей тип новоутворення більше не належить до карциноми в США, та визначається як «неінвазивна фолікулярна неоплазія щитоподібної залози з папілярно-подібними змінами ядер» (англ. noninvasive follicular thyroid neoplasm with papillary-like nuclear features).[21]
Папілярний рак на фоні іншої тиреоїдної патології[ред. | ред. код]
Карцинома може виникати на фоні доброякісної тиреоїдної патології до 30% випадків, що вимагає ретельної оцінки вузлів щитоподібної залози за наявності:
- Хвороби Грейвса[22]
- Тиреоїдиту Хашимото
- Нетоксичного багатовузлового зобу
- Токсичного багатовузлового зобу
- Аденома щитоподібної залози
Генетичний профіль[ред. | ред. код]
З папілярним раком щитоподібної залози як правило асоціюються два типи генетичних аномалій: хромосомні транслокації та точкові мутації, переважно генів, що беруть участь в регуляцій сигнального шляху MAPK/ERK.
Хромосомні транслокації часто спостерігаються в прото-онкогені RET, який кодує рецептор тирозин-кінази. RET розташований на 10 хромосомі людини (10q11), відіграє значну роль в нормальному розвитку нейроендокринних клітин. Транслокації або перестановки з іншими ділянками 10-ї хромосоми призводять до утворення хімерних форм RET (RET/PTC), кодують однойменні білки та мають вплив на MAPK/ERK, що може призводити до утворення карциноми.[7][23]
Приблизно 30% папілярних карцином демонструють точкові мутації в 15 екзоні гену BRAF, що також приймає учать в регуляції сигнального шляху MAPK/ERK.[7][16] За деякими даними, цю мутацію слід асоціювати з більш агресивним фенотипом папілярного раку, оскільки мутація BRAF також спостерігається в низько-диференційованому та анапластичному раках щитоподібної залози, попередниками яких вважається папілярна карцинома.
Папілярний рак щитоподібної характеризується посиленою експресією протеїна S100A6, у порівнянні з фолікулярними пухлинами та нормальною тканиною щитоподібної залози.[11]
Діагностика[ред. | ред. код]
Папілярний рак часто діагностується при рутинному медичному огляді та проявляється асимптоматичним вузловим утворенням щитоподібної залози. У деяких випадках це вузлове утворення може спричиняти появу локальних симптомів, таких як певний дискомфорт в області шиї та при ковтанні, відчуття стороннього тіла в горлі.
Загальні підходи до діагностики[ред. | ред. код]
Загальноприйнятим в тиреоїдології є проведення неінвазивного та високоефективного тесту: ультразвукового дослідження області шиї, за допомогою якого можна визначити вузли розмірами від 3 мм, що можуть бути раннім проявом папілярного раку, т.з. папілярною мікрокарциномою. За наявності вузлових утворень необхідно проведення тонкоголкової аспіраційної пункціїйної біопсії (ТАПБ) та подальшому цитологічному дослідженню — «золотого стандарту» в клінічній оцінці вузлових утворень щитоподібної залози.[24] При неінформативній ТАПБ показана відкрита біопсія та експрес-патологогістологічне дослідження. Папілярний рак часто є клінічною знахідкою на фоні доброякісної тиреоїдної патології, зокрема при нетоксичному багатовузловому зобі, тиреоїдиті Хашимото тощо.[16] У зв'язку з цим будь-яке вузлове утворення щитоподібної залози повинно бути обстежене на предмет злоякісного процесу.[25]
Променева діагностика[ред. | ред. код]
- Рентгенографія органів грудної порожнини — може відігравати певну діагностичну роль за наявності метастазів, що найчастіше спостерігаються в легенях.
- Tc-99m-MIBI — сканування з цим радіофармпрепаратом ефективне за наявності радіойоднечутливих метастазів папілярного раку.[26]
- ПЕТ — позитронно-емісійна томографія, найсучасніший метод діагностики пухлин, зокрема радіойоднечутливих метастазів.[16]
Прогноз[ред. | ред. код]
В цілому, папілярний рак характеризується сприятливим прогнозом в більшості випадків, демонструючи 5-річне виживання від 90%[27] до 97%,[28] а 10-річне виживання за деякими даними сягає 93%.[27]
Стадіювання[ред. | ред. код]
Стадіювання папілярного раку здійснюється за системою TNM, тобто з урахування розміру карциноми, наявності локорегіонарних метастазів в лімфатичні вузли та віддалених метастазів.[29]
Лікування[ред. | ред. код]
Хірургічне[ред. | ред. код]

Тотальна тиреоїдектомія та центральна дисекція шиї — ефективний підхід, що забезпечує високі показники виживання та відсутність рецидивів у більшості випадків.
Ад'ювантна терапія[ред. | ред. код]
Ад'ювантна терапія проводиться радіоактивним йодом-131 після проведення радикального хірургічного лікування (тиреоїдектомії) з метою ліквідації окремих тиреоцитів, що все ще можуть залишатися після операції.
Супресія ТТГ[ред. | ред. код]
Супресивна терапія аналогами левотироксину проводиться після радіойодтерапії та направлена на пригнічення продукції тиреотропного гормону (ТТГ), який може викликати стимуляцію окремих нормальних тиреоцитів та клітин ПРЩ, які все ще можуть залишатися навіть після проведеного лікування.[30]
Хіміотерапія[ред. | ред. код]
Проводиться переважно блокаторами тирозин-кінази за наявності віддалених метастазів папілярного раку або при радіойоднечутливих метастазах.
Посилання[ред. | ред. код]
- ↑ Baloch Z. W., Fleisher S., LiVolsi V. A. et al. Diagnosis of "follicular neoplasm": a gray zone in thyroid fine-needle aspiration cytology // Diagnostic Cytopathology — Wiley-Blackwell, 2002. — Vol. 26, Iss. 1. — P. 41–44. — ISSN 8755-1039; 1097-0339 — doi:10.1002/DC.10043
- ↑ Xue H. GABRB2, a key player in neuropsychiatric disorders and beyond // Gene — Elsevier BV, 2022. — Vol. 809. — ISSN 0378-1119; 1879-0038 — doi:10.1016/J.GENE.2021.146021
- ↑ DeLellis R.A., Lloyd R.V., Heitz P.U. End C. (2004). Pathology and Genetics of Tumours of Endocrine Organs (вид. World Health Organization). Lyon: IARC Press. с. 318. ISBN 92-832-2416-7.
{{cite book}}: Cite має пустий невідомий параметр:|переклад=(довідка) (англ.) - ↑ а б Dinets A, Hulchiy M, Sofiadis A, Ghaderi M, Höög A, Larsson C, Zedenius J. (2012). Clinical, Genetic and Immunohistochemical Characterization of 70 Ukrainian Adult Cases with Post-Chornobyl Papillary Thyroid Carcinoma. Eur J Endocrinol. 166: 1049—60. doi:10.1530/EJE-12-0144. PMID 22457234.
- ↑ а б Дінець А. В., Гульчій М. В., Цимбалюк С. М., Олійник О. Б. (2012). Папілярна мікрокарцинома щитоподібної залози: сучасні підходи до діагностики та лікування. Хірургія України. 43 (3): 92—96.
- ↑ Hu MI, Vassilopoulou-Sellin R, Lustig R, Lamont JP. «Thyroid and Parathyroid Cancers» [Архівовано 28 лютого 2010 у Wayback Machine.] in Pazdur R, Wagman LD, Camphausen KA, Hoskins WJ (Eds) Cancer Management: A Multidisciplinary Approach [Архівовано 2013-10-04 у Wayback Machine.]. 11 ed. 2008.
- ↑ а б в Chapter 20 in: Mitchell, Richard Sheppard; Kumar, Vinay; Abbas, Abul K.; Fausto, Nelson. Robbins Basic Pathology. Philadelphia: Saunders. ISBN 1-4160-2973-7. 8th edition.
- ↑ Lin JD (2007). Thyroglobulin and human thyroid cancer. Clin Chim Acta. 388 (1–2): 15. doi:10.1016/j.cca.2007.11.002. PMID 18060877.
- ↑ Tuttle RM, Leboeuf R, Martorella AJ (2007). Papillary thyroid cancer: monitoring and therapy. Endocrinol. Metab. Clin. North Am. 36 (3): 753—78, vii. doi:10.1016/j.ecl.2007.04.004. PMID 17673127.
- ↑ Papotti M, Rodriguez J, De Pompa R, Bartolazzi A, Rosai J (April 2005). Galectin-3 and HBME-1 expression in well-differentiated thyroid tumors with follicular architecture of uncertain malignant potential. Mod. Pathol. 18 (4): 541—6. doi:10.1038/modpathol.3800321. PMID 15529186.
- ↑ а б Shaha AR (2007). TNM classification of thyroid carcinoma. World J Surg. 31 (5): 879—87. doi:10.1007/s00268-006-0864-0. PMID 17308849.
- ↑ Sofiadis A, Dinets A, Orre LM, Branca RM, Juhlin CC, Foukakis T, Wallin G, Höög A, Hulchiy M, Zedenius J, Larsson C, Lehtiö J. (October 2010). Proteomic study of thyroid tumors reveals frequent up-regulation of the Ca2+ -binding protein S100A6 in papillary thyroid carcinoma. Thyroid. 20 (10): 1067-76. doi:10.1089/thy.2009.0400.. PMID 20629554.
{{cite journal}}: Перевірте значення|doi=(довідка) - ↑ Papillary Carcinoma of Thyroid (Hi Pow). University of Connecticut Health Center. Архів оригіналу за 22 липня 2013. Процитовано 14 вересня 2008.
- ↑ Yang GC, Liebeskind D, Messina AV (2001). Ultrasound-guided fine-needle aspiration of the thyroid assessed by Ultrafast Papanicolaou stain: data from 1135 biopsies with a two- to six-year follow-up. Thyroid. 11 (6): 581—9. doi:10.1089/105072501750302895. PMID 11442006.
- ↑ Thyroid, Papillary Carcinoma. Архів оригіналу за 22 липня 2013. Процитовано 15 липня 2010.
- ↑ а б в г The Thyroid and its Diseases. Архів оригіналу за 1 липня 2010. Процитовано 15 липня 2010.
- ↑ Harach HR, Franssila KO, Wasenius VM (1985). Occult papillary carcinoma of the thyroid. A "normal" finding in Finland. A systematic autopsy study. Cancer. 56 (3): 531—8. doi:10.1002/1097-0142(19850801)56:3<531::AID-CNCR2820560321>3.0.CO;2-3. PMID 2408737.
- ↑ Pakdaman MN, Rochon L, Gologan O, Tamilia M, Garfield N, Hier MP, Black MJ, Payne RJ (2008). Incidence and histopathological behavior of papillary microcarcinomas: Study of 429 cases. Otolaryngol Head Neck Surg. 139 (5): 718—22. doi:10.1016/j.otohns.2008.08.014. PMID 18984270.
- ↑ WOOLNER LB, LEMMON ML, BEAHRS OH, BLACK BM, KEATING FR (January 1960). Occult papillary carcinoma of the thyroid gland: a study of 140 cases observed in a 30-year period. J. Clin. Endocrinol. Metab. 20: 89—105. doi:10.1210/jcem-20-1-89. PMID 13845950.
- ↑ Yang GC, Stern CM, Messina AV. (2010). Cystic papillary thyroid carcinoma in fine needle aspiration may represent a subset of the encapsulated variant in WHO classification. Diagn Cytopathol. 38 (10): 721—726. doi:10.1002/dc.21282. PMID 20024942.
- ↑ Nikiforov YE, Seethala RR, Tallini G, Baloch ZW, Basolo F, Thompson LDR, Barletta J, Wenig BM, Ghuzlan AA, Kakudo K, Giordano TJ, Alves VA, Khanafshar E, Asa SL, El-Naggar AK, Gooding WE, Hodak SP, Lloyd RV, Maytal G, Mete O, Nikiforova MN, Nosé V, Papotti M, Poller DN, Sadow PM, Tischler AS, Tuttle RM, Wall KB, LiVolsi VA, Randolph GW, Ghossein RA (14 квітня 2016). Nomenclature Revision for encapsulated follicular variant of papillary thyroid carcinoma: A Paradigm Shift to Reduce Overtreatment of Indolent Tumors. JAMA Oncol. doi:10.1001/jamaoncol.2016.0386. PMID 27078145.
- ↑ Дінець А. В., Фомін П. Д., Гульчій М. В., Олійник О. Б., Цимбалюк С. М., Белан М. В. Клініко-морфологічні особливості папілярної мікрокарциноми щитоподібної залози на фоні хвороби Грейвса. Український медичний частопис. — 2012. // № 3 (89) — с.136-138. [1].
- ↑ Dinets A, Hulchiy M, Sofiadis A, Ghaderi M, Höög A, Larsson C, Zedenius J. (2012). Clinical, Genetic and Immunohistochemical Characterization of 70 Ukrainian Adult Cases with Post-Chornobyl Papillary Thyroid Carcinoma. Eur J Endocrinol. Epub ahead of print. doi:10.1530/EJE-12-0144. PMID 22457234.
- ↑ Papillary Thyroid Carcinoma: An Overview. Archives of Pathology & Laboratory Medicine. 2006. Процитовано 15 липня 2010.
- ↑ Papillary Carcinoma Prognosis. Архів оригіналу за 22 липня 2013. Процитовано 15 липня 2010.
- ↑ Гульчий Н. В., Кущаева Е. С., Макеев С. С., Цымбалюк С. Н., Олейник А. Б. Использование сцинтиграфии с Tc-99м-МИБИ для диагностики заболеваний щитовидной и паращитовидных желез. Український медичний частопис // № 1 (33).- 2003. — с. 43-55.
- ↑ а б Numbers from National Cancer Database in the US, from Page 10 in: F. Grünwald; Biersack, H. J.; Grںunwald, F. (2005). Thyroid cancer. Berlin: Springer. ISBN 3-540-22309-6.
- ↑ Rounded up to nearest natural number from 96,7% as given by eMedicine > Thyroid, Papillary Carcinoma Author: Luigi Santacroce. Coauthors: Silvia Gagliardi and Andrew Scott Kennedy. Updated: Sep 28, 2010
- ↑ cancer.org > Thyroid Cancer [Архівовано 2013-10-18 у Wayback Machine.] By the American Cancer Society. In turn citing: AJCC Cancer Staging Manual (7th ed).
- ↑ Гульчий Н. В., Динец А. В. Особенности гормональной терапии после операций по поводу рака щитовидной железы. Международный эндокринологический журналю // № 1 (42).- 2012. — с. 98-105.
| |||||||||||||||||||||||||
|