Нейроонкологія

Нейроонкологія спеціалізація в Медицина, яка поєднує Неврологія та Онкологія.
Нейроонкологія займається, перш за все, діагностикою, терапією та дослідженням пухлинних захворювань нервової системи, до яких належать наступні види пухлин:
- первинні пухлини центральної нервової системи (пухлини головного мозку та пухлини спинного мозку)
- вторинні пухлини центральної нервової системи (метастази в головний і спинний мозок)
- злоякісні лімфоми центральної нервової системи
- Пухлини периферичної нервової системи
Цей список уже показує, що це широка сфера, яку важко визначити. У той час як лікування лімфом центральної нервової системи також відповідає рекомендаціям щодо гематологічного лікування, а метастази в головний мозок не лікуються окремо від основної терапії первинної пухлини, пухлини периферичних нервів є доброякісними, як і невриноми, і, як і інші пухлини м’яких тканин, часто локалізуються в ортопедична зона.
Загальна інформація[ред. | ред. код]
Первинні пухлини центральної нервової системи[ред. | ред. код]
Первинні пухлини головного мозку можуть виникнути в будь-якому віці, від дитинства до пізнього віку. Такі фактори, як вік, розташування пухлини та клінічна картина, допомагають у диференціальній діагностиці. Більшість типів первинних пухлин головного мозку частіше зустрічаються у чоловіків, за винятком менінгіом, які частіше зустрічаються у жінок.
Метастатичні пухлини центральної нервової системи[ред. | ред. код]
Пряме вторгнення або здавлення безперервних тканин пов’язане з близькістю нервової системи до інших структур.
Внутрішньочерепні метастази[ред. | ред. код]
Розрізняють три типи внутрішньочерепних метастазів: Mетастази в головний мозок, метастази твердої оболонки та менінгеально-лептоменінгеальні метастази. Метастази в мозок можуть бути одиничними або множинними і вражати будь-яку частину мозку. Метастази в структури твердої оболонки зазвичай відбуваються гематогенним шляхом або прямою інвазією з сусідньої кістки. Метастази в твердій мозковій оболонці можуть вражати головний мозок і викликати вогнищевий набряк і пов’язані з ним неврологічні симптоми. Через кортикальне розташування ці відростки, як правило, викликають напади на ранніх стадіях. Лептоменінгеальні метастази є рідкісним, але добре відомим клінічним явищем у хворих на рак. Лептоменінгеальні метастази найчастіше зумовлені первинними пухлинами молочної залози, легенів або меланоми.
черепні метастази[ред. | ред. код]
Метастази в череп поділяються на дві категорії: Cлизову черепа та основу черепа.
Первинні пухлини центральної нервової системи[ред. | ред. код]
Перший підрозділ пухлин центральної нервової системи (ЦНС) відбувається між первинними (походять безпосередньо з ЦНС) і метастатичними (походять з іншого органу) пухлинами. Останні мають захворюваність приблизно в десять разів частіше, ніж перші. Пухлини головного мозку - це новоутворення, що розвиваються в головному мозку. Такі пухлини, як менінгіома, яка своєю масою стискає, але не проникає в мозок, а також пухлини гіпофіза та епіфіза, які розташовані на стовбурі мозку, часто неправильно називають пухлинами мозку. Термін внутрішньочерепні пухлини узагальнює їх більш точно.
Первинні пухлини ЦНС включають різноманітні патологічні утворення, кожна з яких має свою природну історію. Через те, що одних тільки гліальних пухлин налічується майже 40 % цих пухлин, перш за все можна провести розрізнення між гліальними пухлинами (гліомами) і негліальними пухлинами. Найбільш поширеними гліомами є астроцитоми (походять з клітин гліальних астроцитів), олігодендрогліоми (походять з олігодендрогліальних клітин) і епендимоми (походять з епендимальних клітин).
Епідеміологія[ред. | ред. код]
Злоякісні первинні пухлини центральної нервової системи зустрічаються відносно рідко і складають близько 2 відсотків усіх злоякісних новоутворень. Пухлинні захворювання центральної нервової системи розподіляються на 95 відсотків на мозок і до 5 Відсоток на мозкові оболонки, черепні нерви та спинний мозок. Вони можуть виникнути в будь-якому віці, і ризик розвитку захворювання зростає з віком. У дорослих гістологічно можна виявити гліоми, що походять з опорної тканини нервових клітин, з яких близько 75 відсоток гліобластом Астроцитоми IV. ступеня з несприятливим прогнозом. У дітей грудного та раннього віку переважають ембріональні пухлини. У 2016 році в Німеччині захворіло близько 3970 осіб чоловіків і 3460 Жінки зі злоякісними пухлинами центральної нервової системи. В середньому виживаність становить 21 відсотків для чоловіків і 24 відсотків для жінок. Статистика також рідко включає гістологічно доброякісні пухлини ЦНС, які зустрічаються приблизно у 6000 нових випадків пер рік брехні. Близько 65 Відсоток його надходить з мозкових оболонок. Жінки хворіють набагато частіше. Якщо не лікувати за допомогою хірургічного втручання або променевої терапії, навіть доброякісні пухлини можуть бути летальними через прогресуюче зростання в закритому просторі черепа. Найбільш поширеною злоякісною внутрішньочерепною пухлиною ЦНС є гліобластома, з доброякісної – менінгіома.
Етіологія[ред. | ред. код]
Генетична схильність до новоутворень центральної нервової системи зустрічається відносно рідко, хоча деякі гліоми можуть виникати як ускладнення кількох сімейних захворювань.
Мутація деяких генів-супресорів пухлини характеризує кілька спадкових синдромів, які демонструють підвищену схильність до розвитку пухлин мозку. Наступні мутації та їхні синдроми пов’язані з вищим ризиком розвитку пухлин головного мозку: мутація гена NF1 із нейрофіброматозом 1 типу, мутація APC із синдромом Турко, мутація PTCH із синдромом Горліна та мутація TP53 або CHEK2 із синдромом Лі-Фраумені.
Фактори навколишнього середовища, пов'язані з первинними пухлинами мозку, важко визначити. У деяких дослідженнях вплив вінілхлориду було пов’язано зі збільшенням випадків гліоми високого ступеня злоякісності. Єдиною рідкісною, але добре встановленою причиною первинної пухлини мозку є іонізуюче випромінювання. Зокрема, променева терапія дітей з tinea capitis і пацієнтів з гострим лімфатичним лейкозом, краніофарингіомою або неходжкінською лімфомою пов’язана з підвищеним ризиком гліоми. У хворих на СНІД існує підвищений ризик первинної церебральної лімфоми.
Клініка[ред. | ред. код]
ознаки та симптоми[ред. | ред. код]
Симптоми церебральної неоплазії характеризуються зміщенням або Деструкція навколишніх тканин і інфільтрація тих же причин. Найпоширенішим симптомом, про який повідомляють 35 відсотків пацієнтів, є головний біль. Виникнення сильних головних болів у пацієнтів, які в іншому випадку рідко страждають від них, часто є характерним, особливо якщо напади головного болю або мігрені є сильнішими вранці та супроводжуються нудотою, блюванням та неврологічними розладами. У пацієнтів, які частіше страждають від головного болю, зміна форми, почастішання або інтенсивності нападів може бути симптомом розвитку пухлини головного мозку. Судоми виникають приблизно у однієї третини пацієнтів з гліомою, особливо з пухлинами низького ступеня злоякісності або ЦНС. Фокальний неврологічний дефіцит пов’язаний з розташуванням пухлини. Зміни психічного стану також відбуваються у 15-20 відсотків пацієнтів з гліомою.
Візуалізаційна діагностика[ред. | ред. код]

Комп’ютерна томографія (КТ) і магнітно-резонансна томографія (МРТ) дозволяють ефективно виявити новоутворення в головному мозку. МРТ є більш чутливим, ніж КТ, для визначення уражень, але має протипоказання для пацієнтів із кардіостимуляторами, несумісними протезами, металевими кліпсами та ін. КТ залишається методом вибору для виявлення кальцифікатів всередині пошкоджень або кісткових ерозій черепа або основи. Застосування контрастних речовин, які містять йод у разі КТ та парамагнітних ( гадоліній ) у разі МРТ, дозволяє отримати інформацію про васкуляризацію та цілісність гематоенцефалічного бар’єру, краще визначити пухлинну пухлину порівняно з до навколишнього набряку та формування гіпотез про ступінь злоякісності. Рентгенологічне обстеження також дозволяє оцінити механічні впливи та подальші зміни в структурах головного мозку внаслідок пухлини, такі як гідроцефалія та грижа, наслідки яких можуть бути летальними. Нарешті, під час підготовки до операції цю діагностику можна використовувати для визначення локалізації ураження або проникнення пухлини в життєво важливі ділянки мозку. Для цієї мети МРТ є більш ефективним, ніж КТ, оскільки він може забезпечити тривимірні зображення.
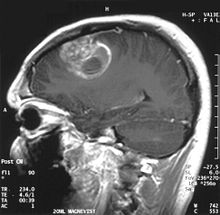
Діагностичні радіологічні інструменти візуалізації підкреслюють зміни в неопластичній тканині порівняно з нормальною паренхімою головного мозку (через зміни щільності тканини в електронному зображенні на КТ та інтенсивності сигналу на МРТ). Як і більшість патологічних тканин, пухлини також можна розпізнати за підвищеним накопиченням внутрішньоклітинної води. На комп’ютерній томограмі вони виглядають гіподенсними, тобто мають меншу щільність, ніж паренхіма головного мозку, на ядерно-магнітно-резонансній томограмі зі спін-ґратковою релаксацією. в спін-спіновому розслабленні а також гіперінтенсивне протонне зважування (PD).
Здорова ділянка мозку не повинна проявляти особливого світіння на рентгенологічному знімку. Тому зрозуміло, що увага приділяється більшим діапазонам контрастного сигналу.
У пухлинній тканині, як правило, більша частка посилення контрасту зумовлена особливим гематогенним бар’єром, який забезпечує проходження йоду (КТ) і гадолінію (МРТ) у внутрішньопухлинний позасудинний інтерстиціальний простір. Це збільшує сигнал (щільність або інтенсивність) пухлини. Однак слід бути обережним, щоб переконатися, що підсилення контрасту не дозволяє остаточно відрізнити неоплазію від навколоранового набряку. Насправді, анатомо-патологічні знахідки в пухлинній тканині злоякісної інфільтрованої гліоми, такої як гліобластома та анапластична астроцитома, також демонструють не тільки вазогенний набряк, спричинений руйнуванням гематоенцефалічного бар’єру пухлиною. Останній клінічний стан погано виявляється за допомогою діагностичних зображень.
Комп’ютерна томографія головного мозку зазвичай показує масу тканини, яка може бути посилена будь-яким контрастом. На КТ гліоми низького ступеня злоякісності зазвичай виглядають рівнощільними до нормальної паренхіми і тому можуть не демонструвати посилення контрасту. Подібним чином ураження задньої черепної ямки важко визначити на КТ. Отже, тільки результатів такої томографії не завжди достатньо для діагностичних цілей. Y сумнівних випадках необхідно використовувати більш чутливу магнітно-резонансну томографію.
Увімкнено - МРТ показує внутрішньочерепну пухлину як масивне ураження, яке може стати більш люмінесцентним після використання контрастної речовини. Однак завжди є аномалія сигналу -Магнітно-резонансна томографія, яка вказує на наявність неоплазії або вазогенного набряку. Як правило, підвищене світіння (підсилення контрасту) свідчить про пухлину вищого ступеня злоякісності. Для гліобластоми характерне контрастне кільце, де люмінесцентна частина відповідає життєво важливій частині злоякісної пухлини, а темніша -hypointense область, що відповідає некрозу тканини.
визначення етапів[ред. | ред. код]
Більшість первинних внутрішньочерепних пухлин залишаються локалізованими в черепі, тому процедури системного визначення стадії не потрібні.
Навпаки, первинні нейроектодермальні пухлини, медулобластоми, пухлини зародкових клітин ЦНС і первинні лімфоми ЦНС часто поширюються через субарахноїдальний простір до лептоменінгів. Тому всім пацієнтам з таким діагнозом також необхідна магнітно-резонансна томографія хребта або люмбальна пункція.
види пухлин[ред. | ред. код]
гліоми[ред. | ред. код]
Первинні пухлини центральної нервової системи (ЦНС) включають різні патологічні тканини, кожна з яких має свою природну історію. У зв’язку з тим, що лише гліоми складають майже 40 відсотків усіх пухлин ЦНС, у літературі прийнято розрізняти гліальні та негліальні пухлини.
Астроцитоми[ред. | ред. код]
З часом у літературі були запропоновані різні системи категорій для класифікації злоякісності астроцитом. З 1993 року найбільш широко використовуваною та застосовуваною є чотирьохрівнева рейтингова система, запропонована Всесвітньою організацією охорони здоров’я (ВООЗ). Він базується на чотирьох гістологічних ознаках: підвищеній щільності клітин, мітозі, проліферації ендотелію та некрозі. Після цього астроцитоми I ступеня, такі як пілоцитарні астроцитоми, зазвичай мають доброякісну гістологію. Астроцитоми II. Ступені (дифузні) показують підвищену щільність клітин як єдину гістологічну ознаку та є новоутвореннями з меншим ступенем інфільтрації. Астроцитоми III демонструють значний мітоз. ступінь (анапластичний). А проліферація або некроз ендотелію спостерігаються в астроцитомах IV. ступеня, так звані гліобластоми.
Низькодиференційовані астроцитоми[ред. | ред. код]

індиПілоцитарні астроцитоми (включаючи піломіксоїдну астроцитому ), субепендимальні гігантоклітинні астроцитоми та плеоморфні ксантастроцитоми входять до числа обмежених пухлин. Це дещо рідші новоутворення доброякісної гістології, які часто можна вилікувати лише хірургічним шляхом. Якщо видалення неповне, пухлинну тканину, що залишилася, можна успішно лікувати за допомогою променевої терапії. У рідкісних випадках, коли місцеве лікування не спрацьовує, може бути успішною системна хіміотерапія, яку необхідно коригувати відуально. Діти реагують на комбінацію карбоплатину та вінкристину.


На комп’ютерній томографії з’являються дифузні астроцитоми ІІ. Ступені, ніж менш інтенсивні ураження. У бажаній магнітно-резонансній томографії контрастні речовини можуть не висвітлити ці новоутворення, їх свічення може бути тоншим і слабшим. Більш інтенсивний може свідчити про підвищену анаплазію тканин. Якщо можливо, пропонується біопсія для отримання зразків анапластичної частини пухлини.
У більшості випадків пацієнти з дифузними астроцитомами мають вік від 20 до 40 років. Для них характерно виникнення епілептичних припадків. Умовами сприятливого прогнозу є молодий вік, розмір пухлини менше 50 міліметрів і максимально широке хірургічне видалення пухлини. Пізні рецидиви зустрічаються відносно часто, тому пацієнти потребують спостереження протягом 15 років після видалення пухлини.
Незважаючи на відносно млявий перебіг, більшість астроцитом прогресують до уражень, що характеризуються великою анаплазією, яка зазвичай не піддається хірургічному втручанню та променевій терапії. Однак терапія пацієнтів з дифузними астроцитомами низького ступеня злоякісності не має одностайної думки в літературі. Роль повної резекції обговорюється в професійному контексті. Результати деяких досліджень показують, що максимальне видалення пухлини дає найкращі результати. Насправді невеликі та односторонні пухлини можна повністю видалити, якщо не задіяні важливі структури мозку. Прагматичний підхід, який загалом прийнятний для загальних випадків, полягає у видаленні неоплазії, наскільки це можливо, щоб уникнути значного неврологічного дефіциту.
Дослідження показали, що променева терапія, призначена відразу після встановлення діагнозу, подовжила період, протягом якого пацієнт не має захворювання до рецидиву пухлини, порівняно з ситуацією, коли курс променевої терапії відкладено до моменту прогресування. Однак наразі немає єдиної думки, що променева терапія незабаром після встановлення діагнозу покращує «загальну виживаність» пацієнта.
У пацієнтів з більш легкими симптомами або без них, або з судомами, які можна контролювати за допомогою протисудомних препаратів, можна відкласти променеву терапію, доки ріст пухлини не досягне критичної фази. Часто виникає бажання зменшити ризик неврологічних пошкоджень, викликаних самою променевою терапією.
Два проспективних рандомізованих клінічних дослідження не показали більшої користі від високодозової радіотерапії, ніж від низькодозової радіотерапії. Зазвичай загальна доза становить від 45 до 54 Грей з фракціонуванням від 1,8 до 2 Греїв.
Ефект ад'ювантної хіміотерапії у пацієнтів з астроцитомами низького ступеня злоякісності все ще досліджується. Попередні результати клінічного випробування, у якому порівнювали лише променеву терапію з променевою терапією з подальшою хіміотерапією, що містить прокарбазин, ломустин і вінкристин (PCV), показали більш тривалий період «виживання без захворювань» із комбінацією, але не подовжену «загальну виживаність». Через токсичність, пов’язану з протоколом PCV, використання темозоломіду рекомендується як у якості початкової терапії, так і після одужання.
Анапластичні астроцитоми[ред. | ред. код]

Анапластична астроцитома - злоякісна пухлина головного мозку, що характеризується дифузним ростом, підвищеною щільністю клітин і фігурами ядерного поділу. Він виникає з популяції специфічних клітин центральної нервової системи, астроцитів. За класифікацією ВООЗ пухлин центральної нервової системи пухлина відповідає III ступеня.
Як правило, пацієнти з анапластичною астроцитомою мають епілептичні припадки, вогнищевий неврологічний дефіцит, головні болі та зміни особистості. Середній вік пацієнтів 45 років. Магнітно-резонансна томографія зазвичай показує масивне ураження з підвищеним контрастним сигналом, який також може бути слабшим. Діагноз ставлять за допомогою гістологічного дослідження ураження шляхом біопсії або хірургічної резекції.
Погіршення прогнозу може бути пов’язане з літнім віком, поганим фізичним станом і значним неврологічним пошкодженням. Загалом терапевтичний результат кращий при повній хірургічній резекції (стандартне лікування) без посилення неврологічного дефіциту. Променева терапія є стандартною, оскільки доведено, що вона збільшує час виживання. Роль хіміотерапії суперечлива.
Гліобластома[ред. | ред. код]

Найбільш поширеними та злоякісними гліальними пухлинами є гліобластоми. Вони складаються з неоднорідної маси низькодиференційованих клітин астроцитоми переважно у дорослих. Зазвичай вони виникають у півкулях головного мозку, рідше в стовбурі головного або спинного мозку. За винятком дуже рідкісних випадків, як і всі пухлини мозку, вони не поширюються за межі структур центральної нервової системи.
Гліобластома може виникнути внаслідок дифузного (II. ступеня) або анапластична астроцитома (III. сорт) розвивати. В останньому випадку він називається вторинним. Однак, якщо це відбувається без попередніх ознак або ознак попередньої злоякісності, його називають первинним. Гліобластоми лікуються хірургічним шляхом, променевою та хіміотерапією. Їх важко вилікувати, і є кілька випадків, які живуть більше трьох років.
Олігодендрогліоми[ред. | ред. код]
Олігодендрогліома - це незвичайна гліальна пухлина головного мозку, яка виникає з олігодендроцитів. Зустрічається переважно у дорослих у віці від 40 до 45 років, переважно в корі головного мозку та білій речовині півкуль головного мозку.
Олігодендрогліоми є відносно рідкісними, вони становлять менше 5 відсотків усіх первинних пухлин головного мозку та не більше 10-15 відсотків усіх гліом. Ці пухлини поділяються на низькодиференційовані та анапластичні ураження. Анапластична олігодендрогліома характеризується підвищеною щільністю клітин, мітозом, проліферацією ендотелію та ядерним поліморфізмом, а також некрозом.
Олігодендрогліоми та олігоастроцитоми низького ступеня злоякісності[ред. | ред. код]
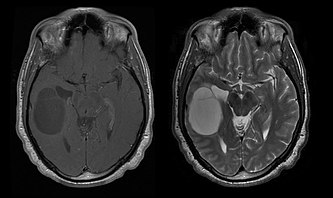
Середня виживаність пацієнтів із чистою олігодендрогліомою становить близько 10 років, з олігоастроцитомою – приблизно 8 років. Подовження порівняно з чистими астроцитомами зумовлено делецією або транслокацією пари 1p/19q у пухлині.
Середній вік пацієнтів на момент встановлення діагнозу – 35 років. Типовими симптомами є епілептичні напади, але також можуть спостерігатися вогнищеві неврологічні порушення, зміни особистості або інші симптоми внутрішньочерепного тиску, такі як головний біль і блювання. Ці пухлини зазвичай не видно на комп’ютерній томографії, тому МРТ є методом вибору для діагностичної візуалізації. На -Магнітно-резонансна томографія, вони розпізнаються як підвищена інтенсивність сигналу. Увімкнено -зображень, з іншого боку, сигнал можна приглушити, а посилення контрасту можна виявити лише зрідка. Може бути відсутнім сигнал кальцифікації.
Ці пухлини прогресують повільніше, ніж астроцитоми низького ступеня злоякісності, і в літературі немає єдиної думки щодо оптимального лікування. Початкове лікування передбачає контроль симптомів за допомогою протисудомних препаратів, опромінення, хіміотерапії або комбінації двох останніх. Хірургія, променева терапія та хіміотерапія відіграють важливу роль у рецидивах. Резекція може полегшити симптоми. На темозоломід показав 50 Відсоток пацієнтів, які рецидивували після променевої терапії, мають позитивну реакцію.
Анапластичні олігодендрогліоми та олігоастроцитоми[ред. | ред. код]
Анапластичні олігодендрогліоми демонструють типові симптоми, що є наслідком мас-ефекту та епілептичних припадків. Незважаючи на їх хіміочутливість, середня виживаність становить лише 3 до 5 років. Лікування передбачає максимальне висічення з подальшою променевою терапією. Стосовно хіміотерапії слід зазначити, що у двох недавніх клінічних дослідженнях III фази порівнювали результати променевої терапії з результатами комбінованої променевої терапії та хіміотерапії прокарбазином, ломустином, вінкристином. Хоча виживаність без відповідних симптомів була довшою при комбінованій терапії, загальна виживаність була однаковою для обох терапій. Пацієнти з делецією 1p/19q досягли найкращих результатів лікування, тоді як пацієнти без делеції 1p/19q змогли покращити свої результати за допомогою хіміотерапії PCV.
Проспективні клінічні дослідження показали, що близько 50 до 70 Відсоток пацієнтів з рецидивом анапластичної олігодендрогліоми після променевої терапії позитивно реагують на хіміотерапію PCV або темозоломідом. Хоча вищої ефективності терапії темозоломідом і PCV не встановлено, відсутність кумулятивної мієлосупресії при застосуванні темозоломіду свідчить про його використання на початку лікування рецидиву.
Епендимоми[ред. | ред. код]

Епендимома — це новоутворення, яке розвивається з епендимальних клітин, що вистилають шлуночки головного мозку, судинне сплетення, кінцеву нитку та центральний канал спинного мозку. Епендимальні клітини також присутні в паренхімі головного мозку в результаті ембріональної міграції з перивентрикулярних областей до кори головного мозку.
Ці досить рідкісні пухлини можуть з'явитися в будь-якому віці, але для них характерні два піки: від 0 до 10 і від 40 до 50 років. Внутрішньочерепні пошкодження, які зазвичай виникають у задній черепній ямці, частіше зустрічаються в першій віковій групі, тоді як травми хребта частіше зустрічаються в другій віковій групі.
Епендимоми поділяються на ураження низького ступеня (I та II. ступінь за шкалою ВООЗ) та анапластичні ураження (III. ступенів) підрозділ. I. ступінь - це, зокрема, субепендимоми та міксопапілярні епендимоми, III. Анапластична епендимома. Пацієнтам з епендимомами хребта низького ступеня злоякісності, які можна повністю видалити, променева терапія після цього не проводиться. Роль післяопераційної променевої терапії при внутрішньочерепних епендимомах низького ступеня злоякісності є суперечливою, але променева терапія зазвичай показана для анапластичних пухлин або пухлин низького ступеня злоякісності, які неможливо повністю видалити.
Клінічні дослідження показали, що епендимоми реагують на хіміотерапію, особливо на основі платини. Перевага хіміотерапії на основі платини становить 67 Відсоток, з іншого боку, 25 для нітрозосечовини Відсоток. Прогноз при епендимомі II. Ступені — 6-річна виживаність без захворювання 68 відсотків і із загальним виживанням 87 Відсоток. При анапластичних епендимомах ці значення падають до 29 відсотків або до 37 Відсоток.
негліальні пухлини[ред. | ред. код]
медулобластоми[ред. | ред. код]
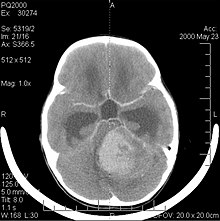
Медулобластома - найпоширеніша злоякісна пухлина головного мозку у дітей. Найбільша захворюваність спостерігається у дітей у віці від 2 до 7 років. Найбільший ризик захворювання залишається в дитячому віці, оскільки медулобластома дуже рідко зустрічається у людей старше 21 року. Ця пухлина характерна для задньої черепної ямки, де вона локалізується в обох півкулях мозочка або в черв’яку мозочка. Оскільки він є інвазивним і швидко зростаючим, він зазвичай поширюється на інші частини центральної нервової системи (ЦНС) через СМР і може проникати в дно найближчого четвертого шлуночка та мозкових оболонок. Рідше можуть виникнути додаткові метастази в ЦНС. Коли виникає злоякісна пухлина, симптоми включають втрату рівноваги, порушення координації, диплопію, дизартрію, а через залучення четвертого шлуночка, що часто призводить до обструктивної гідроцефалії, головний біль, нудоту та блювоту, а також нестійку ходу.
МРТ зазвичай показує масивне контрастне ураження мозочка. Як зазначалося вище, медулобластома має високу схильність до локальної інфільтрації лептоменінгів, а також до поширення через субарахноїдальний простір, залучаючи шлуночки, церебральну опуклість і лептоменінгеальні поверхні хребта. Отже, необхідно привести в резонанс всю черепно-спинномозкову вісь.
Метою хірургічного втручання є видалення якомога більшої частини утворення, представленого ураженням. Фактично, післяопераційні залишкові пухлини призводять до гіршого прогнозу. Також передвісником несприятливого прогнозу є наявність пухлинних клітин в спинномозковій рідині або резонансне виявлення лептоменінгеальних метастазів. Одне тільки хірургічне втручання зазвичай не є лікувальним. У деяких випадках, однак, може бути результатом терапевтичне опромінення черепно-спинномозкової осі, зосереджене на первинному місці пухлини. Додавання хіміотерапії після променевої терапії збільшує відсоток лікування. З вінкристином застосовують препарати на основі платини (цисплатин або карбоплатин), етопозид і алкілуючі речовини (циклофосфамід або ломустин). При належному лікуванні випадки тривалого виживання більше 3 років у пацієнтів з медуллобластомою коливаються від 60 до 60 років. і 80 Відсоток.
Менінгіоми[ред. | ред. код]


Менінгіоми є найпоширенішими внутрішньочерепними зовнішніми або екстрааксіальними пухлинами головного мозку, які виникають із клітин павутинної оболонки, що вистилає головний і спинний мозок. Частота виникнення цієї неоплазії становить близько 2 справ пер рік за 100 000 Резидент. Вони частіше зустрічаються у жінок на шостому та сьомому десятиліттях. Їх частота вища у хворих на нейрофіброматоз 2 типу. Втрата хромосоми 22 є характерним для менінгіом, хоча прогностичне значення цієї знахідки досі неясно.
Пацієнти з менінгіомою можуть мати симптоми, характерні для масивного ураження черепа, включаючи судоми та фокальний неврологічний дефіцит. Оскільки менінгіома також може протікати безсимптомно, її іноді виявляють на комп’ютерній та магнітно-резонансній томографії з інших причин. Ця резонансна пухлина має характерний вигляд, зазвичай складається з рівномірного контрастного посилення вздовж твердої мозкової оболонки з чітким відділенням від паренхіми мозку. Іншою особливістю, хоча й не у всіх випадках, є так званий «хвіст дуральної мозкової оболонки», представлений опуклістю, яка виходить за межі ураження та вказує на точку закріплення в твердій оболонці.
Багато випадково виявлених менінгіом не потребують лікування на момент первинної діагностики. Якщо у пацієнта виявлено значний масовий ефект, незалежно від наявності симптомів чи відсутності, лікуванням вибору зазвичай є повна резекція. У студії Mayo Clinics, яка порівнювала показники контролю пухлини після хірургічної резекції та радіохірургії у пацієнтів із малою та помірною внутрішньочерепною менінгіомою та відсутністю симптомів масового ефекту, радіохірургія призвела до кращого контролю (98 проти 88 відсотків) і з меншою кількістю ускладнень (10 проти 22 відсотків) порівняно з хірургічним видаленням.
Первинні лімфоми ЦНС[ред. | ред. код]

Первинна лімфома центральної нервової системи становить близько 2 відсотків до 3 відсоток усіх пухлин головного мозку у пацієнтів з нормальною імунною системою. Вони частіше зустрічаються у чоловіків старше 55 років до 60 років. Майже половина всіх лімфом виникає у пацієнтів старше 60 років і близько чверті у пацієнтів старше 70 років. років. Здається, що захворюваність зростає з віком, але причина все ще неясна. Пацієнти з ослабленою імунною системою мають вищий ризик розвитку лімфоми ЦНС, тому ті, хто переніс трансплантацію органу, мають вроджений імунодефіцит або аутоімунне захворювання або інфіковані вірусом імунодефіциту людини. ВІЛ-асоційовані лімфоми головного мозку пов’язані з вірусом Епштейна-Барра, особливо у пацієнтів із кількістю лімфоцитів CD4 нижче 500 клітини пер кубічних міліметрів у крові. Більшість лімфом ЦНС є дифузними великоклітинними В-клітинними лімфомами.
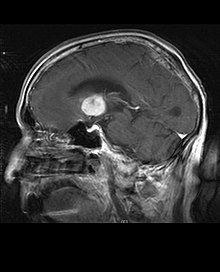
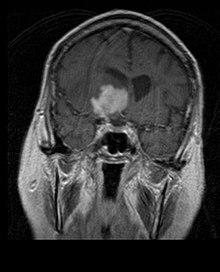
Пацієнти страждають від різноманітних характерних симптомів фокального або мультифокального масивного ураження. МРТ зазвичай показує пухлини з однорідним контрастним посиленням у глибокій перивентрикулярній білій речовині. Багатовогнищевість і неоднорідне посилення характерні для пацієнтів з ослабленою імунною системою. Аналіз лімфоми ЦНС надзвичайно важливий у диференціальній діагностиці новоутворень головного мозку. Слід зазначити, що застосування кортикостероїдів може призвести до повного зникнення посилення, що ускладнить діагностику уражень. Отже, якщо при диференціальній діагностиці слід розглядати лімфому ЦНС, слід уникати кортикостероїдів, якщо масовий ефект не викликає серйозних і негайних проблем у пацієнта.
Біопсія підозрюваного ураження має вирішальне значення. На відміну від системної великоклітинної В-клітинної лімфоми, при якій і хіміотерапія, і променева терапія ефективні, а лікування локалізованих уражень є лікувальним, лімфома центральної нервової системи зазвичай реагує на початкову терапію, але потім рецидивує. Як і у випадку з системною лімфомою, роль хірургічного втручання в основному обмежується отриманням відповідних зразків тканини для діагностики.
У минулому променева терапія проводилася на весь мозок (паненцефалічний). Середня виживаність становить близько 12 навіть при локалізованих ураженнях Місяці. Рецидив зазвичай вражає місце попередньої травми, а також інші області. Відповіді на хіміотерапію є більш обнадійливими. Клінічні випробування, в яких як перше лікування використовували лише високі дози метотрексату, а променеву терапію відкладали до моменту рецидиву або прогресування, показали кращу загальну виживаність, ніж лише променева терапія. Ще більш ефективним виявилося поєднання метотрексату, вінкристину, прокарбазину, інтратекального метотрексату, цитарабіну та паненцефальної променевої терапії та цитарабіну або застосування внутрішньоартеріальної хіміотерапії з внутрішньоартеріальним метотрексатом, внутрішньовенним введенням циклофосфаміду та етопозиду після модифікації крові. мозковий бар'єр з манітом. Середня виживаність при терапії метотрексатом становила 24 до 40 місяців набагато вище, ніж при застосуванні лише променевої терапії (діапазон 24 поки 40 місяців). У деяких випадках променева терапія використовується лише для рецидивів, коли є початковий регрес за допомогою хіміотерапії. Також повідомлялося про випадки тривалого виживання без променевої терапії.
Паненцефальна променева терапія пов'язана з високим ризиком розвитку деменції або лейкоенцефалопатії. Цей ризик можна було б зменшити шляхом розробки ефективних стратегій контролю пухлини, які б уникали паненцефальної променевої терапії. Початкова терапія для пацієнтів з ослабленою імунною системою полягає у зменшенні причин імуносупресії. Прогноз для цих пацієнтів зазвичай гірший, ніж для пацієнтів із нормальною імунною системою. Через супутні пухлинні інфекції та загалом неоптимальний фізичний стан, хіміотерапія часто не може бути проведена цим пацієнтам з імуносупресією. Як і при інших пухлинах головного мозку, відповідь на лікування залежить від віку та фізичного стану.
Метастатичні пухлини центральної нервової системи[ред. | ред. код]
Метастази в мозок[ред. | ред. код]
Метастази в головний мозок є найпоширенішими внутрішньочерепними новоутвореннями у дорослих, у десять разів частіше, ніж первинні пухлини головного мозку. Вони крокують на 20 до 40 відсотків дорослих, хворих на рак, і в основному пов'язані з раком легенів і молочної залози та меланомою. Ці ураження є результатом поширення ракових клітин через кровотік і найчастіше виникають на стику сірої та білої речовини, де змінюється поперечний переріз кровоносних судин, утримуючи емболії пухлинних клітин. 80 відсотків уражень припадає на півкулі головного мозку, 15 відсотків у мозочку і 5 відсотків у стовбурі мозку. Близько 80 відсотків пацієнтів мають в анамнезі системний рак і 70 % мають множинні метастази в мозок.

Останнім часом було досягнуто значних успіхів у діагностиці та лікуванні цих уражень, що призвело до покращення виживання та контролю симптомів. Початок ознак і симптомів подібний до інших масивних уражень головного мозку. Методом діагностики вибору є магнітно-резонансна томографія з контрастною речовиною.
Література показує еквівалентні результати для хірургії та радіохірургії. Останній виявляється зручнішим, ефективнішим і безпечнішим для невеликих уражень або в областях, недоступних для хірургічного втручання. Радіохірургія є розумною альтернативою для пацієнтів, які не можуть бути прооперовані за медичними показаннями. Проте хірургічне втручання є, безумовно, оптимальним методом отримання тканин для діагностики та видалення уражень, які викликають масовий ефект. Тому радіохірургію та хірургію краще розглядати як два взаємодоповнюючі, але різні методи, що застосовуються залежно від різної ситуації пацієнта. Майже на 50 Відсоток пацієнтів з одним або двома метастазами в головний мозок не є кандидатами на хірургічне видалення через недоступність уражень, ступінь системного захворювання або інші фактори. Цим та іншим пацієнтам із множинними метастазами зазвичай пропонують паненцефальну променеву терапію як стандарт лікування. Насправді досягають майже 50 відсотків із них за допомогою цієї терапії покращення неврологічних симптомів і 50 до 70 відсотків помітна реакція. Хіміотерапія рідко використовується переважно для метастазів у мозок.
Для більшості пацієнтів з метастазами в мозок середня виживаність становить лише чотири-шість місяців після паненцефальної променевої терапії. Однак пацієнти віком до 60 років із дискретними ураженнями та контрольованим системним захворюванням можуть досягти довшого виживання, оскільки вони можуть переносити більш агресивний підхід до лікування.
менінгеальні метастази[ред. | ред. код]

Близько 5 відсотка пацієнтів з пухлиною можна діагностувати з метастазами м'якої мозкової оболонки (leptomeninges encephali). Найчастіше вони виникають при меланомі, раку молочної залози і легенів в результаті розповсюдження пухлинних клітин з кровотоком. Потім злоякісні клітини поширюються по центральній нервовій системі (ЦНС), як правило, через спинномозкову рідину, широко відому як мозкова рідина.
Одна або кілька з наступних ознак і симптомів можуть бути спричинені, серед іншого, менінгеальними метастазами:
- місцеві пошкодження нервів, такі як параліч черепних нервів, рухова слабкість і радикулопатії, парестезії та біль,
- пряме вторгнення в тканини мозку або спинного мозку,
- Порушення кровоносних судин головного мозку та хребта з вогнищевим неврологічним дефіцитом та/або судомами,
- Порушення нормального відтоку спинномозкової рідини з головним болем і підвищенням внутрішньочерепного тиску,
- Порушення нормальної функції мозку, такі як енцефалопатія та/або
- периваскулярна інфільтрація пухлинними клітинами з наступними симптомами ішемії та апоплексії.
Діагноз можна поставити за допомогою дослідження спинномозкової рідини або магнітно-резонансної томографії головного і спинного мозку. Наявність злоякісних клітин можна виміряти на 50 відсоток пацієнтів можна визначити. Принаймні 10 % пацієнтів з лептоменінгеальним ураженням цитологічне дослідження залишається негативним. Збільшивши кількість люмбальних пункцій до шести, а кількість видаленої рідини до 10 Мілілітр на пункцію може збільшити можливість позитивного діагнозу. У спинномозковій рідині концентрація білків зазвичай висока, глюкози може бути низькою при наявності плеоцитозу. Рентгенологічне дослідження може виявити гідроцефалію без масивного ураження або дифузного розширення лептоменінгів.
Без терапії середня виживаність становить 4 до 6 тижнів зі смертю внаслідок прогресуючого неврологічного погіршення. Лептоменінгеальні метастази часто є проявом термінальної стадії основного захворювання, і симптоматична терапія може бути найбільш прийнятним рішенням. Кортикостероїди та анальгетики забезпечують тимчасове полегшення. Лікування може бути запропоновано пацієнтам із мінімальним системним захворюванням і прийнятним загальним фізичним станом для полегшення симптомів і продовження виживання.
Середню виживаність можна покращити за допомогою променевої терапії симптоматичних ділянок і більш об’ємних уражених ділянок, виявлених за допомогою рентгена, а також за допомогою інтратекальної терапії метотрексатом, цитарабіном і тіотепою, що виконується за допомогою люмбальної пункції або катетера Ommaya, починаючи з 3 років. на 6 місяців збільшено.
Основним ускладненням інтратекальної терапії на основі метотрексату є некротична лейкоенцефалопатія, яка може розвинутися після місяців терапії у тих небагатьох пацієнтів, які можуть насолоджуватися тривалим виживанням. Цей руйнівний токсичний ефект особливо поширений у пацієнтів, які отримували попередню або супутню променеву терапію з інтратекальною терапією метотрексатом.
біль і термінальний догляд[ред. | ред. код]
Паліативна допомога це особлива форма допомоги, спрямована на покращення якості життя пацієнтів, які страждають від серйозних або небезпечних для життя захворювань, таких як рак. Метою паліативної допомоги є не лікування, а запобігання або лікування якомога раніше симптомів і побічних ефектів хвороби та її лікування, а також пов’язаних із нею психологічних, соціальних і духовних проблем. Паліативна допомога також відома як комфортна допомога, підтримуюча терапія та лікування симптомів. Паліативна допомога надається протягом усього стажу онкологічного захворювання. Зазвичай це починається з діагностики та триває протягом лікування, подальшого спостереження та кінця життя.
Посилання[ред. | ред. код]
- www.cochrane.org/pt/evidence – COCHRANE - Neuro-Oncology Group
- www.eano.eu – European Association of Neuro-Oncology
- https://www.eortc.org/research_field/brain/ – The European Organisation for Research and Treatment of Cancer (EORTC)
Література[ред. | ред. код]
- Jan C. Buckner et al., Central Nervous System Tumors, Mayo Clinic Proceedings, Jg. 82, 2007, lado 1271-1286
- Lisa M. DeAngelis et al., Intracranial Tumors. Diagnosis and Treatment, Dunitz London, 2002, ISBN 1-901865-37-1
- D. N. Louis et al., WHO Classification of Tumours of the Central Nervous System, Genf, 2007, ISBN 978-92-832-2430-3
- Richard Pazdur et al., Cancer management. A multidisciplinary approach. Medical, surgical, & radiation oncology, UBM Medica, 2010, ISBN 978-0-615-41824-7
- Jerome B. Posner, Neurologic Complications of Cancer, Davis, Philadelphia, 1995, ISBN 0-8036-0006-2
- Rüdiger Schenk, Neuroonkologische Therapiekonzepte zur Behandlung von Astrozytomen höheren Malignitätsgrades und Rezidivlokalisation, Regensburg, 2019
- Uwe Schlegel et al., Neuroonkologie, 2. erw., Thieme, Stuttgart, 2003, ISBN 3-13-109062-6
- Jörg-Christian Tonn et al., Oncology of CNS

