Синдром Кавасакі
| Синдром Кавасакі | |
|---|---|
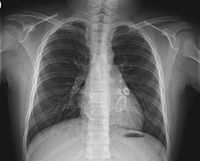 Ураження коронарних судин при синдромі Кавасакі — в тіні серця видно світлі аневризми | |
| Спеціальність | імунологія і педіатр[d] |
| Симптоми | симптом малинового язика, лімфоаденопатія, гарячка, діарея і запалення[1] |
| Препарати | інфліксімаб[2] і ацетилсаліцилова кислота |
| Класифікація та зовнішні ресурси | |
| МКХ-11 | 4A44.5 |
| МКХ-10 | M30.3 |
| OMIM | 611775 |
| DiseasesDB | 7121 |
| MedlinePlus | 000989 |
| eMedicine | med/1223 ped/1236 |
| MeSH | D009080 |
| | |
Синдро́м Каваса́кі або хвороба Кавасакі (англ. Kawasaki syndrome or disease; синоніми — англ. Acute febrile infantile mucocutaneous lymph node syndrome, febrile mucocutaneous lymph node syndrome, mucocutaneous lymph node syndrome) — гостре гарячкове захворювання дитячого віку, ймовірно іммуно-алергічного походження. Характеризується ураженням коронарних та інших судин з можливим утворенням аневризм, тромбозів та розривів судинної стінки. Без адекватного лікування летальність сягає 1 %. Але навіть при інтенсивному лікуванні можлива смерть окремих хворих.
Історичні відомості[ред. | ред. код]
Синдром (хворобу) назвали на честь японського лікаря Томісаку Кавасакі[3], якій вперше побачив у 1961 році в Токійській клініці Червоного Хреста 4-річного хлопчика з такими проявами, що не мали аналогів у медичній літературі того часу, але описав синдром тільки у 1967 році на підґрунті вивчення симптомів вже у 50 хворих дітей.[4] 2 % їх померли від синдрому. У 1974 році він з співавторами надав ще більш розширений опис синдрому.[5] У 1976 році на Гавайях американський лікар М. Меліш вперше в США описав 12 випадків синдрому серед місцевих дітей.[6]
Актуальність[ред. | ред. код]
Синдром Кавасакі на 2018 рік виявляється в усьому світі, хоча найбільше число випадків зареєстровано в Азії. Синдром є основною причиною набутої хвороби серця у дітей в розвинених країнах світу і може бути в подальшому фактором ризику розвитку ішемічної хвороби серця у 25 % дорослих, що перенесли його. У Сполучених Штатах Америки синдром Кавасакі спостерігають у 3000 дітей щорічно, він перевершив за частотою гостру ревматичну гарячку як причину набутих вад серця в дітей у віці до 5 років. На 100 000 дітей, молодших 5 років, припадає 90 % всієї вікової захворюваності, етнічно 32,5 випадків відбуваються в американців азійського походження або вихідців з островів Тихого океану, 16,9 — африканського походження, 11,1 — південноамериканського походження та 9,1 — у білих. У Японії, Тайвані та Кореї захворюваність сягає 6000 випадків за рік, найчастіше протягом січня-червня. В Японії ризик виникнення синдрому в десятки разів вищий ніж у країнах Заходу. Епідемії синдрому відзначені в цій країні 1979, 1982 та 1985 років. Співвідношення уражених хлопчиків до дівчат 1.3-1.83:1[7].
Етіологія[ред. | ред. код]
Інфекційний фактор[ред. | ред. код]
Етіологія невідома. Основною гіпотезою виникнення синдрому вважають дію стафілококових та стрептококових суперантигенів, які стимулюють популяцію Т-лімфоцитів, що призводить до розвитку імунних реакцій, які пошкоджують ендотеліальні клітини. Про це свідчить певна кількість проведених епідеміологічних та імунологічних досліджень. Особливості епідеміологічного поширення синдрому свідчать про виникнення спалахів, перш за все, в кінці зими і навесні з інтервалом 3 роки і хвилеподібного географічного поширення цих спалахів. До інфекційних ознак синдрому належать характерні для інфекційних хвороб гарячка, лімфаденопатія і очні симптоми. Синдром Кавасакі є незвичайним для немовлят у віці до 4-х місяців, припускають, що материнські антитіла можуть забезпечувати їм пасивний імунітет. Епідеміологічні дані свідчать, проте, що від людини до людини передача цього синдрому малоймовірна. Є припущення, що допомагають реалізувати інфекційні фактори в генезі синдрому деякі побутові засоби: килимовий шампунь, зволожувачі повітря, тощо.[8] Є також припущення, що для реалізації синдрому потрібна наявність біля хворого певних мас неводопровідної води (водойми, басейни, тощо). Деякі проведені дослідження показали, що при синдромі Кавасакі відбувається вироблення олігоклональних антитіл, а не поліклональних, як це відбувається у відповідь на суперантигени, що мало б бути, якщо саме ці антигени були етіологічним фактором синдрому.[9] Станом на 2015 рік немає свідчень, що якийсь інфекційний фактор випливає як ведуча причина виникнення синдрому. Виявили, що такими факторами є[10]:
- Yersinia pseudotuberculosis;[11][12]
- парвовірус В19;
- менінгокок;
- бактеріальні суперантигени стафілококів та стрептококів;
- Mycoplasma pneumoniae;
- Klebsiella pneumoniae;
- аденовіруси;
- цитомегаловірус;
- вірус парагрипу типу 3;
- ротавіруси;
- вірус кору;
- вірус Епштейна — Барр;
- людський лімфотропний вірус;
- збудники кліщових хвороб;
- деякі види рикетсій;
- Propionibacterium acnes.
Є припущення, яке ґрунтують на факті виявлення при електронній та оптичній мікроскопії у 85 % хворих, які померли від синдрому Кавасакі, цитоплазматичних тілець, що містять РНК. Такі ж тільця виявили в 25 % дітей з контрольної групи, що не мали синдрому. Висунули гіпотезу, що ці тільця належать невідомому РНК-вмісному вірусу, що є широко поширеним серед дітей і спричинює у більшості малосимптомну чи, взагалі, безсимптомну інфекцію, тоді як у генетично сприйнятливих людей виникає синдром Кавасакі. Автори продовжують пошук цього вірусу.[13]
Генетичні фактори[ред. | ред. код]
Також певну роль віддають автоімунним реакціям та генетичним факторам.[14] Виявили, що у братів, сестер постраждалих дітей у 10-20 разів вища ймовірність розвитку синдрому Кавасакі, ніж серед населення в цілому. Японські діти, чиї батьки хворіли свого часу на хворобу Кавасакі, можуть хворіти на тяжчу форму захворювання і бути більш сприйнятливими до рецидиву.[15] Цей ризик 2 членів сім'ї, що мають хвороби Кавасакі є найбільшим для близнюків, для яких цей показник становить близько 13 %.[16] Проведені дослідження показали, що відповідальним за синдром є HLA-Bw22J2, який представляє собою антиген головного комплексу гістосумісності, що відзначали переважно в японських популяціях, тим самим ще більше відзначаючи генетичний вплив на підвищену сприйнятливість до синдрому Кавасакі у японських пацієнтів.[17] Аналіз багатоточкового зв'язку показав докази того, що для виникнення синдрому мають бути проблеми у хромосомі 12 (локус 12q24).[18] Описали також декілька сімей з кількома членами, які страждали на синдром Кавасакі. У цих сім'ях ураження мали місце в 2-х поколіннях або у декількох братів і сестер. Таким чином, генетичні фактори, поліморфні алелі, ймовірно, впливають на сприйнятливість до синдрому.
Є повідомлення, що у деяких хворих синдром розвинувся після вакцинації, зокрема після введення ротавірусної та проти гепатиту В вакцин.
Патогенез[ред. | ред. код]
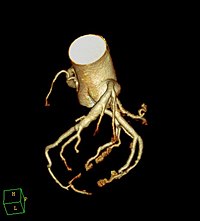
Усі питання патогенезу на сьогодні не є розв'язаними. Вважають, що внаслідок первинних імунних реакцій відбувається запалення судин — васкуліт. Він при синдромі Кавасакі пошкоджує переважно артерії середнього калібру. Розщеплення зовнішньої та внутрішньої еластичних мембран коронарних судин серця призводить до розвитку аневризм. Інтима потовщується, просвіт судини звужується і там можуть утворитися тромби. Незважаючи на те, що запалення найбільш яскраво виражене в коронарних судинах, васкуліт може також виникати у венах, капілярах, дрібних артеріолах та артеріях великого калібру.
Рання стадія[ред. | ред. код]
На ранніх стадіях захворювання, ендотеліальні клітини і основа судин набряклі, але внутрішня еластична пластинка залишається неушкодженою. Потім, приблизно через 7-9 днів від початку гарячки, відбувається приплив нейтрофілів, який швидко супроводжується поширенням CD8+ цитотоксичних лімфоцитів та імуноглобулін А-продукуючих плазматичних клітин.
Запальні клітини секретують різні цитокіни, інтерлейкіни і матричні металопротеїнази, які націлені на ендотеліальні клітини і призводять до каскаду подій, які проявляються у фрагментації внутрішньої еластичної пластинки і повному пошкодженні судин. У сильно постраждалих судини розвивається запалення з некрозом клітин гладкої мускулатури, пошкодженням усіх 3-х шарів судинної стінки. Внутрішній і зовнішній шари еластичної пластинки можуть відділитися одне від одного, що призводить до аневризми.
Розвинута стадія[ред. | ред. код]
Протягом наступних кількох тижнів до кількох місяців, активні запальні клітини замінюються фібробластамии і моноцитами, що призводить до формування волокнистої сполучної тканини всередині стінки судини. У дрібних судинах також накопичуються еозинофіли, що є свідченням того, що у запальних реакціях є компонент алергічного, бо еозинофіли знешкоджують гістамін та володіють протизапальними властивостями. Інтима судини проліферується і потовщується. Стінки судин, зрештою, звужуються, може відбутися їхня оклюзія, іноді не тільки через стеноз, але й тромбоз. Серцево-судинна смерть може статися від інфаркту міокарда або від розриву великої аневризми. Збільшення кількості тромбоцитів у периферичній крові відповідає найбільшому ризику смерті від тромбозу при синдромі Кавасакі. В інших органах подальші зміни не відбуваються.
Клінічні ознаки[ред. | ред. код]
Класифікують синдром Кавасакі у Міжнародному класифікаторі хвороб 10-го перегляду як «Шкірно-слизовий та лімфаденітний синдром (Кавасакі)» (англ. Mucocutaneous lymph node syndrome [Kawasaki]) (М30.3).

Рання стадія[ред. | ред. код]
Вона починається з раптової появи гарячки і триває в середньому близько 7-14 днів. Гарячка, як правило, є в межах 39-40 °C або вище. Вона не припиняється при призначенні антибіотиків або жарознижувальних засобів і може зберігатися до 3-4 тижнів, якщо хворобу не лікувати адекватно. При відповідній терапії, яка включає високі дози ацетилсаліцилової кислоти і внутрішньовенного імуноглобуліну, гарячка, як правило, зникає протягом 48 годин. На додаток до неї, ознаки та симптоми цієї стадії можуть включати наступні:
- Збудження.
- Неексудативний двобічний кон'юнктивіт (90 %).
- Передній увеїт (70 %).
- Періанальна еритема (70 %).
- Еритема і набряки на руках і ногах; останній перешкоджає вставанню.
- Малинові / полуничні язик і губи.
- Печінкові, ниркові ушкодження та дисфункція шлунково-кишкового тракту.
- Міокардит і перикардит.
- Збільшення лімфатичних вузлів (75 %), як правило, поодинокі, негнійні шийні вузли розміром приблизно до 1,5 см.
Діагноз має бути поставлений у цій стадії.
Розгорнута стадія[ред. | ред. код]
Ця стадія починається тоді, коли стихає гарячка. Стадія триває до 4-6 тижнів. Відмінними рисами цього етапу є лущення шкіри, тромбоцитоз (кількість тромбоцитів може перевищувати 1 млн / мкл), а також розвиток коронарних аневризм. Ризик раптової смерті є найвищим на цьому етапі. Відзначають на цій стадії також стійку дратівливість, анорексію і продовження кон'юнктивіту. Повернення гарячки за 2-3 тижні може бути ознакою рецидиву. Якщо гарячка зберігається, прогноз для життя є менш сприятливим через великий ризик тяжких серцево-судинних ускладнень.
Більшість випадків рецидивів синдрому відбуваються протягом 2-х років з моменту першого епізоду. Найвищі шанси до рецидиву мають діти до 1 року і ті, хто мав ускладнення з боку серця при першому епізоді.
Ускладнення[ред. | ред. код]
- Ускладнення з боку ССС: інфаркт міокарду, вальвуліт, міокардит, розриви аневризм з розвитком гемоперикарду.
- Інші ускладнення: асептичний менінгіт, артрит, середній отит, водянка жовчного міхура, діарея, периферична гангрена.
Прогноз[ред. | ред. код]
За відсутності лікування летальність досягає 1 %, у дітей у віці до 1 року може перевищувати 4 %. Пік смертності відбувається через 15-45 днів після початку гарячки. У дорослих не зареєстрували жодного випадку смерті від цього синдрому. У нелікованих хворих аневризми коронарних артерій розвиваються в 25 % випадків. Фактори ризику виникнення аневризм включають:
- гарячка протягом більш ніж 16 днів;
- рецидив гарячки після періоду її відсутності тривалістю не менше 48 годин;
- чоловіча стать;
- кардіомегалія (збільшення серця);
- вік молодше 1 року.
Лікування в/в імуноглобуліном знижує ризик розвитку аневризм до 10 %. Спонтанну регресію аневризм вінцевих судин спостерігають у половини пацієнтів, однак ризик коронарних подій у них залишається таким самим високим, як у пацієнтів з персистуючими аневризмами. Пізнє встановлення діагнозу та відповідно запізніле лікування є також важливим фактором ризику аневризм.
Показано, що у 50 % тих дітей, в яких аневризма не утворилась, спостерігають зниження функції лівого шлуночка і / або легку клапанну регургітацію на ехокардіографії. Найбільший ризик пошкодження серця є у дітей у віці до 1 року і старших від 5 років, що може бути пов'язано з нетиповим клінічним перебігом в таких випадках, що призводить до затримки у лікуванні.
Діагностичні критерії[ред. | ред. код]
| Зауважте, Вікіпедія не дає медичних порад! Якщо у вас виникли проблеми зі здоров'ям — зверніться до лікаря. |
Клінічні критерії діагнозу синдрому[ред. | ред. код]
Для постановки діагнозу синдрому Кавасакі необхідна наявність гарячки більше 5 днів і будь-яких 4 нижчеперелічених критеріїв:
- Двобічна кон'юнктивальна ін'єкція;
- Зміни на губах або в порожнині рота: «малиновий / полуничний» язик, еритема або тріщини на губах, ін'єктованість слизової порожнини рота і глотки
- Будь-які з перерахованих змін, локалізовані на кінцівках
- Еритема долонь або стоп
- Щільний набряк кистей або стоп на 3-5-й день хвороби
- Лущення шкіри на кінчиках пальців на 2-3-му тижні захворювання
- Поліморфна екзантема на тулубі без пухирців або кірочок
- Гостра негнійна шийна лімфаденопатія (діаметр одного лімфатичного вузла >1,5 см).
Якщо відсутні 2-3 з 4 обов'язкових ознак хвороби, встановлюється діагноз неповної клінічної картини захворювання.
Лабораторні критерії розвитку аневризми[ред. | ред. код]
Такими вважають:
- рівень гематокриту менший 35 %;
- кількість тромбоцитів менша за 35х109/л;
- рівень лейкоцитів більший за 12х106/л.
- високий рівень С-протеїну;
- рівень альбуміну менший за 35 г/л;
Лікування[ред. | ред. код]
Метою лікування синдрому є зменшення рівня запалення та активації тромбоцитів. Рання та агресивна (настійлива) терапія явно покращує прогноз.
Стандартне лікування[ред. | ред. код]
Включає внутрішньовенний імуноглобулін (IVIG) для лікування запалення і для запобігання наслідків ураження коронарних судин. Ацетилсаліцилова кислота традиційно була частиною стандартного лікування. Більшість лікарів використовують високі дози її різною тривалістю, а потім більш низькі дози через її антитромбоцитарні ефекти. Абсорбція ацетилсаліцилової кислоти при прийомі всередину може зменшуватися при синдромі Кавасакі до <50 % (в порівнянні з типовою біодоступністю 85-90 %). Зменшення біодоступності є причиною того, що більш високі дози необхідні для досягнення ефекту. Ібупрофена в лікуванні саме синдрому Кавасакі слід уникати.
Нестандартне лікування резистентного та ускладненого перебігу[ред. | ред. код]
Інші антикоагулянти або антиагреганти (наприклад, варфарин, дипіридамол) використовують значно рідше, переважно при виникненні великих аневризм. Глюкокортикостероїди (преднізолон, метилпреднізолон) використовують, як правило, у тих пацієнтів, які не зреагували на стандартні методи лікування. Їх використання на первинному етапі є спірним. Лікування імуноглобуліном разом з метотрексатом або циклофосфамідом було ефективним при тих випадках синдрому, який є резистентним для стандартного лікування. Також в такій ситуації рекомендують інфліксімаб.
За умови виникнення великих аневризм проводять інтервенційну катетеризацію серця, вводять тромболітики. Оскільки існує ймовірність алергічних ускладнень при застосуванні стрептокінази у хворих, у яких був стрептококовий фарингіт протягом останніх 6 місяців і тому, що пусковим фактором синдрому Кавасакі залишається неясним, цього препарату краще уникати. Інші препарати цієї категорії, такі, як тканинний активатор плазміногену, активізатор тенектеплази і урокіназа можуть більше стати в пригоді.
Про плазмоферез говорять як про ефективний метод лікування пацієнтів з синдромом Кавасакі. [джерело?]
Профілактика несприятливого перебігу синдрому[ред. | ред. код]
Слід довести до відома пацієнта і його сім'ї, що синдром Кавасакі є потенційно смертельним, що він може рецидивувати. Слід наголошувати на необхідності постійного догляду, якщо виникли серцеві ураження. Необхідно вимагати продовження антикоагулянтної терапії, зокрема ацетилсаліциловою кислотою, доти, поки її не припинить лікар. Батьки та інші вихователі повинні розуміти необхідність тісного педіатричного і кардіологічного спостереження, поки хвороба повністю не закінчилась. Лікарі також мають повідомити сім'ю захворілого про потенційний підвищений ризик синдрому Кавасакі серед інших дітей сім'ї. Через необхідність тривалого прийому ацетилсаліцилової кислоти дітьми у гострий період синдрому необхідно провести вакцинацію проти грипу та вітряної віспи.
Смерть Джетта Траволти[ред. | ред. код]
Випадком, який був начебто пов'язаним з синдромом Кавасакі та отримав найбільш широкого розголосу, став випадок смерті Джетта Траволти, що є рідним сином відомого голлівудського актора та режисера Джона Траволти та Келлі Престон.
Джетт Траволта помер 2 січня 2009 від травми, отриманої внаслідок втрати рівноваги у ванній кімнаті, імовірно, у зв'язку з епілептичним нападом. Лікарі не змогли врятувати життя старшого сина Траволти. Відомо, що у дворічному віці у Джетта діагностували синдром Кавасакі. Хоча начебто прямого зв'язку між смертю і перенесеною в дитинстві хворобою немає, але такий факт мав місце.
Примітки[ред. | ред. код]
- ↑ Disease Ontology — 2016.
- ↑ Drug Indications Extracted from FAERS — doi:10.5281/ZENODO.1435999
- ↑ Whonamedit?- A dictionary of medical eponyms. Kawasaki's disease. Архів оригіналу за 18 вересня 2016. Процитовано 29 липня 2016.
- ↑ Kawasaki T. «Acute febrile mucocutaneous syndrome with lymphoid involvement with specific desquamation of the fingers and toes in children: clinical observation of 50 cases». Japan Journal of Allergology March 1967, 16 (3): 178—222.
- ↑ T. Kawasaki, F Kosake, S Okawa, I Shigematsu, and H. L. Yanagawa: A new infantile acute febrile mucocutaneous lymph node syndrome (MLNS) prevailing in Japan. Pediatrics, Evanston, Illinois, 1974, 54: 271-6.
- ↑ Melish ME, Hicks RM, Larson EJ. Mucocutaneous lymph node syndrome in the United States. Am J Dis Child. 1976 Jun. 130(6):599-607.
- ↑ Kawasaki Disease [1] [Архівовано 29 травня 2020 у Wayback Machine.] (англ.)
- ↑ Treadwell TA, Maddox RA, Holman RC, Belay ED, Shahriari A, Anderson MS, et al. Investigation of Kawasaki syndrome risk factors in Colorado. Pediatr Infect Dis J. 2002 Oct. 21(10):976-8.
- ↑ Leung DY, Meissner HC, Fulton DR, Murray DL, Kotzin BL, Schlievert PM. Toxic shock syndrome toxin-secreting Staphylococcus aureus in Kawasaki syndrome. Lancet. 1993 Dec 4. 342(8884):1385-8.
- ↑ Yanagawa H, Nakamura Y, Yashiro M, Ojima T, Tanihara S, Oki I, et al. Results of the nationwide epidemiologic survey of Kawasaki disease in 1995 and 1996 in Japan. Pediatrics. 1998 Dec. 102(6): E65.
- ↑ Vincent P, Salo E, Skurnik M, et al. Similarities of Kawasaki disease and Yersinia pseudotuberculosis infection epidemiology. Pediatr Infect Dis J. 2007 Jul. 26(7):629-31.
- ↑ Tahara M, Baba K, Waki K, et al. Analysis of Kawasaki disease showing elevated antibody titres of Yersinia pseudotuberculosis. Acta Paediatr. 2006 Dec. 95(12):1661-4.
- ↑ Rowley AH, Shulman ST. Pathogenesis and management of Kawasaki disease. Expert Rev Anti Infect Ther. 2010 Feb. 8(2):197-203.
- ↑ Onouchi Y. Susceptibility genes for Kawasaki disease. Nihon Rinsho. 2014 Sep. 72(9):1554-60.
- ↑ Uehara R, Yashiro M, Nakamura Y, Yanagawa H. Clinical features of patients with Kawasaki disease whose parents had the same disease. Arch Pediatr Adolesc Med. 2004 Dec. 158(12):1166-9.
- ↑ Mason WH, Takahashi M, Schneider T. Recurrence of Kawasaki disease in a large urban cohort in the United States. In: Takahashi M, Taubert K, eds. Proceedings of the Fourth International Symposium on Kawasaki Disease. Dallas, Tex: American Heart Association; 1993:21-6.:
- ↑ Kato S, Kimura M, Tsuji K, Kusakawa S, Asai T, Juji T, et al. HLA antigens in Kawasaki disease. Pediatrics. 1978 Feb. 61(2):252-5.
- ↑ Onouchi Y, Tamari M, Takahashi A, Tsunoda T, Yashiro M, Nakamura Y, et al. A genomewide linkage analysis of Kawasaki disease: evidence for linkage to chromosome 12. J Hum Genet. 2007. 52(2):179-90.
Джерела[ред. | ред. код]
- Noah S Scheinfeld, Steven J Parrillo, Paul R Ogershok, Elena L Jones Kawasaki Disease Updated: Sep 13, 2015 Medscape / Pediatrics: General Medicine Articles / Infectious Diseases (Chief Editor Russell W Steele) [2] [Архівовано 10 серпня 2016 у Wayback Machine.] (англ.)
- Burns JC, Glodé MP. Kawasaki syndrome. Lancet. 2004 Aug 7-13. 364(9433):533-44. (англ.)
- Melish ME, Hicks RV. Kawasaki syndrome: clinical features. Pathophysiology, etiology and therapy. J Rheumatol Suppl. 1990 Sep. 24:2-10. (англ.)
- Jane W. Newburger, Masato Takahashi, Michael A. Gerber, Michael H. Gewitz, Lloyd Y. Tani, Jane C. Burns, Stanford T. Shulman, Ann F. Bolger, Patricia Ferrieri, Robert S. Baltimore, Walter R. Wilson, Larry M. Baddour, Matthew E. Levison, Thomas J. Pallasch, Donald A. Falace and Kathryn A. Taubert Diagnosis, Treatment, and Long-Term Management of Kawasaki Disease Circulation October 26, 2004, Volume 110, Issue 17 (англ.)
Посилання[ред. | ред. код]
| Вікісховище має мультимедійні дані за темою: Синдром Кавасакі |
- Синдром Кавасакі, наочна анімація [Архівовано 31 жовтня 2012 у Wayback Machine.]
- Синдром Кавасакі [Архівовано 2 березня 2014 у Wayback Machine.]
- Хвороба Кавасакі може поширюватися по повітрю
- Хвороба Кавасакі у фотографіях [Архівовано 2 березня 2014 у Wayback Machine.]
|