Розподіл Максвелла — Больцмана: відмінності між версіями
| [неперевірена версія] | [неперевірена версія] |
Addbot (обговорення | внесок) |
Kirsim (обговорення | внесок) Немає опису редагування |
||
| Рядок 1: | Рядок 1: | ||
{{Розподіл ймовірностей| |
|||
name = Розподіл Максвелла — Больцмана| |
|||
type = pdf| |
|||
pdf_image = [[Image:Maxwell-Boltzmann distribution pdf.svg|325px]]| |
|||
cdf_image =[[Image:Maxwell-Boltzmann distribution cdf.svg|325px]]| |
|||
parameters =<math>a>0\,</math>| |
|||
support =<math>x\in [0;\infty)</math>| |
|||
pdf =<math>\sqrt{\frac{2}{\pi}} \frac{x^2 e^{-x^2/(2a^2)}}{a^3}</math>| |
|||
cdf =<math>\textrm{erf}\left(\frac{x}{\sqrt{2} a}\right) -\sqrt{\frac{2}{\pi}} \frac{x e^{-x^2/(2a^2)}}{a},</math> де ''erf'' — [[функція помилок]] | |
|||
mean =<math>\mu=2a \sqrt{\frac{2}{\pi}}</math>| |
|||
median =| |
|||
mode =<math>\sqrt{2} a</math>| |
|||
variance =<math>\sigma^2=\frac{a^2(3 \pi - 8)}{\pi}</math>| |
|||
skewness =<math>\gamma_1=\frac{2 \sqrt{2} (16 -5 \pi)}{(3 \pi - 8)^{3/2}}</math>| |
|||
kurtosis =<math>\gamma_2=4\frac{(-96+40\pi-3\pi^2)}{(3 \pi - 8)^2}</math>| |
|||
entropy =<math>\frac{1}{2}-\gamma-\ln(a\sqrt{2\pi})</math>| |
|||
mgf =| |
|||
char =| |
|||
}} |
|||
'''Розпо́діл Ма́ксвелла — Бо́льцмана''' визначає ймовірність того, що частинка [[ідеальний газ|ідеального газу]] перебуває в стані з певною [[енергія|енергією]]. |
'''Розпо́діл Ма́ксвелла — Бо́льцмана''' визначає ймовірність того, що частинка [[ідеальний газ|ідеального газу]] перебуває в стані з певною [[енергія|енергією]]. |
||
Версія за 17:15, 28 червня 2013
| Розподіл Максвелла — Больцмана | |
|---|---|
|
Щільність розподілу 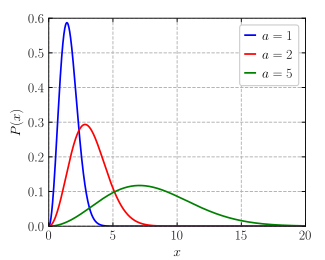 | |
|
Функція розподілу ймовірностей  | |
| Параметри | |
| Носій функції | |
| Розподіл імовірностей | |
| Функція розподілу ймовірностей (cdf) | де erf — функція помилок |
| Середнє | |
| Мода | |
| Дисперсія | |
| Коефіцієнт асиметрії | |
| Коефіцієнт ексцесу | |
| Ентропія | |
Розпо́діл Ма́ксвелла — Бо́льцмана визначає ймовірність того, що частинка ідеального газу перебуває в стані з певною енергією.
Ймовірність того, що частинка перебуває в стані з енергією згідно з розподілом Больцмана визначається формулою:
- ,
де μ — хімічний потенціал, T — температура, kB — стала Больцмана.
Хімічний потенціал μ визначається з умови
де N — число частинок.
Розподіл Больцмана справедливий тільки в тих випадках, коли . Ця умова реалізується при високих температурах.
Граничний випадок квантовомеханічних розподілів
В квантовій статистиці розподіли для ферміонів і бозонів мають різний вигляд і різні властивості. Проте при високій температурі, коли ймовірність знайти частку в будь-якому стані набагато менша за одиницю, як розподіл Фермі-Дірака так і розподіл розподіл Бозе-Ейнштейна переходять в розподіл Больцмана.
Розподіл Больцмана в класичній статистиці
В класичній статистиці частка ідеального газу має лише кінетичну енергію.
Число часток з імпульсами в проміжку визначається формулою:
- ,
де m — маса частки.
У випадку коли дана формула виражена через швидкості, а не через імпульси, вона носить назву розподілу Максвелла
- .
Розподіл Больцмана в зовнішньому потенціальному полі
У випадку, коли частки ідеального газу перебувають у зовнішньому полі з потенціалом , це збільшує їхню енергію. В такому випадку, розподіл Больцмана визначає залежну від координати густину часток:
- .
Зокрема, у випадку газу в полі тяжіння Землі це співвідношення визначає барометричну формулу
- .
Аналогічні формули справедливі для розподілу густини носіїв заряду (електронів чи дірок) у електричному полі в напівпровідникових приладах.
Див. також
- Статистика Фермі-Дірака
- Статистика Бозе-Ейнштейна
- Розподіл Максвелла молекул ідеального газу за швидкостями
Джерела
- Ландау Л.Д., Лившиц Е.М. (1976). Теоретическая физика. т. V. Статистическая физика. Часть 1 (російська) . Москва: Наука.



















