Суперантиген



Суперантігени (СА) представляють собою клас антигенів, які призводять до надмірної активації імунітету. Зокрема, це викликає неспецифічну активацію Т-клітин, що призводить до поліклональної активації Т-клітин і масованого вивільнення цитокінів. SAgs виробляються деякими патогенними вірусами та бактеріями, швидше за все, як захисний механізм проти імунної системи.[1] У порівнянні з нормальною антиген-індукованою Т-клітинною відповіддю, коли активовано 0,0001-0,001% Т-клітин організму, SAg здатні активувати до 20% Т-клітин організму.[2] Крім того, антитіла до CD3 і CD28 (CD28-SuperMAB) також виявились високоефективними суперантигенами (і можуть активувати до 100% Т-клітин).
Велика кількість активованих Т-клітин викликає масивну імунну відповідь, яка не є специфічною для жодного конкретного епітопу на SAg, таким чином підриваючи одну з фундаментальних сильних сторін адаптивної імунної системи, тобто її здатність націлюватися на антигени з високою специфічністю. Що ще важливіше, велика кількість активованих Т-клітин секретують велику кількість цитокінів, найвагомішим з яких є гамма-інтерферон. Його надлишкова кількість, у свою чергу, активує макрофаги. Активовані макрофаги, у свою чергу, надмірно виробляють прозапальні цитокіни, такі як IL-1, IL-6 і TNF-альфа. TNF-альфа особливо важливий як частина запальної реакції організму. За звичайних обставин він виділяється локально в низьких рівнях і допомагає імунній системі перемогти патогени. Однак, коли він системно виділяється в кров і у високих рівнях (через масову активацію Т-клітин у результаті зв’язування SAg), він може викликати серйозні та небезпечні для життя симптоми, включаючи шок та поліорганну недостатність.
Структура[ред. | ред. код]
SAg виробляються бактеріями і вивільняються при інфекції у формі позаклітинних зрілих токсинів.[3]
Послідовності цих токсинів відносно стабільні серед різних підгруп. Більш важливо, ніж гомологія послідовності, що 3D-структура дуже схожа у різних SAg, що призводить до подібних функціональних ефектів.[4][5]
Кристалічні структури цих ентеротоксінов показують, що вони є компактними, еліпсоїдальними білками, які мають характерний дводоменний складний патерн, що містить NH2-кінцевий β-глобулярний домен відомий як комплекс олігосахарид/олігонуклеотид, довгу альфа-спіраль, що по діагоналі охоплює центр молекули і кінцевий глобулярний домен COOH.[4]
Домени мають ділянки зв’язування для основного комплексу гістосумісності класу II (MHC класу II) і Т-клітинного рецептора (TCR).[6]
Зв'язування[ред. | ред. код]
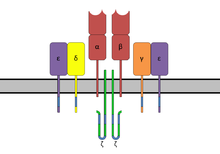
Суперантигени зв’язуються спочатку з MHCII, а потім координуються із варіабельним альфа- або бета-ланцюгом TCR[5][7][8]
MHC класу II[ред. | ред. код]
SAgs віддають перевагу формі HLA-DQ.[8] Зв’язування з α-ланцюгом ставить SAg у відповідне положення для координації з TCR.
Рідше SAg приєднуються до поліморфного β-ланцюга MHCII у взаємодії, опосередкованої координаційним комплексом іонів цинку між трьома залишками SAg і висококонсервативною областю ланцюга HLA-DR β.[5] Використання іона цинку для зв’язування призводить до вищої афінної взаємодії.[4] Деякі стафілококові SAgs здатні до перехресного зв'язування молекул MHC шляхом поєднання з обома α і β ланцюгами.[4][5] Цей механізм стимулює експресію та вивільнення цитокінів антигенпрезентувальними клітинами (АПК), а також індукує вироблення костимулюючих молекул, які дозволяють клітині зв’язуватися з Т-клітинами та активувати їх більш ефективно.[5]
Т-клітинний рецептор[ред. | ред. код]
Ділянка SAg, яка зв'язується з Т-клітиною, взаємодіє з варіабельною ділянкою β-ланцюга TCR (Vβ-ділянка). Конкретний SAg може активувати велику частину популяції Т-клітин, оскільки усі Т-клітини людини містять лише близько 50 типів елементів Vβ, а деякі SAg здатні зв’язуватися з кількома типами Vβ-ділянок. Ця взаємодія дещо різниться у різних групах SAgs.[6] Варіабельність типів Т-клітин у різних людей, пояснює, чому деякі люди сильніше реагують на певні SAgs. SAgs групи I контактують з Vβ в CDR2 і каркасній ділянці молекули.[9][10] SAg групи II взаємодіють з Vβ-ділянкою за допомогою механізмів, які є конформаційно-залежними. Ці взаємодії здебільшого не залежать від специфічних бічних ланцюгів амінокислот Vβ. Було показано, що SAgs групи IV зачіпають усі три петлі CDR певних форм Vβ.[9][10] Взаємодія відбувається в щілині між малим і великим доменами SAg і дозволяє SAg діяти як клин між TCR і MHC. Це витісняє антигенний пептид з TCR і обходить нормальний механізм активації Т-клітин.[5][11]
Біологічна сила SAg (його стимулювальна здатність) визначається його спорідненістю до TCR. SAgs з найвищою спорідненістю до TCR викликають найсильнішу реакцію.[12] SPMEZ-2 є найпотужнішим SAg, відкритим на сьогоднішній день.[12]
Передача сигналів у Т-клітинах[ред. | ред. код]
SAg з’єднує MHC і TCR, індукуючи сигнальний шлях, що призводить до проліферації клітини та вироблення цитокінів. Це відбувається тому, що споріднений антиген активує Т-клітину не через її структуру як таку, а тому, що її спорідненість дозволяє їй зв’язувати TCR протягом досить тривалого періоду часу, а SAg імітує цей тимчасовий зв’язок. Низькі рівні Zap-70 були виявлені в Т-клітинах, активованих SAgs, що вказує на те, що нормальний сигнальний шлях активації Т-клітин порушений.[13]
Існує гіпотеза, що активація тирозинкіназою Fyn,а не Lck, призводить до адаптивної індукції анергії.[14]
Активуються як шлях протеїнкінази С, так і шляхи протеїнкінази тирозинкінази, що призводить до активізації вироблення прозапальних цитокінів.[15]
Цей альтернативний сигнальний шлях незначно порушує шляхи кальцій/кальциневрин і Ras/МАРкіназа [14] але дозволяє сфокусувати запальну відповідь.
Прямі ефекти[ред. | ред. код]
Коли SAg стимулює АПК і Т-клітини, викликається реакція, яка є переважно запальною, зосередженою на дії Т-хелперів Th1 . Деякі з основних продуктів: IL-1, IL-2, IL-6, TNF-α, IFN-γ, макрофагальний запальний білок 1α (MIP-1α), MIP-1β і моноцитний хемоатрактантний білок 1 ( MCP-1).[15]
Таке надмірне нескоординоване вивільнення цитокінів (особливо TNF-α) перевантажує організм і призводить до висипань, гарячки та може призвести до поліорганної недостатності, коми та смерті.[8][10]
За інфікуванням йде делеція або анергія активованих Т-клітин. Це є результатом вироблення IL-4 та IL-10 внаслідок тривалого впливу токсину. IL-4 та IL-10 зменшують вироблення IFN-γ, MHCII та костимулюючих молекул на поверхні АПК. Ці ефекти призводять до появи клітин пам’яті, які не реагують на антигенну стимуляцію.[16][17]
Один з механізмів, за допомогою якого це можливо - опосередковане цитокінами пригнічення Т-клітин. Перехресне зв'язування MHC також активує сигнальний шлях, який пригнічує гемопоез і посилює Fas-опосередкований апоптоз .[18]
IFN-α є ще одним продуктом тривалого впливу SAg. Цей цитокін тісно пов’язаний з індукцією аутоімунітету[19]. Аутоімунне захворювання хвороба Кавасакі, як відомо, викликається інфекцією SAg.[12]
Після активації Т-клітин SAgs відбувається продукція ліганду CD40, який активує перемикання типу антитіл в В-клітинах на IgG, IgM, IgE.[20]
Підсумовуючи, можна сказати, що Т-клітини стимулюються і виробляють надмірну кількість цитокінів, що призводить до опосередкованого цитокінами пригнічення Т-клітин і видалення активованих клітин, коли організм повертається до гомеостазу. Токсичний вплив мікробів і SAg також пошкоджує тканини та системи органів, стан, відомий як синдром токсичного шоку.[20]
Якщо початкове запалення зберігається, клітини-господарі стають анергічними або видаляються, що призводить до серйозного порушення імунної системи.
Незалежні від суперантигенності (непрямі) ефекти[ред. | ред. код]
Крім своєї мітогенної активності, SAgs здатні викликати симптоми, характерні для інфекції.[1]
Одним з таких ефектів є блювання. Цей ефект спостерігається у випадках харчового отруєння, коли бактерії, що продукують SAg, виділяють токсин, який має високу стійкість до високої температури (термостабільність). Існує окрема ділянка молекули, яка активна в індукції шлунково-кишкової токсичності.[1] Ця активність дуже потужна, усього 20-35 мкг SAg здатні викликати блювання.[8]
SAgs здатні стимулювати міграцію нейтрофілів до місця інфекції незалежно від стимуляції Т-клітин. Цей ефект пов’язаний зі здатністю SAgs активувати моноцитарні клітини, стимулюючи вивільнення цитокіну TNF-α, що призводить до посилення експресії молекул адгезії, які затримують лейкоцити в інфікованих ділянках. Це викликає запалення в легенях, кишковій тканині та будь-якому місці, де розмножуються бактерії.[21] Хоча певна частина запалення є природним і корисним процесом, надмірне запалення може призвести до руйнування тканин.
Один з найбільш небезпечних непрямих ефектів суперантигенної інфекції стосується здатності SAg посилювати дію ендотоксинів в організмі. Це досягається шляхом зниження порога ендотоксичності. Шліверт продемонстрував, що при одночасному введенні ефект SAg та ендотоксину збільшується у 50 000 разів.[7] Це може бути пов’язано зі зниженням ефективності імунної системи, спричиненою SAg. Крім синергичного зв’язку між ендотоксином і SAg, ефект «подвійного удару» призводить до ефектів, більш шкідливих, ніж при типовій бактеріальній інфекції. Це також пов'язує SAgs із прогресуванням сепсису у пацієнтів з бактеріальними інфекціями.[20]
Захворювання, пов’язані суперантигенами[ред. | ред. код]
- Цукровий діабет
- Екзема
- Гутатний псоріаз
- Хвороба Кавасакі
- Поліпи носа [22]
- Ревматична гарячка
- Ревматоїдний артрит
- Скарлатина [8]
- Синдром токсичного шоку
- Інфекційний ендокардит [23]
Лікування[ред. | ред. код]
Основні цілі медикаментозного лікування полягають у стабілізації гемодинаміки пацієнта та, якщо він присутній, у знищенні мікроба, який виробляє SAgs. Це досягається за допомогою вазопресорів, регідратації та антибіотиків.[1]
Організм природним чином виробляє антитіла до деяких SAg, і цей ефект можна посилити, стимулюючи вироблення цих антитіл В-клітинами.[24]
Певні імуноглобуліни здатні нейтралізувати специфічні антитіла і запобігати активації Т-клітин. Синтетичні антитіла та пептиди були створені для імітації SAg-зв’язуючих ділянок до MHC класу II, блокуючи цю взаємодію та запобігаючи активації Т-клітин.[1]
Імуносупресанти також використовуються для запобігання активації Т-клітин і вивільнення цитокінів. Кортикостероїди використовуються для зменшення запальних ефектів.[20]
Еволюція[ред. | ред. код]
Продукція SAg ефективно порушує імунну відповідь, дозволяючи мікробам, які їх секретують, безперешкодно розповсюджуватись. Один з механізмів, за допомогою якого це робиться, полягає в індукції анергії Т-клітин до антигенів і SAg.[13][16] Луссов і Макдональд продемонстрували це, систематично вводячи тваринам стрептококовий антиген. Вони виявили, що вплив інших антигенів після інфікування SAg не викликав імунної відповіді.[16] В іншому експерименті Уотсон і Лі виявили, що Т-клітини пам’яті, створені нормальною стимуляцією антигеном, були анергічні до стимуляції SAg, а Т-клітини пам’яті, що з'явилися після інфекції SAg, були анергічними до будь-якої антигенної стимуляції. Механізм, за допомогою якого це відобувалося, не визначений.[13] Гени, які регулюють експресію SAg, також регулюють механізми імунного ухилення, такі як експресія М-білка і бактеріальної капсули, підтверджуючи гіпотезу про те, що продукція SAg розвивалася в основному як механізм ухилення від імунітету.[25]
Коли структуру окремих доменів SAg порівняли з іншими білками стрептокока, що зв’язують імуноглобулін (такими як токсини, що виробляються E. coli ), було виявлено, що окремі домени SAg нагадують членів цих сімейств. Ця гомологія свідчить про те, що SAgs еволюціонували шляхом рекомбінації двох менших мотивів β-ланцюга.[26]
Ендогенні SAgs[ред. | ред. код]
Незначні лімфоцитостимулюючі екзотоксини спочатку були виявлені в клітинах строми тимуса мишей. Ці токсини кодуються генами SAg, які були включені в геном миші з вірусу пухлини молочної залози миші (MMTV). Наявність цих генів у геномі миші дозволяє миші експресувати антиген у тимусі як засіб негативного відбору лімфоцитів із варіабельною бета-ділянкою, яка чутлива до стимуляції вірусним SAg. В результаті ці миші мають імунітет до зараження вірусом.[1]
Подібний ендогенний SAg-залежний відбір ще не був ідентифікований в геномі людини, але самі ендогенні SAg були виявлені, і, як підозрюють, вони відіграють невід'ємну роль у вірусній інфекції. Наприклад, відомо, що зараження вірусом Епштейна-Барр викликає вироблення SAg в інфікованих клітинах, але ген токсину не знайдено в геномі вірусу. Вірус маніпулює інфікованою клітиною, щоб ті експресували власні гени SAg, і це допомагає вірусу уникати імунної системи хазяїна. Подібні результати були знайдені для сказу, цитомегаловірусу та ВІЛ.[1]
Посилання[ред. | ред. код]
- ↑ а б в г д е ж Llewelyn M, Cohen J (March 2002). Superantigens: microbial agents that corrupt immunity. Lancet Infect Dis. 2 (3): 156—62. doi:10.1016/S1473-3099(02)00222-0. PMID 11944185.
- ↑ Li H., Llera A., Malchiodi E.L., Mariuzza R.A. The structural basis of T cell activation by superantigens. Annu. Rev. Immunol. 1999;17:435–466. doi: 10.1146/annurev.immunol.17.1.435.
- ↑ Sriskandan S, Faulkner L, Hopkins P (2007). Streptococcus pyogenes: Insight into the function of the streptococcal superantigens. Int. J. Biochem. Cell Biol. 39 (1): 12—9. doi:10.1016/j.biocel.2006.08.009. PMID 17029999.
- ↑ а б в г Petersson K, Forsberg G, Walse B (April 2004). Interplay between superantigens and immunoreceptors. Scand. J. Immunol. 59 (4): 345—55. doi:10.1111/j.0300-9475.2004.01404.x. PMID 15049778.
- ↑ а б в г д е Mehindate K, Thibodeau J, Dohlsten M, Kalland T, Sékaly RP, Mourad W (November 1995). Cross-linking of major histocompatibility complex class II molecules by staphylococcal enterotoxin A superantigen is a requirement for inflammatory cytokine gene expression. J. Exp. Med. 182 (5): 1573—7. doi:10.1084/jem.182.5.1573. PMC 2192187. PMID 7595227.
- ↑ а б Papageorgiou AC, Tranter HS, Acharya KR (March 1998). Crystal structure of microbial superantigen staphylococcal enterotoxin B at 1.5 A resolution: implications for superantigen recognition by MHC class II molecules and T-cell receptors. J. Mol. Biol. 277 (1): 61—79. doi:10.1006/jmbi.1997.1577. PMID 9514739.
- ↑ а б Schlievert PM (April 1982). Enhancement of host susceptibility to lethal endotoxin shock by staphylococcal pyrogenic exotoxin type C. Infect. Immun. 36 (1): 123—8. doi:10.1128/IAI.36.1.123-128.1982. PMC 351193. PMID 7042568.
- ↑ а б в г д Alouf JE, Müller-Alouf H (February 2003). Staphylococcal and streptococcal superantigens: molecular, biological and clinical aspects. Int. J. Med. Microbiol. 292 (7–8): 429—40. doi:10.1078/1438-4221-00232. PMID 12635926.
- ↑ а б Brouillard JN, Günther S, Varma AK та ін. (April 2007). Crystal structure of the streptococcal superantigen SpeI and functional role of a novel loop domain in T cell activation by group V superantigens. J. Mol. Biol. 367 (4): 925—34. doi:10.1016/j.jmb.2007.01.024. PMID 17303163.
{{cite journal}}: Явне використання «та ін.» у:|author=(довідка) - ↑ а б в Buonpane RA, Moza B, Sundberg EJ, Kranz DM (October 2005). Characterization of T cell receptors engineered for high affinity against toxic shock syndrome toxin-1. J. Mol. Biol. 353 (2): 308—21. doi:10.1016/j.jmb.2005.08.041. PMID 16171815.
- ↑ Li H, Llera A, Tsuchiya D та ін. (December 1998). Three-dimensional structure of the complex between a T cell receptor beta chain and the superantigen staphylococcal enterotoxin B. Immunity. 9 (6): 807—16. doi:10.1016/S1074-7613(00)80646-9. PMID 9881971.
{{cite journal}}: Явне використання «та ін.» у:|author=(довідка) - ↑ а б в Arcus VL, Proft T, Sigrell JA, Baker HM, Fraser JD, Baker EN (May 2000). Conservation and variation in superantigen structure and activity highlighted by the three-dimensional structures of two new superantigens from Streptococcus pyogenes. J. Mol. Biol. 299 (1): 157—68. doi:10.1006/jmbi.2000.3725. PMID 10860729.
- ↑ а б в Watson AR, Lee WT (August 2006). Defective T cell Receptor-mediated Signal Transduction in Memory CD4 T Lymphocytes Exposed to Superantigen or anti-T cell Receptor Antibodies. Cell. Immunol. 242 (2): 80—90. doi:10.1016/j.cellimm.2006.09.008. PMC 1829409. PMID 17083922.
- ↑ а б Choi S, Schwartz RH (June 2007). Molecular mechanisms for adaptive tolerance and other T cell anergy models. Semin. Immunol. 19 (3): 140—52. doi:10.1016/j.smim.2007.02.005. PMC 2045643. PMID 17400472.
- ↑ а б Stiles BG, Krakauer (2005). Staphylococcal Enterotoxins: a Purging Experience in Review, Part I. Clinical Microbiology Newsletter. 27 (23): 23. doi:10.1016/j.clinmicnews.2005.11.001.
- ↑ а б в Lussow AR, MacDonald HR (February 1994). Differential effects of superantigen-induced "anergy" on priming and effector stages of a T cell-dependent antibody response. Eur. J. Immunol. 24 (2): 445—9. doi:10.1002/eji.1830240227. PMID 8299694.
- ↑ Miller C, Ragheb JA, Schwartz RH (July 1999). Anergy and Cytokine-Mediated Suppression as Distinct Superantigen-Induced Tolerance Mechanisms in Vivo. J. Exp. Med. 190 (1): 53—64. doi:10.1084/jem.190.1.53. PMC 2195559. PMID 10429670.
- ↑ Yamaguchi M, Nadler S, Lee JW, Deeg HJ (September 1999). Induction of negative regulators of haematopoiesis in human bone marrow cells by HLA-DR cross-linking. Transpl. Immunol. 7 (3): 159—68. doi:10.1016/S0966-3274(99)80035-5. PMID 10608299.
- ↑ Stauffer Y, Marguerat S, Meylan F та ін. (October 2001). Interferon-alpha-induced endogenous superantigen. a model linking environment and autoimmunity. Immunity. 15 (4): 591—601. doi:10.1016/S1074-7613(01)00212-6. PMID 11672541.
{{cite journal}}: Явне використання «та ін.» у:|author=(довідка) - ↑ а б в г Jabara HH, Geha RS (October 1996). The superantigen toxic shock syndrome toxin-1 induces CD40 ligand expression and modulates IgE isotype switching. Int. Immunol. 8 (10): 1503—10. doi:10.1093/intimm/8.10.1503. PMID 8921429.
- ↑ Diener K, Tessier P, Fraser J, Köntgen F, McColl SR (June 1998). Induction of acute inflammation in vivo by staphylococcal superantigens I: Leukocyte recruitment occurs independently of T lymphocytes and major histocompatibility complex Class II molecules. Lab. Invest. 78 (6): 647—56. PMID 9645755.
- ↑ Van Cauwenberge P, Gevaert P, Van Hoecke H, Van Zele T, Bachert C (2005). New insights into the pathology of nasal polyposis: the role of superantigens and IgE. Verh K Acad Geneeskd Belg. 67 (5–28): 5—28, discussion 29–32. PMID 15828304.
- ↑ Salgado-Pabón W, et al. (2013) Superantigens are critical for Staphylococcus aureus infective endocarditis, sepsis, and acute kidney injury. MBio 4:e00494-00413.
- ↑ Erlandsson E, Andersson K, Cavallin A, Nilsson A та ін. (2003). Identification of the Antigenic Epitopes in Staphylococcal Enterotoxins A and E and Design of a Superantigen for Human Cancer Therapy. J. Mol. Biol. 333 (5): 893—905. doi:10.1016/j.jmb.2003.09.009. PMID 14583188.
{{cite journal}}: Явне використання «та ін.» у:|author=(довідка) - ↑ Cleary PP, McLandsborough L, Ikeda L, Cue D, Krawczak J, Lam H (April 1998). High-frequency intracellular infection and erythrogenic toxin A expression undergo phase variation in M1 group A streptococci. Mol. Microbiol. 28 (1): 157—67. doi:10.1046/j.1365-2958.1998.00786.x. PMID 9593304.
- ↑ Bachert C, Gevaert P, van Cauwenberge P (June 2002). Staphylococcus aureus enterotoxins: a key in airway disease?. Allergy. 57 (6): 480—7. doi:10.1034/j.1398-9995.2002.02156.x. PMID 12028112.