Гідрати: відмінності між версіями
| [неперевірена версія] | [неперевірена версія] |
Олег.Н (обговорення | внесок) доповнення |
Немає опису редагування |
||
| Рядок 2: | Рядок 2: | ||
'''Гідра́ти''' — комплекси, які містить зв'язані [[молекула|молекули]] [[вода|води]], що можуть входити до її структури. |
'''Гідра́ти''' — комплекси, які містить зв'язані [[молекула|молекули]] [[вода|води]], що можуть входити до її структури. |
||
Координування молекул води відбувається за рахунок донорно-акцепторної взаємодії: атом оксигену у молекулі води має неподілені пари електронів, на ньому зосереджується частково негативний заряд, тому |
Координування молекул води відбувається за рахунок донорно-акцепторної взаємодії: атом оксигену у молекулі води має неподілені пари електронів, на ньому зосереджується частково негативний заряд, тому він може притягатися до позитивно заряджених частинок-катіонів (зазвичай, ними є метали), які утворюються у розчині внаслідок [[електролітична дисоціація|дисоціації]]. |
||
[[Файл:Copper sulfate.jpg|міні|праворуч|200пкс|Кристалогідрат CuSO<sub>4</sub>·5H<sub>2</sub>O]] |
[[Файл:Copper sulfate.jpg|міні|праворуч|200пкс|Кристалогідрат CuSO<sub>4</sub>·5H<sub>2</sub>O]] |
||
Як правило, гідрати є нестійкими сполуками, що легко розкладаються при випарюванні розчину. Однак, існують і такі гідрати, що утримують молекули води у своїй кристалічній структурі і виділяються з [[розчин]]ів у формі [[кристалогідрат]]ів. Кристалогідрати характерні також для природних [[горючий газ|горючих газів]]. |
Як правило, гідрати є нестійкими сполуками, що легко розкладаються при випарюванні розчину. Однак, існують і такі гідрати, що утримують молекули води у своїй кристалічній структурі і виділяються з [[розчин]]ів у формі [[кристалогідрат]]ів. Кристалогідрати характерні також для природних [[горючий газ|горючих газів]]. |
||
Версія за 17:07, 27 березня 2015
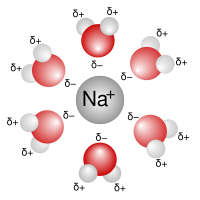
Гідра́ти — комплекси, які містить зв'язані молекули води, що можуть входити до її структури.
Координування молекул води відбувається за рахунок донорно-акцепторної взаємодії: атом оксигену у молекулі води має неподілені пари електронів, на ньому зосереджується частково негативний заряд, тому він може притягатися до позитивно заряджених частинок-катіонів (зазвичай, ними є метали), які утворюються у розчині внаслідок дисоціації.

Як правило, гідрати є нестійкими сполуками, що легко розкладаються при випарюванні розчину. Однак, існують і такі гідрати, що утримують молекули води у своїй кристалічній структурі і виділяються з розчинів у формі кристалогідратів. Кристалогідрати характерні також для природних горючих газів.
У водних розчинах катіони багатозарядних металів завжди утворюють аквокомплекси, які, на відміну від гідратів, мають чітко визначену кількість координованих молекул води (відповідно до координаційного числа металу-комплексоутворювача): [Be(H2O)4]2+, [Co(H2O)6]2+. Аквокомплекси відрізняються від кристалогідратів міцнішим зв'язком між молекулами H2O та металом. Окрім того, молекули води можуть бути одночасно координованими у комплексі та кристалі: [Fe(H2O)6]SO4·2H2O.
Див. також
| Вікісховище має мультимедійні дані за темою: Гідрати |
Література
- Мала гірнича енциклопедія : у 3 т. / за ред. В. С. Білецького. — Д. : Донбас, 2004. — Т. 1 : А — К. — 640 с. — ISBN 966-7804-14-3.
- Глинка Н. Л. Общая химия / А. И. Ермакова. — 30. — М. : Интеграл-Пресс, 2003. — 728 с. — ISBN 5-89602-017-1.
- Химический энциклопедический словарь / И. Л. Кнунянц. — М. : Сов. энциклопедия, 1983. — 792 с.

|
Це незавершена стаття з хімії. Ви можете допомогти проєкту, виправивши або дописавши її. |