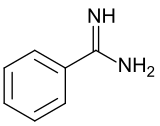
Бензамідин
| Бензамідин | |
|---|---|
 | |
 | |
| Назва за IUPAC | Бензенкарбоксимідамід |
| Ідентифікатори | |
| Номер CAS | 618-39-3 |
| PubChem | 2332 |
| Номер EINECS | 210-546-3 |
| KEGG | C01784 |
| ChEBI | 41033 |
| SMILES | [NH]=C(N)c1ccccc1 |
| InChI | 1/C7H8N2/c8-7(9)6-4-2-1-3-5-6/h1-5H,(H3,8,9) |
| Номер Бельштейна | 606020 |
| Номер Гмеліна | 326011 |
| Властивості | |
| Молекулярна формула | C7H8N2 |
| Молярна маса | 120,15 г/моль |
| Зовнішній вигляд | біла тверда речовина |
| Густина | 1.22 g/cm3 |
| Тпл | 78-80 |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Бензаміди́н (англ. benzamidine) — це органічна сполука з формулою 6H5C(NH)NH2. Це найпростіший ариламідин. Сполука є білою твердою речовиною, яка слабо розчиняється у воді. Зазвичай з ним поводяться як з гідрохлоридною сіллю, білою, водорозчинною сіллю[1].
За своєю молекулярною структурою, бензамідин має один короткий зв'язок C=NH і один довший зв'язок C-NH2, 129 і 135 пікометрів, відповідно[2].
Бензамідин є зворотним конкурентним інгібітором трипсину, трипсиноподібних ферментів та серинових протеаз[3].
Його часто використовують як ліганд у білковій кристалографії, щоб запобігти деградації протеазами білка, що цікавить; трикутна діамінова група внизу надає йому дуже очевидну форму «stick-man», яка показується на картах різниці щільності. Бензамідинова група також міститься в деяких фармацевтичних препаратах, таких як дабігатран.
Конденсація з α-галокетонами утворює імідазол[1].
- ↑ а б Bryan Li, Charles K-F Chiu, Richard F. Hank, Jerry Murry, Joshua Roth, Harry Tobiassen (2005). Preparation of 2,4-Disubstituted Imidazoles: 4-(4-Methoxyphenyl)-2-Phenyl-1H-Imidazole. Organic Syntheses. 81: 105. doi:10.15227/orgsyn.081.0105.
- ↑ Barker, J.; Phillips, P. R.; Wallbridge, M. G. H.; Powell, H. R. (1996). Benzamidine. Acta Crystallographica Section C Crystal Structure Communications. 52 (10): 2617—2619. doi:10.1107/S0108270196006282.
- ↑ Tanizawa, Kazutaka; Ishii, Shin-ichi; Hamaguchi, Kazo; Kanaoka, Yuichi (1 травня 1971). Proteolytic EnzymesVI. Aromatic Amidines as Competitive Inhibitors of Trypsin. The Journal of Biochemistry. 69 (5): 893—899. doi:10.1093/oxfordjournals.jbchem.a129540. ISSN 0021-924X. PMID 5577153.
| Це незавершена стаття про органічну сполуку. Ви можете допомогти проєкту, виправивши або дописавши її. |