Каталізатор Вілкінсона
| Каталізатор Вілкінсона | |
|---|---|
 Каталізатор Вілкінсона
| |
 Каталізатор Вілкінсона
| |
 Каталізатор Вілкінсона
| |
 Каталізатор Вілкінсона
| |
| Назва за IUPAC | (SP-4)хлоридотріс(трифенілфосфан)родію |
| Інші назви | Родію(I) тріс-(трифенілфосфін) хлорид, каталізатор Вілкінсона |
| Ідентифікатори | |
| Номер CAS | 14694-95-2 |
| Номер EINECS | 238-744-5 |
| RTECS | none |
| SMILES | C1=CC=C(C=C1)P(C2=CC=CC=C2)C3=CC=CC=C3.C1=CC=C(C=C1)P(C2=CC=CC=C2)C3=CC=CC=C3.C1=CC=C(C=C1)P(C2=CC=CC=C2)C3=CC=CC=C3.[Cl-].[Rh+][1] |
| InChI | InChI=1S/3C18H15P.ClH.Rh/c3*1-4-10-16(11-5-1)19(17-12-6-2-7-13-17)18-14-8-3-9-15-18;;/h3*1-15H;1H;/p-1 |
| Властивості | |
| Молекулярна формула | C54H45ClP3Rh |
| Молярна маса | 925,22 г/моль |
| Зовнішній вигляд | цегляний порошок |
| Тпл | 245-250 °C |
| Розчинність (вода) | нерозчинний |
| Розчинність (бензен) | розчинний |
| Структура | |
| Координаційна геометрія |
плаский квадрат |
| Небезпеки | |
| R-фрази | жодної |
| S-фрази | S22 S24/25 |
| Головні небезпеки | жодної |
| Пов'язані речовини | |
| Пов'язані речовини | трифенілфосфін Pd(PPh3)4 IrCl(CO)[P(C6H5)3]2 |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
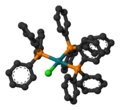
Каталіза́тор Ві́лкінсона — тривіальна назва хімічної речовини з формулою RhCl(PPh3)3 (Ph = феніл). Названий на честь лауреата Нобелівської премії з хімії Джефрі Вілкінсона, який ввів цю сполуку до широкої синтетичної практики.
Молекула речовини являє собою плаский квадратний 16-електронний комплекс. Речовину виділяють у вигляді червоно-коричневого порошку після реакції хлориду родію(ІІІ) із надлишком трифенілфосфіну у киплячому етанолі[2].
Частина трифенілфосфіну виступає відновником, перетворюючись на трифенілфосфіноксид. Реакція, що відбувається, записується рівнянням
Каталізатор Вілкінсона використовується для гідрування алкенів[3][4]. На початковій стадії механізм цієї реакції включає в себе дисоціацію одного або двох лігандів трифенілфосфіну з утворенням 14-ти або 12-ти електронних комплексів відповідно, після чого відбувається окиснювальне приєднання H2 до металу. Наступне утворення π-комплексу з алкеном, внутрішньомолекулярне перенесення гідриду (вставка олефіну) та відновне елімінування призводять до утворення алканового продукту, тобто:
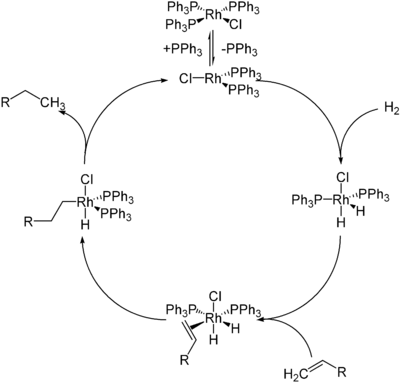
Також каталізатор Вілкінсона використовують при каталітичному гідроборуванні алкенів з допомогою катехолборану та пінаколборану]][5] та селективному 1,4-відновленні α,β-ненасичених карбонільних сполук при взаємодії з триетилсиланом[6].
- ↑ chlorotris(triphenylphosphine)rhodium
- ↑ Osborn, J. A.; Jardine, F. H.; Young, J. F.; Wilkinson, G. (1966). The Preparation and Properties of Tris(triphenylphosphine)halogenorhodium(I) and Some Reactions Thereof Including Catalytic Homogeneous Hydrogenation of Olefins and Acetylenes and Their Derivatives. Journal of the Chemical Society A: 1711—1732. doi:10.1039/J19660001711.
- ↑ A. J. Birch, D. H. Williamson (1976). Organic Reactions. 24: 1ff.
{{cite journal}}: Пропущений або порожній|title=(довідка) - ↑ B.R. James, Homogeneous Hydrogenation. John Wiley & Sons, New York, 1973.
- ↑ D. A. Evans, G. C. Fu and A. H. Hoveyda (1988). Rhodium(I)-catalyzed hydroboration of olefins. The documentation of regio- and stereochemical control in cyclic and acyclic systems. J. Am. Chem. Soc. 110 (20): 6917—6918. doi:10.1021/ja00228a068.
- ↑ I. Ojima, T. Kogure (1972). Selective reduction of α,β-unsaturated terpene carbonyl compounds using hydrosilane-rhodium(I) complex combinations. Tetrahedron Lett. 13 (49): 5035—5038. doi:10.1016/S0040-4039(01)85162-5.
