Нікотинамідаденіндинуклеотид: відмінності між версіями
| [перевірена версія] | [неперевірена версія] |
Немає опису редагування |
SimondR (обговорення | внесок) Немає опису редагування |
||
| Рядок 25: | Рядок 25: | ||
}} |
}} |
||
}} |
}} |
||
'''Нікотинамідаденіндинуклеоти́д''' |
'''Нікотинамідаденіндинуклеоти́д''' або '''НАД''' ({{lang-en|Nicotinamide adenine dinucleotide}}, '''NAD''') — складна органічна сполука, [[кофермент]], наявний у всіх живих [[клітина]]х. НАД є дінуклеотідом і складається з двох [[нуклеотид]]ів, з'єднаних своїми [[фосфат]]ними групами. Нікотинамідаденіндинуклеотид існує в двох формах: [[Окиснення|окисненої]] (NAD<sup>+</sup>, NAD<sub>''ox''</sub>) і [[Відновлення|відновленої]] (NADH, NAD<sub>''red''</sub>). |
||
| ⚫ | Є небілковою частиною [[фермент]]ів дегідрогеназ, які беруть участь у процесах окиснення органічних сполук у клітині. Молекула НАД складається з двох залишків п'ятивуглецевого цукру [[рибоза|рибози]], які з'єднані двома фосфатними групами. Один цукор зв'язаний з [[аденін]]ом, а другий — з іншою азотистою основою — нікотинамідом. Фермент дегідрогеназа переносить атом водню з двома електронами з субстрату, що окиснюється, на кофермент НАД. Активною групою коферменту є амід нікотинової кислоти. Він приймає водень у вигляді гідрид-йону на піридинове кільце, інший атом водню у вигляді протону переходить у розчин. Цей процес є стереоспецифічним, одна група ферментів (алкогольдегідрогеназа, лактатдегідрогеназа) переносять водень на одну сторону піридинового кільця, інші (гліцеральдегідфосфатдегідрогеназа) — на іншу сторону. Таке дегідрування можна коротко описати рівнянням: |
||
Відкритий у [[1904]] році англійськими біохіміками [[Артур Гарден|Артуром Гарденом]] та [[Вільям Яндін|Вільямом Яндіном]] у екстракті [[дріжджі]]в. Будова коферменту встановлена у 1936 [[Отто Генріх Варбург|Отто Варбургом]] та [[Ганс Карл Август Симон фон Ейлер-Хельпін|Гансом Ейлером-Хельпіном]]. |
|||
| ⚫ | |||
| ⚫ | Є небілковою частиною [[фермент]]ів дегідрогеназ, які беруть участь у процесах |
||
| ⚫ | |||
| ⚫ | |||
Хоча NAD<sup>+</sup> записується з плюсом через [[Ступінь окиснення|формальний позитивний заряд]] [[атом]]а [[азот]]у, за фізіологічних значеннях [[Водневий показник|pH]] велика частина NAD<sup>+</sup> насправді є [[аніон]]ом з негативним зарядом -1, а NADH — аніоном з зарядом -2. |
|||
| ⚫ | |||
Окиснені та відновлені форми коферментів мають різні максимуми в [[спектр поглинання|спектрах поглинання]] світла. На цій властивості засновані оптичні методи визначення активності ферментів. |
|||
== Фармакологічне та медичне застосування == |
|||
Ферменти, залучені у синтезу, і використання NAD<sup>+</sup>, мають важливе значення для [[Фармакологія|фармакології]] та досліджень, спрямованих на пошук нових способів лікування хвороб. При розробленні нових препаратів NAD<sup>+</sup> розглядається з трьох позицій: як безпосередня мішень для ліків, для розробки інгібіторів і активаторів ферментів, що завдяки своїй структурі змінюють активність NAD-залежних ферментів, і для вивчення методів придушення [[біосинтез]]у NAD<sup>+</sup><ref>{{cite pmid|17465726}}</ref>. |
|||
Наразі сам по собі кофермент NAD<sup>+</sup> не використовується для лікування жодних захворювань. Однак вивчається його потенційна роль у терапії [[Нейродегенеративні захворювання|нейродегенеративних захворювань]], таких як [[хвороба Альцгеймера]] і [[хвороба Паркінсона]]. Є різні дані про дію NAD<sup>+</sup> у нейродегенеративних хворобах. Деякі дослідження на мишах дають обнадійливі результати<ref>{{cite pmid|16988050}}</ref>, проте клінічні випробування на людях з використанням [[плацебо]] не дали жодного ефекту<ref>{{cite pmid|9805207}}</ref>. |
|||
NAD<sup>+</sup> також є безпосередньою мішенню препарату [[ізоніазид]]у, що застосовується для лікування [[туберкульоз]]у — інфекції, спричиненої бактерією [[Mycobacterium tuberculosis|''Mycobacterium tuberculosis'']]. Ізоніазид є [[Проліки|проліками]] і при попаданні в клітину бактерії він активується пероксидазою, яка окиснює цю речовину до [[Вільні радикали|вільно-радикальної]] форми. Цей радикал далі реагує з NADH з утворенням [[аддукт]]ів, які є дуже сильними інгібіторами ферментів {{нп5|Редуктаза білка-переносника еноіл-ацілу|редуктази білка-переносника еноіл-ацілу|en|Enoyl-acyl carrier protein reductase}}<ref>{{cite pmid|14623976}}</ref> й [[DHFR|дигідрофолатредуктази]]. В одному експерименті у мишей, яким давали NAD протягом тижня, поліпшувалося взаємодія клітинного ядра і мітохондрій<ref>{{cite pmid|24360282}}</ref>. |
|||
Через величезну кількість [[Оксидоредуктази|оксидоредуктаз]], що використовують NAD<sup>+</sup> і NADH в якості субстратів і зв'язуються з ними за допомогою одного висококонсервативного структурного мотиву, ідея розроблення інгібітору, що блокує центр зв'язування NAD<sup>+</sup>, і специфічного лише для певного ферменту, здається сумнівною<ref name=Pankiewicz>{{cite pmid|15083807}}</ref>. Однак це може бути здійсненним: так, інгібітори, засновані на {{нп5|Мікофенолінова кислота|мікофеноліновій кислоті|en|Mycophenolic acid}} й {{нп5|Тіазофурин|тіазофурині|en|Tiazofurin}}, пригнічують {{нп5|Інозинмонофосфатдегідрогеназа|інозинмонофосфатдегідрогенази|en|IMP dehydrogenase}} у місті зв'язування з NAD<sup>+</sup>. Через важливу роль цього ферменту в [[Пуриновий метаболізм|метаболізмі пуринів]] ці сполуки можуть бути корисними [[Протипухлинні препарати|протипухлинними]] і [[Противірусні препарати|противірусними препаратами]] або [[Імуносупресори|імуносупресорами]]<ref name=Pankiewicz/><ref>{{cite pmid|10390603}}</ref>. Інші препарати не є інгібіторами, а, навпаки, активаторами ферментів, залучених в метаболізм NAD<sup>+</sup>. Інші препарати не є інгібіторами, а, навпаки, активаторами ферментів, залучених у метаболізм NAD<sup>+</sup>. Зокрема, цікавою мішенню для таких препаратів можуть бути сиртуїни, бо активація цих NAD-залежних деацетілаз збільшують тривалість життя<ref name=Kim>{{cite pmid|19017485}}</ref>. Такі сполуки, як [[резвератрол]], збільшують активність цих ферментів, які можуть мати велике значення завдяки їх здатності до переносу старіння на пізніший строк як у [[Хребетні|хребетних]]<ref>{{cite pmid|16461283}}</ref>, так і [[Модельний організм|модельних організмів]] з числа [[Безхребетні|безхребетних]]<ref>{{cite pmid|12939617}}</ref><ref>{{cite pmid|15254550}}</ref>. |
|||
Через відмінності шляхів біосинтезу NAD<sup>+</sup> у різних організмів, зокрема, між бактеріями і людиною, біосинтез NAD<sup>+</sup> може стати новою сферою розвитку нових [[антибіотик]]ів<ref>{{cite pmid|12504674}}</ref><ref>{{cite pmid|11153263}}</ref>. Наприклад, фермент {{нп5|нікотинамідаза||en|Nicotinamidase}}, перетворює нікотинамід у нікотинову кислоту, слугує мішенню розроблюваних ліків, так як цей фермент відсутній у людини, але є у бактерій і дріжджів<ref name=Rongvaux/>. |
|||
== Історія == |
|||
[[Файл:ArthurHarden.jpg|thumb|upright=0.6|Артур Гарден, один з першовідкривачів NAD<sup>+</sup>]] |
|||
Кофермент NAD+ був відкритий англійськими [[біохімік]]ами [[Артур Гарден|Артуром Гарденом]] та {{нп5|Янґ Вільям|Вільямом Янґом|en|William John Young}} 1904 року<ref>{{ref-en}} {{Cite journal|author= A. Harden, W. J. Young |title= The alcoholic ferment of yeast-juice Part II.--The coferment of yeast-juice |work= Proceedings of the Royal Society of London|series= Series B, Containing Papers of a Biological Character|volume= 78|date= 24 жовтня 1906|pages= 369–375|issue= 526|jstor=80144 }}</ref>. Вони помітили, що додавання прокип'яченого і профільтрованого екстракту [[дріжджі]]в до непрокип'ячених екстрактів значно посилювало [[спиртове бродіння]] в останніх. Невідомий фактор, відповідальний за це явище, вони назвали ''коферментом''. У ході тривалого і складного виділення з екстрактів дріжджів цей теплостійкий фактор був ідентифікований як нуклеотид-сахарофосфат [[Ганс Карл Август Симон фон Ейлер-Хельпін|Гансом Ейлером-Хельпіном]]<ref>{{ref-en}} {{Cite web|url= http://nobelprize.org/nobel_prizes/chemistry/laureates/1929/euler-chelpin-lecture.pdf|title= Fermentation of sugars and fermentative enzymes|work= Nobel Lecture, 23 May 1930|accessdate=2007-09-30|publisher=Nobel Foundation|format=PDF}}</ref>. 1936 року німецький вчений [[Отто Генріх Варбург]] встановив функцію цього коферменту з перенесення гідридного йона і визначив, що в окисно-відновних реакціях бере участь нікотинамідний залишок<ref>{{ref-de}} {{Cite journal|author=Warburg O, Christian W.|title=Pyridin, der wasserstoffübertragende bestandteil von gärungsfermenten (pyridin-nucleotide)|trans_title=Pyridin, the hydrogen-transferring component of the fermentation enzymes (pyridine nucleotide)|journal=Biochemische Zeitschrift|volume=287|year=1936|page=291|doi=10.1002/hlca.193601901199 }}</ref>. |
|||
== Література == |
== Література == |
||
* Шлегель Г. Общая микробиология. Перевод с нем. Л. |
* Шлегель Г. Общая микробиология. Перевод с нем. Л. В. Алексеевой. М.: Мир, 1987. С. 567. |
||
== Примітки == |
|||
{{примітки}} |
|||
== Посилання == |
== Посилання == |
||
* [http://referatu.net.ua/referats/66/11890/?page=7 Регуляція активності ферментів] |
* [http://referatu.net.ua/referats/66/11890/?page=7 Регуляція активності ферментів] |
||
Версія за 15:08, 6 грудня 2017
| Нікотинамідаденіндинуклеотид | |
|---|---|
| |
| Інші назви | Дифосфопіридиннуклеотид (DPN+), Коензим I |
| Ідентифікатори | |
| Абревіатури | НАД, NAD |
| Номер CAS | 53-84-9 |
| Номер EINECS | 200-184-4 |
| DrugBank | 14128 |
| Назва MeSH | D03.633.100.759.646.138.694, D08.211.589, D13.695.667.138.694 і D13.695.827.068.694 |
| ChEBI | 13389 |
| RTECS | UU3450000 |
| SMILES | C1=CC(=C[N+](=C1)C2C(C(C(O2)COP(=O)([O-])OP(=O)(O)OCC3C(C(C(O3)N4C=NC5=C4N=CN=C5N)O)O)O)O)C(=O)N |
| InChI | |
| Властивості | |
| Молекулярна формула | C21H27N7O14P2 |
| Молярна маса | 663,43 г/моль |
| Тпл | 160 °C |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
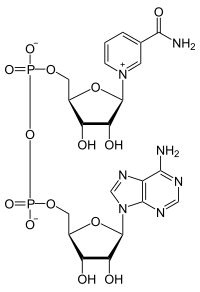
Нікотинамідаденіндинуклеоти́д або НАД (англ. Nicotinamide adenine dinucleotide, NAD) — складна органічна сполука, кофермент, наявний у всіх живих клітинах. НАД є дінуклеотідом і складається з двох нуклеотидів, з'єднаних своїми фосфатними групами. Нікотинамідаденіндинуклеотид існує в двох формах: окисненої (NAD+, NADox) і відновленої (NADH, NADred).
Є небілковою частиною ферментів дегідрогеназ, які беруть участь у процесах окиснення органічних сполук у клітині. Молекула НАД складається з двох залишків п'ятивуглецевого цукру рибози, які з'єднані двома фосфатними групами. Один цукор зв'язаний з аденіном, а другий — з іншою азотистою основою — нікотинамідом. Фермент дегідрогеназа переносить атом водню з двома електронами з субстрату, що окиснюється, на кофермент НАД. Активною групою коферменту є амід нікотинової кислоти. Він приймає водень у вигляді гідрид-йону на піридинове кільце, інший атом водню у вигляді протону переходить у розчин. Цей процес є стереоспецифічним, одна група ферментів (алкогольдегідрогеназа, лактатдегідрогеназа) переносять водень на одну сторону піридинового кільця, інші (гліцеральдегідфосфатдегідрогеназа) — на іншу сторону. Таке дегідрування можна коротко описати рівнянням:
- CH3-CH2-OH + NAD+ → CH3-CH-O + NADH + H+
Кофермент вільно дисоціює, тобто можуть відділятися від одного фермента й з'єднуватись з іншим, переносячи Гідроген та електрони від молекули донора на молекулу акцептор. NADH переносить Гідроген на попередників кінцевих продуктів бродіння або передає у дихальний ланцюг.
Хоча NAD+ записується з плюсом через формальний позитивний заряд атома азоту, за фізіологічних значеннях pH велика частина NAD+ насправді є аніоном з негативним зарядом -1, а NADH — аніоном з зарядом -2.
Окиснені та відновлені форми коферментів мають різні максимуми в спектрах поглинання світла. На цій властивості засновані оптичні методи визначення активності ферментів.
Фармакологічне та медичне застосування
Ферменти, залучені у синтезу, і використання NAD+, мають важливе значення для фармакології та досліджень, спрямованих на пошук нових способів лікування хвороб. При розробленні нових препаратів NAD+ розглядається з трьох позицій: як безпосередня мішень для ліків, для розробки інгібіторів і активаторів ферментів, що завдяки своїй структурі змінюють активність NAD-залежних ферментів, і для вивчення методів придушення біосинтезу NAD+[1].
Наразі сам по собі кофермент NAD+ не використовується для лікування жодних захворювань. Однак вивчається його потенційна роль у терапії нейродегенеративних захворювань, таких як хвороба Альцгеймера і хвороба Паркінсона. Є різні дані про дію NAD+ у нейродегенеративних хворобах. Деякі дослідження на мишах дають обнадійливі результати[2], проте клінічні випробування на людях з використанням плацебо не дали жодного ефекту[3].
NAD+ також є безпосередньою мішенню препарату ізоніазиду, що застосовується для лікування туберкульозу — інфекції, спричиненої бактерією Mycobacterium tuberculosis. Ізоніазид є проліками і при попаданні в клітину бактерії він активується пероксидазою, яка окиснює цю речовину до вільно-радикальної форми. Цей радикал далі реагує з NADH з утворенням аддуктів, які є дуже сильними інгібіторами ферментів редуктази білка-переносника еноіл-ацілу[en][4] й дигідрофолатредуктази. В одному експерименті у мишей, яким давали NAD протягом тижня, поліпшувалося взаємодія клітинного ядра і мітохондрій[5].
Через величезну кількість оксидоредуктаз, що використовують NAD+ і NADH в якості субстратів і зв'язуються з ними за допомогою одного висококонсервативного структурного мотиву, ідея розроблення інгібітору, що блокує центр зв'язування NAD+, і специфічного лише для певного ферменту, здається сумнівною[6]. Однак це може бути здійсненним: так, інгібітори, засновані на мікофеноліновій кислоті й тіазофурині[en], пригнічують інозинмонофосфатдегідрогенази[en] у місті зв'язування з NAD+. Через важливу роль цього ферменту в метаболізмі пуринів ці сполуки можуть бути корисними протипухлинними і противірусними препаратами або імуносупресорами[6][7]. Інші препарати не є інгібіторами, а, навпаки, активаторами ферментів, залучених в метаболізм NAD+. Інші препарати не є інгібіторами, а, навпаки, активаторами ферментів, залучених у метаболізм NAD+. Зокрема, цікавою мішенню для таких препаратів можуть бути сиртуїни, бо активація цих NAD-залежних деацетілаз збільшують тривалість життя[8]. Такі сполуки, як резвератрол, збільшують активність цих ферментів, які можуть мати велике значення завдяки їх здатності до переносу старіння на пізніший строк як у хребетних[9], так і модельних організмів з числа безхребетних[10][11].
Через відмінності шляхів біосинтезу NAD+ у різних організмів, зокрема, між бактеріями і людиною, біосинтез NAD+ може стати новою сферою розвитку нових антибіотиків[12][13]. Наприклад, фермент нікотинамідаза[en], перетворює нікотинамід у нікотинову кислоту, слугує мішенню розроблюваних ліків, так як цей фермент відсутній у людини, але є у бактерій і дріжджів[14].
Історія

Кофермент NAD+ був відкритий англійськими біохіміками Артуром Гарденом та Вільямом Янґом[en] 1904 року[15]. Вони помітили, що додавання прокип'яченого і профільтрованого екстракту дріжджів до непрокип'ячених екстрактів значно посилювало спиртове бродіння в останніх. Невідомий фактор, відповідальний за це явище, вони назвали коферментом. У ході тривалого і складного виділення з екстрактів дріжджів цей теплостійкий фактор був ідентифікований як нуклеотид-сахарофосфат Гансом Ейлером-Хельпіном[16]. 1936 року німецький вчений Отто Генріх Варбург встановив функцію цього коферменту з перенесення гідридного йона і визначив, що в окисно-відновних реакціях бере участь нікотинамідний залишок[17].
Література
- Шлегель Г. Общая микробиология. Перевод с нем. Л. В. Алексеевой. М.: Мир, 1987. С. 567.
Примітки
- ↑ PMID 17465726 (PMID 17465726)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ PMID 16988050 (PMID 16988050)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ PMID 9805207 (PMID 9805207)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ PMID 14623976 (PMID 14623976)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ PMID 24360282 (PMID 24360282)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ а б PMID 15083807 (PMID 15083807)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ PMID 10390603 (PMID 10390603)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ PMID 19017485 (PMID 19017485)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ PMID 16461283 (PMID 16461283)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ PMID 12939617 (PMID 12939617)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ PMID 15254550 (PMID 15254550)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ PMID 12504674 (PMID 12504674)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ PMID 11153263 (PMID 11153263)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота. - ↑ Помилка цитування: Неправильний виклик тегу
<ref>: для виносок під назвоюRongvauxне вказано текст - ↑ (англ.) A. Harden, W. J. Young (24 жовтня 1906). The alcoholic ferment of yeast-juice Part II.--The coferment of yeast-juice. Proceedings of the Royal Society of London. Series B, Containing Papers of a Biological Character. 78 (526): 369—375. JSTOR 80144.
- ↑ (англ.) Fermentation of sugars and fermentative enzymes (PDF). Nobel Lecture, 23 May 1930. Nobel Foundation. Процитовано 30 вересня 2007.
- ↑ (нім.) Warburg O, Christian W. (1936). Pyridin, der wasserstoffübertragende bestandteil von gärungsfermenten (pyridin-nucleotide) [Pyridin, the hydrogen-transferring component of the fermentation enzymes (pyridine nucleotide)]. Biochemische Zeitschrift. 287: 291. doi:10.1002/hlca.193601901199.