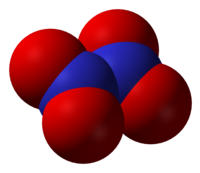
Азотний тетраоксид
| Азотний тетраоксид | |
|---|---|
| |
| Інші назви | динітроген тетраоксид |
| Ідентифікатори | |
| Номер CAS | 10544-72-6 |
| Номер EINECS | 234-126-4 |
| ChEBI | 29803 |
| RTECS | QW9800000 |
| SMILES | [N+](=O)([N+](=O)[O-])[O-][1] |
| InChI | InChI=1S/N2O4/c3-1(4)2(5)6 |
| Номер Гмеліна | 2249 |
| Властивості | |
| Молекулярна формула | N2O4 |
| Молярна маса | 92,011 г/моль |
| Зовнішній вигляд | летка рідина |
| Тпл | -11,2 °C |
| Ткип | 21,1 °C |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Те́трокси́д діазо́ту, азо́тний тетрокси́д (АТ, «аміл»[2]) — неорганічна сполука складу N2O4. Тетроксид утворюється при зрідженні та наступній димеризації оксиду NO2.
Являє собою жовтувато-коричневу летку рідину з їдким запахом; колір зумовлений домішкою діоксиду азоту. Температура кипіння при атмосферному тиску складає 21,15 °C, кристалізації −11 °С. Кристали при температурах нижче −12 °С безбарвні.
Хімічні властивості[ред. | ред. код]
За нормальних умов тетроксид азоту перебуває в рівновазі з діоксидом азоту:
- ; ΔH>O
При нагріванні повністю дисоціює до діоксиду азоту. Склад суміші залежить від температури і тиску. Зі зростанням температури рівновага зміщується до діоксиду азоту — окисник набуває бурого кольору. При зростанні тиску при постійній температурі ступінь дисоціації N2O4 зменшується, практично повністю дисоціює при 140 °C.
Реагує з водою утворюючи суміш нітратної і нітритної кислот:
Сильний окисник, високотоксичний і корозійний. Суміші з органічними речовинами вибухонебезпечні.
Використання[ред. | ред. код]
Широко використовується в ракетній техніці як висококиплячий (некріогенний) окисник ракетного палива.
В ракетних двигунах використовується в парі з паливами на основі похідних гідразину (метилгідразином, несиметричним диметилгідразином).
Раніше використовувався розчиненим в нітратій кислоті, через високу температуру переходу в твердий стан. Зокрема, в українських РН «Циклон»; російських «Космос», (у вигляді АК-27І), «Протон»; американських — родини «Титан»; французьких — родини «Аріан»; в рушійних установках пілотованих кораблів, супутників, орбітальних і міжпланетних станцій. Другий за частотою використання окисник палива після рідкого кисню.
В парі з алкілгідразинами утворює паливну пару, що самозаймається, з періодом затримки запалювання близько 0,003 с.
Зберігання[ред. | ред. код]
В резервуарах з легованої сталі або алюмінію об'ємом до 100 м³. Резервуари обладнують зливно-наливними трубами, запобіжними клапанами, манометрами і рівнемірами. Оскільки інтервал рідкого стану (262–294,3 °К) дуже малий, резервуари розміщують в заглиблених приміщеннях, де підтримується температура 268…288 К.
Особливістю зберігання є насичення компоненту азотом або повітрям і підтримання в резервуарі підвищеного тиску 0,15—0,22 МПа, для запобігання потрапляння в окисник з атмосфери вологи і забруднюючих речовин, а також для зменшення часу насичення газами при заправці ампульованих ракет. Заправлені ракети також перебувають під трохи вищим тиском, щоб уникнути кавітації в турбонасосному агрегаті (ТНА) при роботі рушійної установки.
Транспортування[ред. | ред. код]
Для транспортування використовуються спеціальні цистерни з ізоляцією і системою трубопроводів, в яку залежно від температури зовнішнього повітря подають теплу воду або охолоджувальний розчин.
Транспортується під надлишковим тиском 0,1—0,15 МПа. Використовуються залізничні цистерни ємністю близько 40 м³, автоцистерни — 30—60 м³. Залізничні й автомобільні цистерни обладнані зливно-наливними трубами, запобіжними клапанами, манометрами і рівнемірами.
Посилання[ред. | ред. код]
- NIOSH Pocket Guide to Chemical Hazards — Nitrogen Dioxide [Архівовано 28 жовтня 2020 у Wayback Machine.]
Примітки[ред. | ред. код]
| Ця стаття потребує додаткових посилань на джерела для поліпшення її перевірності. (грудень 2014) |
| Це незавершена стаття про неорганічну сполуку. Ви можете допомогти проєкту, виправивши або дописавши її. |

