Оксалілхлорид
| Оксалілхлорид | |
|---|---|
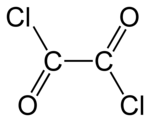 Oxalyl chloride
| |

| |
 |
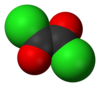 |
| Систематична назва | Етандиоїл дихлорид |
| Інші назви | Щавлевої кислоти хлорид Щавлевої кислоти дихлорид (1:2) Щавлевої кислоти дихлорид Оксалоїлхлорид |
| Ідентифікатори | |
| Номер CAS | 79-37-8 |
| PubChem | 65578 |
| Номер EINECS | 201-200-2 |
| RTECS | KI2950000 |
| SMILES | ClC(=O)C(=O)Cl |
| InChI | 1/C2Cl2O2/c3-1(5)2(4)6 |
| Властивості | |
| Молекулярна формула | C2O2Cl2 |
| Молярна маса | 126.93 г/моль |
| Зовнішній вигляд | Безбарвна рідина |
| Запах | фосгеноподібний[1] |
| Густина | 1.4785 г/мл |
| Тпл | -16 |
| Розчинність (вода) | реагує |
| Показник заломлення (nD) | 1.429 |
| Небезпеки | |
| ГГС піктограми |   [2] [2]
|
| ГГС формулювання небезпек | 314, 331 |
| ГГС запобіжних заходів | 261, 280, 305+351+338, 310 |
| Головні небезпеки | Токсичний, корозійний, лакриматор[2] |
| NFPA 704 | |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Оксалілхлорид — органічна хімічна сполука з формулою (COCl)2. Безбарвна рідина з різким запахом, диацилхлорид щавлевої кислоти, є популярним реагентом в органічному синтезі[3].
Одержання[ред. | ред. код]
Оксалілхлорид вперше був одержаний у 1892 році французьким хіміком Адрієном Фоконьє, реакцією діетилоксалату з пентахлоридом фосфору[4]. Його також одержують шляхом обробки щавлевої кислоти пентахлоридом фосфору[5].
Оксалілхлорид промислово виробляють з етиленкарбонату. Фотохлорування дає тетрахлорид, який згодом розкладається:
- C2H4O2CO + 4 Cl2 → C2Cl4O2CO + 4 HCl
- C2Cl4O2CO → C2O2Cl2 + COCl 2
Реакції[ред. | ред. код]
Оксалілхлорид реагує з водою, утворюючи лише газоподібні продукти: хлористий водень (HCl), вуглекислий газ (CO 2 ) і оксид вуглецю (CO).
- (COCl)2 + H2O → 2 HCl + CO2 + CO
Цим він значно відрізняється від інших ацилхлоридів, які гідролізуються з утворенням хлористого водню та вихідної карбонової кислоти .
Застосування в органічному синтезі[ред. | ред. код]
Окислення спиртів[ред. | ред. код]
Розчин, що містить ДМСО та оксалілхлорид, з подальшим додаванням триетиламіну перетворює спирти на відповідні альдегіди та кетони за допомогою процесу, відомого як окиснення Сверна[6][7][8].
Синтез ацилхлоридів[ред. | ред. код]
Оксалілхлорид зазвичай використовується N, N -диметилформамідом як каталізатором в органічному синтезі для одержання ацилхлоридів з відповідних карбонових кислот. Подібно до тіонілхлориду, у цій реакції реагент розкладається на леткі побічні продукти, що спрощує обробку. Одним із другорядних побічних продуктів реакції, що каталізується N,N-диметилформамідом, є сильний канцероген, що виникає внаслідок розкладання N,N-диметилформаміду[9]. Порівняно з тіонілхлоридом оксалілхлорид має тенденцію бути більш м’яким і селективнішим реагентом. Він також дорожчий, ніж тіонілхлорид, тому його, як правило, використовують у менших масштабах.
Ця реакція включає перетворення ДМФА в похідне імідоїлхлориду (Me2N=CHCl+), схоже на першу стадію в реакції Вільсмаєра–Хака. Імідоілхлорид є активним хлоруючим агентом.
Формілювання аренів[ред. | ред. код]
Оксалілхлорид реагує з ароматичними сполуками в присутності хлориду алюмінію з утворенням відповідного ацилхлориду в процесі, відомому як ацилювання Фріделя-Крафтса[10][11]. Одержаний ацилхлорид можна гідролізувати з утворенням відповідної карбонової кислоти.
Одержання оксалатних діефірів[ред. | ред. код]
Як і інші ацилхлориди, оксалілхлорид реагує зі спиртами з утворенням естерів:
- 2 RCH2OH + (COCl)2 → RCH2OC(O)C(O)OCH2R + 2 HCl
Як правило, такі реакції проводять у присутності основи, такої як піридин. Діефір, отриманий з фенолу, ефір фенілового оксалату, є ціалумом, активним інгредієнтом світлових паличок.
Інше[ред. | ред. код]
Повідомляється, що оксалілхлорид був використаний у першому синтезі діоксантетракетону (C4O6), оксиду вуглецю[12].
Запобіжні заходи[ред. | ред. код]
У березні 2000 року Airbus A330-300 авіакомпанії Malaysia Airlines отримав пошкодження, які не підлягали ремонту, після витоку забороненого для перевезення оксалілхлориду (помилково декларованого як гідроксихінолін) у вантажний відсік[13]. Він токсичний при вдиханні, хоча більш ніж на порядок менш токсичний, ніж споріднена сполука фосген[14].
Див. також[ред. | ред. код]
- Оксаліл
- Окислення Сверна
Примітки[ред. | ред. код]
- ↑ Oxalyl chloride: odor
- ↑ а б в г Oxalyl chloride MSDS (PDF). Архів оригіналу (PDF) за 23 вересня 2015. Процитовано 2 березня 2023.
- ↑ Salmon, R. (2001). Encyclopedia of Reagents for Organic Synthesis. New York: John Wiley & Sons. doi:10.1002/047084289X.ro015. ISBN 0471936235.
{{cite encyclopedia}}: Пропущений або порожній|title=(довідка) - ↑ Fauconnier, Adrien (1892). Action du perchlorure de phosphore sur l'oxalate d'éthyle [The action of phosphorus pentachloride on diethyl oxalate]. Comptes rendus hebdomadaires des séances de l'Académie des Sciences (фр.). 114: 122—123.
- ↑ [1]
- ↑ Synthesis of 1,1-Dimethyl Ethyl-(S)-4-formyl-2,2-dimethyl-3-oxazolidinecarboxylate by Oxidation of the Alcohol, Org. Synth., 2004
- ↑ 9-Thiabicyclo[3.3.1]nonane-2,6-dione, Org. Synth., 1998
- ↑ Selective hydroboration of a 1,3,7-triene: Homogeraniol, Org. Synth., 1990
- ↑ Clayden, Jonathan (2005). Organic chemistry (вид. Reprinted(with corrections)). Oxford [u.a.]: Oxford Univ. Press. с. 296. ISBN 978-0-19-850346-0.
- ↑ Preparation of 4-Alkyl- and 4-Halobenzoyl Chlorides: 4-Pentylbenzoyl Chloride, Org. Synth., 61: 8
- ↑ Mesitoic Acid, Org. Synth., 44: 69
- ↑ Strazzolini, P.; Gambi, A.; Giumanini, A. G.; Vancik, H. (1998). The reaction between ethanedioyl (oxalyl) dihalides and Ag2C2O4: a route to Staudinger's elusive ethanedioic (oxalic) acid anhydride. Journal of the Chemical Society, Perkin Transactions 1. 1998 (16): 2553—2558. doi:10.1039/a803430c.
- ↑ Firm told to pay $65 mln for ruining plane. Reuters. 6 грудня 2007. Процитовано 6 грудня 2007.
- ↑ Barbee, S.J.; Stone, J.J.; Hilaski, R.J. (January 1995). Acute Inhalation Toxicology of Oxalyl Chloride. American Industrial Hygiene Association Journal (англ.). 56 (1): 74—76. doi:10.1080/15428119591017358. ISSN 0002-8894. PMID 7872205.
|

