Вірус гепатиту C
| Ця стаття в процесі редагування певний час. Будь ласка, не редагуйте її, бо Ваші зміни можуть бути втрачені. Якщо ця сторінка не редагувалася кілька днів, будь ласка, приберіть цей шаблон. Це повідомлення призначене для уникнення конфліктів редагування. Останнє редагування зробив користувач Шкурба Андрій Вікторович (внесок, журнали) о 23:01 UTC (1164696 хвилин тому). |
Вірус гепатиту C (англ. hepatitis C virus (HCV)) — невеликий одноланцюговий позитивно спрямований РНК-вмісний вірус родини Flaviviridae. Є збудником вірусного гепатиту C, при якому часто розвивається окрім гепатиту ще й широкий спектр уражень інших органів і систем, насамперед цироз печінки і гепатоцелюлярну карциному.
Таксономія
| Hepatitis C virus / вірус гепатиту C | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
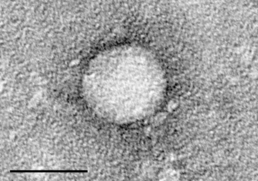 Електронна мікрофотографія вірусу C, очищеного з клітинної культури.
| ||||||||||
| Класифікація вірусів | ||||||||||
| ||||||||||
| Синоніми | ||||||||||
| Вірус гепатиту C, Hepatitis C virus | ||||||||||
Посилання
| ||||||||||
|
Вірус належить до роду Hepacivirus. Один вид цього роду був виявлений у собак: собачий гепацивірус. У цьому роду також є принаймні один вид, який уражає коней. Кілька видів описано у кажанів і гризунів. Ізоляти вірусу згруповані в сім генотипів і ряд підтипів із чітким географічним розподілом і чутливістю до лікування на основі інтерферону.
Структура
Частка вірусу гепатиту С складається з ліпідної оболонки. Два глікопротеїни вірусної оболонки, E1 (E1[en]) і E2 (E2[en]), вбудовані до неї. E1 і E2 ковалентно зв'язані, коли вони вбудовуються в оболонку вірусу, і стабілізуються дисульфідними зв'язками. E2 має кулясту форму і, за даними спостереження при електронній мікроскопії, виступає на 6 нм із мембрани оболонки. Ці глікопротеїни відіграють важливу роль у взаємодії вірусу гепатиту С з імунною системою людини. На глікопротеїні E2 є гіперваріабельна ділянка. Вона є гнучкою і цілком доступною для навколишніх молекул. Допомагає E2 захистити вірус від імунної системи, запобігає причепленню CD81 до відповідного рецептора вірусу. Крім того, Е2 може захистити і Е1 від імунної системи. Хоча цю ділянку складає досить варіабельна амінокислотна послідовність, гіперваріабельна ділянка має схожі хімічні, фізичні та конформаційні характеристики для багатьох E2 глікопротеїнів.
Геном
Геном складається з однієї відкритої рамки зчитування, яка завдовжки у 9600 нуклеотидних основ. Ця єдина відкрита рамка зчитування перетворюється на отримання єдиного білкового продукту, який згодом обробляється для отримання менших активних білків. Через це в загальнодоступних вірусних базах даних вірусний протеом складається лише з 2 білків. На 5′ і 3′ кінцях РНК знаходяться нетрансльовані ділянки, які не транслюються в білки, але важливі для трансляції та реплікації вірусної РНК. 5′ кінець має сайт зв'язування рибосоми, який ініціює трансляцію дуже протяжного білка, що містить близько 3000 амінокислот. Основний домен HCV IRES (Hepatitis C virus internal ribosome entry site[en]) містить чотиристоронню гвинтову структуру Холлідея, яка інтегрована у передбачений псевдовузол (pseudoknot[en]). Конформація цього основного домену обмежує орієнтацію відкритої рамки зчитування для позиціонування на рибосомній субодиниці 40S. Великий білок-попереднік пізніше розщеплюється клітинними та вірусними протеазами на 10 менших білків, які забезпечують реплікацію вірусу в клітині-хазяїні або збираються у зрілі вірусні частинки. Структурні білки, що виробляються вірусом гепатиту С, включають коровий білок (HCVcor), Е1 і Е2. Неструктурні білки включають NS2, NS3, NS4A, NS4B, NS5A і NS5B. На виявленні антитіл до них частково ґрунтується серологічна діагностика гепатиту C.

Молекулярна біологія
Білки вірусу гепатиту C розташовані вздовж генома в такій послідовності: N-термінальна оболонка-ядро-оболонка (E1)–E2–p7-неструктурний білок 2 (NS2)–NS3–NS4A–NS4B–NS5A–NS5B–C кінцевий. Покоління зрілих неструктурних білків (NS2 — NS5B) залежить від активності вірусних протеїназ. З'єднання NS2/NS3 розщеплюється металзалежною автокаталітичною протеїназою, що кодується всередині NS2 та N-кінця NS3. Решта розщеплення каталізуються сериновою протеазою, яка також міститься в N-кінцевій області NS3.
Основний білок містить 191 амінокислоту і за гідрофобністю його можна розділити на три домени:
- домен 1 (залишки 1–117) містить переважно основні залишки з двома короткими гідрофобними ділянками;
- домен 2 (залишки 118—174) менш основний і більш гідрофобний, а його С-кінець знаходиться на кінці p21;
- домен 3 (залишки 175—191) дуже гідрофобний і діє як сигнальна послідовність для білка оболонки E1.
Обидва білки оболонки (E1 і E2) високоглікозильовані, є важливими для проникнення в клітину. E1 є фузогенною субодиницею, а E2 діє як білок, що зв'язує рецептор. E1 має 4–5 N-зв'язаних гліканів, а E2 — 11 сайтів N-глікозилювання.
Білок NS1 (p7), необхідний для реплікації вірусного геному, відіграє вирішальну роль у морфогенезі вірусу. Цей білок складається з 63 амінокислот, що охоплюють мембрану, яка розташовується в ендоплазматичній мережі. Розщеплення p7 опосередковується сигнальними пептидазами ендоплазматичної мережі. Два трансмембранних домени (transmembrane domain[en]) р7 з'єднані цитоплазматичною петлею і орієнтовані в бік просвіту ендоплазматичної мережі.
Білок NS2 є трансмембранним білком масою 21–23 кДа, з протеазною активністю.
NS3 є білком масою 67 кДа, N-кінець якого має активність серинової протеази, а С-кіненць має активність НТФази/гелікази. Він розташований всередині ендоплазматичного ретикулума і утворює гетеродимерний комплекс із NS4A — мембранним білком із 54 амінокислот, який діє як кофактор протеїнази.
NS4B є невеликим (27 кДа) гідрофобним інтегральним мембранним білком із чотирма трансмембранними доменами. Він міститься всередині ендоплазматичної сітки і відіграє важливу роль у залученні інших вірусних білків. Спричинює морфологічні зміни в ендоплазматичному ретикулумі, утворюючи структуру — мембранну павутину.
NS5A є гідрофільним фосфопротеїном, який відіграє важливу роль у реплікації вірусу, модуляції клітинних сигнальних шляхів та інтерферонової відповіді. Виявлено, що він зв'язується з білками VAP людини, закріпленими на ендоплазматичному ретикулумі.
Білок NS5B (65 кДа) являє собою вірусну РНК-залежна РНК-полімеразу. Виконує ключову функцію реплікації вірусної РНК ВГС, використовуючи позитивний ланцюг РНК вірусу як свою матрицю, і каталізує полімеризацію рибонуклеозидтрифосфатів під час реплікації РНК. Декілька кристалічних структур полімерази NS5B у кількох кристалічних формах було визначено на основі однієї консенсусної послідовності HCV-BK, генотип 1. Конструкція може бути представлена формою правої руки з пальцями, долонею та великим пальцем. Активний центр, унікальний для NS5B, міститься в структурі долоні білка. Нещодавні дослідження структури білка NS5B генотипу 1b штаму J4 (HC-J4) вказують на наявність активного центру, де можливий контроль зв'язування нуклеотидів та ініціація синтезу нової РНК. Додає необхідні праймери для ініціації реплікації РНК. Сучасні дослідження намагаються зв'язати структури з цим активним сайтом, щоб змінити його функціональність, щоб запобігти подальшій реплікації вірусної РНК.
Описаний 11-й білок, який кодується зсувом рамки +1 в гені капсида. Його функція достеменно невідома.
Примітки
Джерела
- Dubuisson, Jean; Cosset, François-Loïc (2014). «Virology and cell biology of the hepatitis C virus life cycle — An update». Journal of Hepatology. 61 (1): S3–S13. doi:10.1016/j.jhep.2014.06.031. PMID 25443344. [1] (англ.)
- Genus: Hepacivirus [2] (англ.)
- Kato N (2000). «Genome of human hepatitis C virus (HCV): gene organization, sequence diversity, and variation». Microb. Comp. Genom. 5 (3): 129–51. doi:10.1089/mcg.2000.5.129. PMID 11252351 (англ.)
- Sanjiv Chopra Characteristics of the hepatitis C virus. UpToDate Sep 14, 2021.[3] (англ.)
Посилання
- Hepatitis C virus (англ.)
|
|