Супрамолекулярна хімія
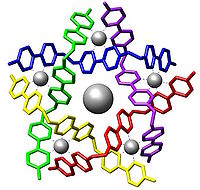
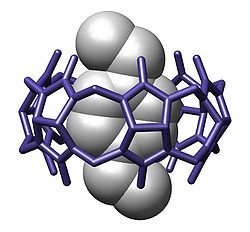
Су́прамолекуля́рна хі́мія — міждисциплінарна галузь хімії, що зосереджується на вивчені хімічних систем, що складаються з певної визначеної кількості молекулярних блоків чи компонентів, індивідуальні властивості яких інтегровані у властивості всього ансамблю[2].
Загальний опис[ред. | ред. код]
Фундаментальні причини та особливості[ред. | ред. код]
Сили, що відповідають за просторову організацію можуть варіюватися від слабких (міжмолекулярні, електростатичні сили чи водневий зв'язок) до сильних (наближаючись до ковалентних зв'язків), за умови, що ступінь електростатичної взаємодії між молекулярними компонентами залишається малим по відношенню до відповідних енергетичних параметрів компоненту[3][4].
Супрамолекулярна хімія як наука[ред. | ред. код]
Головна проблема, яку вивчає супрамолекулярна хімія — дослідження будови та властивостей надмолекулярних структур, які утворюються за рахунок невалентних взаємодій (водневий зв'язок, електростатичні взаємодії, гідрофобні сили) та існують і функціонують як хімічні індивіди. Енергія таких взаємодій є невеликою і тому лише участь багатьох центрів зв'язування може привести до більш сильної взаємодії між окремими частинками. Молекули в супрамолекулярній структурі (частинці), попри певні зміни, зберігають свою хімічну індивідуальність. Супрамолекулярна хімія торкається вивчення практично усіх органічних систем, по суті є місточком між класичною хімією і біологією. Сюди відносять, зокрема, асоціацію пептидів, утворення льоду, реологічні властивості нафти, поведінка світла в тонких плівках, властивості кераміки. Супрамолекулярна хімія має перспективу створення найсучасніших «хай-текових» технологій, нанотехнологій, що ведуть до створення нових матеріалів, надмалих електронних у тому числі біосумісних пристроїв (чипів), а також вирішення проблем екології. Так шкідливі забруднювачі (важкі метали тощо) можуть бути видалені із застосуванням систем здатних до молекулярного розпізнання.
Зв'язок із органічною хімією[ред. | ред. код]
Створення супрамолекулярних пристроїв (механізмів) включає у себе синтез органічних молекул, які несуть відповідну функцію, створення організованих багатомолекулярних ансамблів та створення молекулярних пристроїв.
Конструювання органічних молекул є задачею молекулярної хімії, яка вивчає питання організації окремих атомів, сполучення їх між собою та їх розташування один відносно одного з метою досягнення необхідних координаційних характеристик.
Зв'язок із традиційною хімією[ред. | ред. код]
Стандартні способи орієнтації матеріалів (кристалізація, орієнтація у потоці, епітаксія тощо) є непридатними для конструювання ансамблів молекулярних розмірів. Така задача вирішується шляхом самоорганізації й примусової організації. Раптове формування подвійної спіралі нуклеїнових кислот, під час якого відбувається розпізнавання й селективне спарювання остовів - класичний приклад самоорганізації. Іншим прикладом є самоорганізація моношарів алкілсилоксанів, жирних кислот, диалкілсульфідів, диалкілдисульфідів й тіолів на алюмінії, сріблі, золоті, оксиді кремнію тощо. Метод Ленгмюра-Блоджет є примусовим, оскільки формування моношару із заданою організацією на поверхні води й його перенесення на твердий остов потребує енергетичних витрат. Лише таким методом можуть бути отримані надґратки, тобто нанометрові шари органічних молекул, які впорядковані слідуванням по товщині. Застосування цього методу завжди призводить до утворення супрамолекулярних ансамблів, властивості яких визначаються злагодженою поведінкою молекул, що їх утворюють. Щоб така супрамолекулярна конструкція була пристроєм (механізмом), вона повинна бути наділена певною функціональністю з огляду на прагматику інженера. Ця проблема вирішується на більш високому рівні.
У той час як традиційна хімія зосереджується на ковалентному зв'язку, супрамолекулярна хімія вивчає слабші та оборотні нековалентні взаємодії між молекулами. Ці сили включають водневі зв'язки, сили ван дер Ваальса, пі-пі взаємодію, електростатичні ефекти тощо. Важливими концепціями супрамолекулярної хімії є молекулярна самоорганізація, фолдинг, молекулярне розпізнання, комплекс гість-господар, молекулярні ансамблі типу ключ-замок та ін.[5] Вивчення нековалентних взаємодій є надзвичайно важливим до розуміння біологічних процесів від клітинної структури до розуміння того, як залежить від цих сил структура та функції біологічних систем, тому останні дуже часто стають об'єктами інтенсивних супрамолекулярних досліджень.
| Цей розділ потребує доповнення. |
Історія[ред. | ред. код]
Супрамолекулярна хімія вважається відносно молодою наукою, яка бере свій початок з кінця 1960-х — початку 1970-х років. Попри це, її концепції та уявлення, а також велика кількість простих (і не зовсім простих) супрамолекулярних хімічних систем були відомі з самого зародження хімії[2]. 1810 року Гемфрі Деві отримав газовий гідрат хлору, ця сполука належить до класу клатратів (газових гідратів). 1823 року Майкл Фарадей вивів формулу цього клатрата[2].
Існування міжмолекулярних зв'язків вперше відкрив Ян Дидерик ван дер Ваальс у 1873 році. Крім того, лауреат Нобелівської премії Герман Еміль Фішер розробив філософське підґрунтя супрамолекулярної хімії. У 1894 році[6], Фішер припустив, що фермент-субстратна взаємодія має форму «ключ-замок», сформулював основоположні принципи молекулярного розпізнавання та хімії гість-хазяїн[en]. На початку ХХ століття нековалентні зв'язки були вивчені більш детально, а водневий зв'язок був описаний Латімером та Родебушем в 1920 році.
Використання цих принципів призвело до покращення розуміння структури білків та біологічних процесів. Наприклад, важливий прорив, який дозволив виявити подвійну спіральну структуру в ДНК стався, коли стало зрозуміло, що є два окремих ланцюга нуклеотидів, пов'язаних водневими зв'язками. Використання нековалентних зв'язків має важливе значення для реплікації, оскільки вони дозволяють розділюватися ланцюгу і використовуватися як матриці нового дволанцюгового ДНК. Одночасно хіміки почали розпізнавати і вивчати синтетичні структури, засновані на нековалентних взаємодіях, таких як міцели та мікроемульсії.

Супрамолекулярні йонні канали[ред. | ред. код]
Природні транспорті білки характеризуються високим ступенем регульованості. Їх перехід з зачиненого у відчинений (або провідний) стан зазвичай відбувається в результаті певного процесу: фосфорилювання, зв'язування малих молекул (ацетилхоліну, катіонів кальцію тощо) або зміни трансмембранного потенціалу. Більшість штучних йонних каналів не регулюються: вони переходять із зачиненого стану у відчинений в результаті випадкових агрегаційних процесів у ліпідному бішарі.
У роботах[7][8] повідомляється про створення потенціал-залежних йонних каналів на основі холевої кислоти та її похідних. Довжина каналів, які формуються цими сполуками, приблизно складає 40 Ангстрем. Жорсткі амфіфільні стероїдні скелети сполук 10-13 позитивно впливають на стабільність утворюваних каналів.
Див. також[ред. | ред. код]
Примітки[ред. | ред. код]
- ↑ Hasenknopf, Bernold (1996). Self-Assembly of a Circular Double Helicate. Angewandte Chemie International Edition in English. 35: 1838. doi:10.1002/anie.199618381.
{{cite journal}}:|first2=з пропущеним|last2=(довідка);|first3=з пропущеним|last3=(довідка);|first4=з пропущеним|last4=(довідка);|first5=з пропущеним|last5=(довідка) - ↑ а б в Дж.В. Стид, Дж.Л.Этвуд (2007). Супрамолекулярная химия 1 Т. (Російська) . Москва: ИКЦ "Академкнига". с. 31. ISBN 978-5-94628-305-2.
- ↑ Lehn JM (1993). Supramolecular chemistry. Science. 260 (5115): 1762—3. doi:10.1126/science.8511582. PMID 8511582.
- ↑ Supramolecular Chemistry, J.-M. Lehn, Wiley-VCH (1995) ISBN 978-3-527-29311-7
- ↑ Gennady V. Oshovsky, Dr. Dr., David N. Reinhoudt, Prof. Dr. Ir., Willem Verboom, Dr. (2007). Supramolecular Chemistry in Water. Angewandte Chemie International Edition. 46 (14): 2366—2393. doi:10.1002/anie.200602815.
- ↑ Fischer, E. (1894). Einfluss der Configuration auf die Wirkung der Enzyme. Berichte der deutschen chemischen Gesellschaft (нім.). 27 (3): 2985. doi:10.1002/cber.18940270364.
- ↑ Y.Kobuke, T.Nagatani. J.Org.Chem.,66,5094(2001).
- ↑ Ch.Goto,M.Yammamura,A.Satake,Y.Kobuke.J.Am.Chem.Soc.,114,7618 (1992).
Література[ред. | ред. код]
- Прикладна супрамолекулярна хімія / В. І. Рибаченко, Богуміл Бжезінскі, Л. І. Опейда, Богуслава Ленска, Н. І. Борисенко, Рафаїл Франьскі, Петро Пшибільскі, Іоанна Вирнал, Н. В. Ляпченко. За ред. Г.Шредера, В.Рибаченка та Й.Опейди. — Донецьк: ТОВ Юго-Восток Лтд., 2005. — 268 с.
- Gdaniec M., Ibragimov B.T., Talipov S.A. Supramolecular Chemistry, vol. 6, Pergamon, Oxford, 1996.
- Мала гірнича енциклопедія : у 3 т. / за ред. В. С. Білецького. — Д. : Східний видавничий дім, 2013. — Т. 3 : С — Я. — 644 с.
- Глосарій термінів з хімії / Укладачі Й. Опейда, О. Швайка. Інститут фізико-органічної хімії і вуглехімії ім. Л. М. Литвиненка, Донецький національний університет. — Донецьк : Видавництво «Вебер», 2008. — 758 с.

|
Це незавершена стаття з хімії. Ви можете допомогти проєкту, виправивши або дописавши її. |
| |||||||||||||||||||||||||||||||||||
