Ізотопи

По горизонталі — кількість протонів (заряд ядра).
По вертикалі — кількість нейтронів.
Колір — стабільність ізотопу (тривалість напіврозпаду).
Ізото́пи — нукліди одного і того самого хімічного елементу, які мають різну кількість нейтронів, а, отже, різне масове число і різну атомну масу.
Загальний опис[ред. | ред. код]
Ізотопи позначають тими самими символами, що й хімічний елемент, додаючи зверху з лівого боку символу масове число, наприклад, ізотопи хлору позначають: 35Cl і 37Cl, або масове число подають після назви чи символу елементу, наприклад: уран-233 чи Pu-239.
Ізотопи одного хімічного елемента мають однаковий заряд атомного ядра, тобто один порядковий номер, і займають те ж саме місце в періодичній системі, мають однакову кількість протонів в ядрі атома, але відрізняються один від одного кількістю нейтронів. Так, в атомному ядрі ізотопу хлору 35Cl міститься 17 протонів, оскільки порядковий номер хлору 17, і 18 нейтронів (35-17=18), а в ядрі ізотопу хлору 37Cl — 17 протонів і 20 нейтронів (37-17 = 20).
Деякі хімічні елементи мають невелику кількість стабільних ізотопів. Так, для кисню відомо три стабільні ізотопи: 16O (ядро складається з 8 протонів і 8 нейтронів), 17O (ядро складається з 8 протонів і 9 нейтронів) і 18О (ядро складається з 8 протонів і 10 нейтронів). Для водню відомо теж три ізотопи: 1H (ядро складається лише з одного протона), 2H (ядро складається з одного протона і одного нейтрона), 3H (ядро складається з одного протона і двох нейтронів). Деякі ж хімічні елементи складаються з досить великої кількості ізотопів. Наприклад, ксенон має 9 ізотопів у природній суміші, олово — 10 і т. д.; для цих елементів також відомі десятки штучних радіоактивних ізотопів.
Переважна більшість ізотопів не має спеціальних назв, але для ізотопів деяких елементів, зокрема для ізотопів водню, існують спеціальні назви і навіть спеціальні символи. Так, ізотоп водню 1H називають протій, ізотоп 2H — дейтерій і позначають символом D, а ізотоп 3Н — тритій (символ T).
Деякі ізотопи в природі досить поширені, як, наприклад, ізотоп кисню 16O та ізотоп водню 1Н, а інші ізотопи зустрічаються в дуже мізерних кількостях, як ізотопи кисню 17O і 18O і ізотопи водню 2H і 3H.
За хімічними властивостями всі ізотопи окремого елементу дуже близькі, тому значної різниці між ними у хімічних реакціях не спостерігається. Виняток становлять лише ізотопи водню, які за своїми властивостями помітно відрізняються один від одного.
Атомна маса ізотопу виражена у вуглецевих одиницях і не є цілим числом для всіх елементів окрім С-12, на відміну від масового числа, яке є завжди цілим числом, рівним сумі протонів та нейтронів.
Історія[ред. | ред. код]

До 20 століття загальноприйнятою була думка, що атомна маса елементу є його постійною і незмінною характеристикою. Проте, з відкриттям наприкінці 19 століття радіоактивних речовин, це уявлення почало змінюватися.
Під час радіоактивного розпаду утворювалися елементи, що, через їх різну атомну масу, вважали різними, і давали їм окремі назви. У 1910 році Фредерік Содді показав, що мезоторій (тодішня назва радію-228), радій (радій-226, довгоживучий ізотоп, що зустрічається в природі) і торій-X (радій-224) хімічно нероздільні. А в 1913 році він же показав, що під час розпадів радіоактивних речовин на проміжку від урану до свинцю утворюється близько 40 радіоелементів з різною масою, тоді як у таблиці Менделєєва між цими елементами може розміщуватись не більш як 11 інших.
Того самого року Содді й Казимір Фаянс запропонували закон радіоактивних зміщень, згідно з яким альфа-розпад зміщує елемент у таблиці на дві позиції вліво, зменшуючи його масу на 4, тоді як бета-розпад — на одну позицію вправо, залишаючи масу незмінною. Таким чином, альфа-розпад, що супроводжується двома бета-розпадами, породжує елемент, що не відрізняється від материнського хімічно, проте має меншу атомну масу.
Сам термін "ізотоп", що з грецької можна перекласти як "в тому самому місці", Содді підказала шотландський фізик Маргарет Тодд під час бесіди, у якій той поділився з нею своїми ідеями.[1]
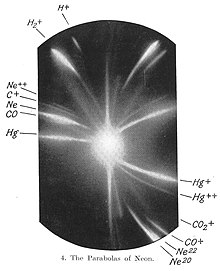
Пізніше були відкрито, що деякі нерадіоактивні елементи є сумішшю кількох стабільних ізотопів. Першим елементом, для якого були відкриті такі ізотопи був неон: у 1913 році Джозеф Томпсон показав, що у природному неоні присутні дві фракції з атомними масами 20 і 22. З розвитком мас-спектрометрії виявляти такі ізотопи стало простіше. У 1919 році Френсіс Астон відкрив велику кількість елементів, що мають кілька стабільних ізотопів. Крім того, Астон показав, що усі ізотопи мають атомні маси пропорційні до атомної маси водню, а елементи, атомна маса яких відхиляється від цього правила, є сумішами ізотопів. Наприклад, хлор у природі існує у вигляді двох ізотопів з масами 35 і 37, а його атомна маса, що вважалася рівною 35.45, насправді є середнім зваженим мас цих ізотопів (відповідно до їх часток у природному хлорі).[2]
І Фредерік Содді і Френсіс Астон за свої роботи з відкриття і дослідження ізотопів отримали нобелівські премії з хімії, у 1921 і 1922 році відповідно.[3]
У 1932 році був відкритий нейтрон, і згодом стало зрозуміло, що саме різна кількість нейтронів у ядрі відрізняє ізотопи один від одного. У 1934 році Фредерік та Ірен Жоліо-Кюрі виявили, що при бомбардуванні легких елементів альфа-частинками утворюються короткоживучі ізотопи деяких легких елементів, а розпад таких ізотопів іде по невідомому раніше каналу (β+), і супроводжується емісією позитронів[4]. В той же час Енріко Фермі показав, що опромінення стабільних елементів нейтронами призводить до їх захоплення ядрами, і утворення нових ізотопів цих же елементів. Усі ці явища отримали назву штучна радіоактивність. За допомогою таких методів фізики отримали можливість створювати велику кількість нестабільних ізотопів.
Стабільність[ред. | ред. код]
Більшість відомих ізотопів нестабільні щодо радіоактивного розпаду. Характеристиками нестабільних ізотопів є період напіврозпаду та канал розпаду. Основними каналами розпаду є бета-радіоактивність та альфа-радіоактивність. При бета-розпаді ядро ізотопу випромінює електрон або позитрон і, відповідно, або збільшує, або зменшує свій атомний номер. При альфа-розпаді ядро ізотопу випромінює альфа-частинку, і відповідно, його атомний номер зменшується на двійку, а масове число на 4. Деякі ізотопи, наприклад, 235U, можуть ділитися.
Період напіврозпаду нестабільних ізотопів може бути дуже різним, від 1× 10-24 c до значень, що перевищують вік Всесвіту. В останньому випадку слабку радіоактивність можна зареєструвати точними вимірюваннями, однак ізотоп можна вважати практично стабільним.
В навколишній природі зустрічаються здебільшого стабільні ізотопи хімічних елементів, оскільки нестабільні врешті-решт розпадаються. Однак вони також і утворюються внаслідок ядерних реакцій.
Загалом, існує 254 стабільних ізотопи, що належать 81 елементу, при тому, що загалом відомо 3339 різних ізотопів[5]. З цих ізотопів, теоретично, лише 90 є повністю стабільними, а решта просто має дуже довгі періоди напіврозпаду, проте на практиці їх розпад не спостерігався.
Розподіл елементів за кількістю стабільних ізотопів такий:[6]
- 10 стабільних ізотопів — 1 елемент (олово)
- 8 стабільних ізотопів — 1 елемент (ксенон)
- 7 стабільних ізотопів у чотирьох елементів
- 6 стабільних ізотопів мають вісім елементів
- 5 стабільних ізотопів мають десять елементів
- 4 стабільних ізотопи є у дев'яти елементів
- три стабільні ізотопи є у п'яти елементів
- 16 елементів мають два стабільні ізотопи, рахуючи метастабільний збуджений стан танталу-180m
- 26 елементів представлені лише одним нуклідом
Розділення ізотопів[ред. | ред. код]
У багатьох галузях використовуються речовини зі зміщеним ізотопним складом. В першу чергу це стосується урану, радіоактивний нуклід якого (з атомною масою 235), є вкрай вживаним у виробництві зброї, ядерній енергетиці, тощо. Загалом, проблема розділення ізотопів є вкрай складною, через те, що хімічно вони практично еквівалентні.
Існує дві великих групи методів розділення ізотопів: абсолютні методи, які дозволяють виділити ізотопи в чистому вигляді, а також методи, що лише збільшують концентрацію деякого нукліду.
До абсолютних методів відносять:
- Електромагнітне розділення: суміш ізотопів випаровують і іонізують, прискорюють електричним полем, після чого запускають в камеру з магнітним полем, перпендикулярним напрямку руху іонів. Таким чином, відхилення окремих атомів у полі є пропорційним відношенню m/z (яке є різним для різних ізотопів), і суміш розділяється на окремі пучки ізотопів, що вловлюються і відокремлюються.
- Лазерне розділення, що працює завдяки тому, що молекули, що містять різні ізотопи, збуджуються під дією світла різної частоти. Потім збуджені молекули відокремлюються електричним полем чи будь-яким іншим способом.
Проте, хоча абсолютне розділення здається більш ефективним, через велику вартість, в промислових масштабах воно використовується порівняно рідше. Натомість застосовується велика кількість методів, що ненабагато зміщує пропорції ізотопів у зразку. Для того, щоб отримати порівняно чистий ізотоп, ці методи треба застосовувати багато разів. Щоб оцінити ефективність розділення, використовується показник, що називається коефіцієнт сепарації, що розраховується як , де N1 і N2 — концентрації ізотопу, що виділяється, у збагаченій і у збідненій фракції. Серед методів такого типу можна відмітити такі[7]:
- Газова дифузія: швидкості молекул легких ізотопів більші, ніж важких, тому при пропусканні через мембрану газу, що складається з суміші ізотопів, легкі ізотопи проходять швидше.
- Термодифузія: при існуванні градієнту температури у рідині чи газі атоми легких ізотопів частіше опиняються у більш теплих місцях, тому у цих зонах їх концентрація підвищується.
- Дистиляція: при переведенні речовини у стан рівноваги між рідиною і парою легкий ізотоп концентрується в парі.
- Газові центрифуги: при розкрученні газової суміші ізотопів у центрифузі легкі ізотопи концентруються біля осі.
- Ізотопний обмін: при контакті двох різних сполук розділюваного елементу, що перебувають у різних фазах, різні ізотопи концентруються в різних фракціях,
- Електроміграція іонів: при прикладенні електричного поля до розплаву або розчину іони різних ізотопів рухаються з різною швидкістю.
В найкращих з цих методів коефіцієнти розділення не перевищують відсотка, тому для ефективного збагачення потрібно повторювати процес сотні або тисячі разів.[8]
Використання ізотопів[ред. | ред. код]
Радіоізотопне датування[ред. | ред. код]
Оскільки різні ізотопи мають різний період напіврозпаду, то, знаючи вихідну концентрацію ізотопів у речовині, замірявши її пізніше, можна дізнатися вік зразка.
Найбільш відомим прикладом такого використання є радіовуглецевий метод: вуглець-14 (т. зв. радіовуглець) постійно утворюється в атмосфері під час реакції ядер азоту з космічними променями і розпадається з періодом напіврозпаду 5370 років. Ці протилежні процеси компенсують один одного, тому концентрація цього ізотопу в атмосфері є постійною, близько 1 атому 14С на 1012 атомів стабільного вуглецю. Допоки деякий організм живе, він постійно обмінюється вуглецем з навколишнім середовищем, тому та сама концентрація встановлюється і в ньому. Коли організм помирає і процеси обміну речовин у ньому припиняються, доля вуглецю-14 у ньому починає зменшуватися. Таким чином, вимірявши питому активність 14С в вуглецю, виділеному з залишків того чи іншого організму, можна доволі точно визначити, коли саме жив цей організм. Зручність цього методу полягає в тому, що вуглець входить до складу практично всіх організмів, тому такий метод є доволі універсальним. З іншого боку, через відносно короткий період напіврозпаду, радіовуглецевий метод може використовуватися лише для датування віку організмів, що не старіші за 60 000 років.
Для мінералів застосовують калій-аргоновий та уран-свинцевий методи, що дозволяють датувати більші часові інтервали.
Мічені атоми[ред. | ред. код]
Через хімічну нероздільність, радіоактивні ізотопи можуть використовуватися організмом (або брати участь у хімічних реакціях) так само, як і звичайні. Це дозволяє дуже точно спостерігати за шляхами метаболізму того чи іншого елементу (або речовини, деякі атоми якої замінені) у організмі. Ця методика є широко вживаною в біології, медицині і техніці.
Використання в кліматичних дослідженнях[ред. | ред. код]
Природний кисень представлений трьома стабільними ізотопами кисень-16, кисень-17 і кисень-18. Незважаючи на хімічну подібність, ізотопи трохи по різному беруть участь у таких процесах як випаровування і конденсація, тому концентрація кисню-18 у океані залежить від клімату планети (а саме від розміру льодовиків). Цей факт використовують для того, щоб дізнатися кліматичні умови в далекому минулому — досліджуючи льодяні керни з полярних льодовиків, або визначаючи концентрацію цих ізотопів у мушлях скам'янілостей. [9]
Ядерна енергетика і зброя[ред. | ред. код]
На відміну від урану-238, в урані-235 можлива самопідтримувана ланцюгова реакція. Це найбільш розповсюджений у природі ізотоп, що має такі властивості, через що саме він використовується при виробництві ядерної зброї, а також в атомних реакторах. При цьому його концентрація в природному урані становить лише 0,72%, тому дуже важливим є питання розділення ізотопів.
Ядерний магнітний резонанс[ред. | ред. код]
У медицині, на використанні явища ядерного магнітного резонансу побудовані кілька важливих діагностичних технік, таких як ЯМР-спектроскопія і магнітно-резонансна томографія. Проте, ядерний магнітний резонанс виникає за рахунок магнітних властивостей ядра, а тому такі методики працюють лише для ядер, що мають нецілий спін. Таким чином, лише ізотопи з непарним числом нуклонів можуть використовуватися для цього.[10]
Див. також[ред. | ред. код]
Примітки[ред. | ред. код]
- ↑ Elements and Atoms: Chapter 20 [Архівовано 23 грудня 2016 у Wayback Machine.](англ.)
- ↑ Mass spectra and isotopes [Архівовано 9 серпня 2017 у Wayback Machine.](англ.)
- ↑ All Nobel Prizes in Chemistry [Архівовано 5 грудня 2015 у Wayback Machine.](англ.)
- ↑ Штучна радіоактивність. Архів оригіналу за 18 грудня 2016. Процитовано 24 грудня 2016.
- ↑ National Nuclear Data Center. Архів оригіналу за 23 грудня 2016. Процитовано 25 грудня 2016.
- ↑ Chart of Nuclides [Архівовано 10 жовтня 2018 у Wayback Machine.](англ.)
- ↑ ИЗОТОПОВ РАЗДЕЛЕНИЕ [Архівовано 24 грудня 2016 у Wayback Machine.](рос.)
- ↑ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИЕ МЕТОДЫ [Архівовано 25 грудня 2016 у Wayback Machine.](рос.)
- ↑ Изотопы в климатологических исследованиях [Архівовано 6 червня 2015 у Wayback Machine.](рос.)
- ↑ FAQ: Ядерный магнитный резонанс [Архівовано 25 грудня 2016 у Wayback Machine.](рос.)
Джерела[ред. | ред. код]
- Деркач Ф. А. Хімія : посібник для вступ. до вузів / Ф. А. Деркач. — Л. : Видавництво Львівського університету, 1968. — 312 с.
- Глосарій термінів з хімії / уклад. Й. Опейда, О. Швайка ; Ін-т фізико-органічної хімії та вуглехімії ім. Л. М. Литвиненка НАН України, Донецький національний університет. — Дон. : Вебер, 2008. — 738 с. — ISBN 978-966-335-206-0.
Посилання[ред. | ред. код]
- Ізотопи [Архівовано 3 вересня 2017 у Wayback Machine.] //ЕСУ
- А. М. Бризицька. Ізотопи // Фармацевтична енциклопедія [Архівовано 3 жовтня 2016 у Wayback Machine.]
- М. Д. Корнієнко. Ізотопи // Українська радянська енциклопедія [Архівовано 18 жовтня 2016 у Wayback Machine.]
- М. Д. Корнієнко. Радіоактивні зотопи // Українська радянська енциклопедія [Архівовано 18 жовтня 2016 у Wayback Machine.]
- (англ.) Nuclides [Архівовано 16 липня 2015 у Wayback Machine.] — таблиця ізотопів.
- (рос.) Хімічна енциклопедія онлайн. [Архівовано 18 липня 2010 у Wayback Machine.]
