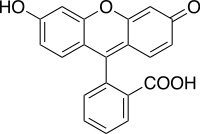
Флуоресцеїн
| Флуоресцеїн | |
|---|---|
| |

| |
| Інші назви | Fluorescein, resorcinolphthalein, C.I. 45350, solvent yellow 94, D & C yellow no. 7, angiofluor, Japan yellow 201, soap yellow |
| Ідентифікатори | |
| Номер CAS | 2321-07-5 |
| PubChem | 16850 |
| Номер EINECS | 219-031-8 |
| DrugBank | 00693 |
| KEGG | D01261 |
| Назва MeSH | Fluorescein |
| ChEBI | 31624 |
| Код ATC | S01JA01 |
| SMILES | c1ccc2c(c1)C(=O)OC23c4ccc(cc4Oc5c3ccc(c5)O)O |
| InChI | 1/C20H12O5/c21-11-5-7-15-17(9-11)24-18-10-12(22)6-8-16(18)20(15)14-4-2-1-3-13(14)19(23)25-20/h1-10,21-22H |
| Номер Бельштейна | 94324 |
| Номер Гмеліна | 248626 |
| Властивості | |
| Молекулярна формула | C20H12O5 |
| Молярна маса | 332,306 г/моль |
| Тпл | 314—316 °C |
| Розчинність (вода) | Помірна, висока в основному середовищі |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |

Флуоресцеїн (англ. Fluorescein) — хімічна сполука ряду фталеїнів, синтетичний барвник помаранчевого кольору, що демонструє жовто-зелену флуоресценцію у розчинах.
Гарно розчиняється в органічних розчинниках, таких як спирт. У воді у присутності основ утворює добре розчинну аніонну форму.
У флуоресцентній спектроскопії використовується як стандарт при вимірюванні квантових виходів флуоресценції.[1] Численні похідні флуоресцеїну застосовуються в біохімії та клітинній біології як флуоресцентні мітки.
Максимум спектру абсорбції — 494 нм, а емісії — 521 нм (у воді). Коефіцієнт екстинкції 92300 M−1см−1 (500 нм, основний етанол). Часто використовують похідні: ізотіоціанати (FITC) та 5(6)-карбоксифлуоресцеїн.
Колір водного розчину — жовтий «на просвіт» або зелений «збоку».
Фізичні властивості[ред. | ред. код]
Барвник має яскраву флуоресценцію (поглинання 494 нм / емісія 521 нм):
Квантовий вихід — 50—70 %. Час життя збудженого стану варіює між 3 нс (pH < 5) i 4 нс (pH > 9).
Флуоресцеїн має ізобестичну точку (однакове поглинання за різних значень pH) на 460 нм.
Отримання[ред. | ред. код]
Вперше синтезовано Адольфом фон Баєром в 1871 році. Легко отримується сплавленням фталевого ангідриду з 1,3-дигідроксибензолом (резорцином) в присутності хлориду цинку:
Застосування CH3SO3H як каталізатора дає дещо кращі виходи й м'якші умови реакції.[2][3]
Механізм[ред. | ред. код]
Перший етап утворення барвнику — реакція Фріделя-Крафтса. При цьому кислотний каталізатор відщеплює протон, який приєднується до фталевого ангідриду, утворюючи карбокатіон — електрофіл, який заміщує гідроген в молекулі резорцину, повертаючи каталізатор. В молекулі збереглася карбонільна група, яка може знову бути протонована з утворенням карбокаіону.
Далі все проходить як спочатку, а протон потім приєднується до OH-групи залишку резорцину, каталізуючи його етерифікацію з іншим залишком резорцину. Утворюється столука, яка біля центрального атома містить гідроксильну групу. Остання вступає у реакцію внутрішньомолелулярної естерифікації з утворенням лактону, який, завдяки таутомерії, частково перетворюється на забарвлену форму з хіноїдною будовою[4]:
Похідні[ред. | ред. код]

Для мічення протеїнів використовують флуоресцеїн ізотіоціанат та активовані естери карбоксифлуорисцеїну. Багато інших барвників містять скелет флуоресцеїну і додаткові замісники (скажімо сульфогрупи), що підвищують розчинність та фотостабільність. Похідними флуоресцеїну є також барвники типу еозину.
Застосування[ред. | ред. код]
Спостереження за потоками води[ред. | ред. код]
Одним з перших застосувань флуоресцеїну (у XIX ст.) було фарбування води в річках для відстеження напрямку потоку. Зараз подекуди застосовують для відстежень витоків трубопроводів.
Біологія[ред. | ред. код]
У клітинній біології флуоресцеїн та його похідні — незамінний інструмент для флуоресцентної мікроскопії. Перевагою флуоресцеїну є те, що він ідеально підходить для збудження відносно доступним аргоновим лазером (488 нм). Недоліком барвників на основі флуоресцеїну є низька фотостабільність.
Див. також[ред. | ред. код]
- Похідні:
- Еозин
- Carboxyfluorescein[en]
- Fluorescein isothiocyanate[en] (FITC)
- Fluorescein amidite[en] (FAM)
- Еритрозин
- Rose Bengal[en]
- DyLight Fluor[en] — комерційні флуорофори на основі фулоресцеїну
- Pseudomonas aeruginosa, бактерія, яка виділяє фулоресцеїн
- Fluorescein diacetate hydrolysis[en], a biochemistry laboratory test
Примітки[ред. | ред. код]
- ↑ Albert M. Brouwer. Standards for photoluminescence quantum yield measurements in solution (IUPAC Technical Report) // Pure and Applied Chemistry. — 2011. — Т. 83, вип. 12 (28 квітня). — С. 2213–2228. — DOI:.
- ↑ Sun, W. C.; Gee, K. R.; Klaubert, D. H.; Haugland, R. P., Synthesis of Fluorinated Fluoresceins. Journal of Organic Chemistry 1997, 62, (19), 6469-6475.
- ↑ Yuichiro Ueno; Jiao, G.-S.; Burgess, K., Preparation of 5- and 6-Carboxyfluorescein. Practical Synthetic Procedures 2004, 31, (15), 2591—2593.
- ↑ Microsoft Word - M52LC_Experiment_1S12.doc (PDF).
Посилання[ред. | ред. код]
- Absorption and Emission Spectra of Fluorescein in Ethanol і Basic Ethanol на OGI School of Science and Engineering
- Fluorescein Ionization Equilibria на Invitrogen
- MSDS at Oxford University
- Absorption spectra and fluorescence emission spectra
| Це незавершена стаття про органічну сполуку. Ви можете допомогти проєкту, виправивши або дописавши її. |


