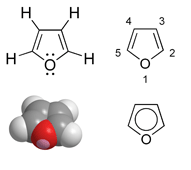
Фуран
| Фуран | |
|---|---|
| |
| Назва за IUPAC | Furan |
| Інші назви | Oxole, furfuran, divinyl oxide |
| Ідентифікатори | |
| Номер CAS | 110-00-9 |
| Номер EINECS | 203-727-3 |
| KEGG | C14275 |
| ChEBI | 35559 |
| SMILES | C1=CC=CO1 |
| InChI | InChI=1S/C4H4O/c1-2-4-5-3-1/h1-4H |
| Номер Бельштейна | 103221 |
| Номер Гмеліна | 25716 |
| Властивості | |
| Молекулярна формула | C4H4O |
| Молярна маса | 68,07 г/моль |
| Зовнішній вигляд | colorless, volatile liquid |
| Густина | 0,936 г/мл |
| Тпл | -85,6 °C |
| Ткип | 31,4 °C |
| Небезпеки | |
| ГГС піктограми | 
|
| ГГС формулювання небезпек | H224, H302, H315, H332, H341, H350, H373 |
| ГГС запобіжних заходів | P201, P202, P210, P233, P240, P241, P242, P243
,P260, P261, P264, P270, P271, P273, P280, P281 ,P301+P312, P302+P352, P303+P361+P353, P304+P312, P304+P340, P308+P313, P312, P314 ,P321, P330, P332+P313, P362, P370+P378, P403+P235, P405, P501 |
| NFPA 704 | |
| Температура спалаху | -35 °C |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Фура́н — гетероциклічна органічна сполука. Добувається, зазвичай, шляхом термічного розкладання пентозних матеріалів, наприклад целюлозних субстратів (деревина сосни). Фуран — це безбарвна легкозаймиста, досить нестабільна рідина з температурою кипіння близької до кімнатної. Є токсичною і може бути канцерогенною. Каталітичним гідруванням фурану на паладієвих каталізаторах добувають тетрагідрофуран.
Фуран вважається ароматичним тому, що одна з пар електронів на атомі кисню делокалізована в кільце, створюючи 4n+2 ароматичну систему (за правилом Гюккеля), аналогічно бензену. Через ароматичність молекула є плоскою з делокалізованими «ароматичними» зв‘язками. Друга пара електронів атому оксигену знаходиться в площині молекулярної системи. Суть sp2 гібридизації полягає в тому, щоб одна вільна пара оксигену належала π-орбіталі, і саме так, щоб вона могла взаємодіяти рамках π-системи.
Назва фурану походить від лат. furfur, що означає висівки.[1] Перша похідна фурану, яка була описана — 2-фуранова кислота, Карлом Вільгельмом Шеєле в 1780 році. Інша важлива похідна, фурфураль, представлена Йоганном Вольфгангом Деберайнером в 1831 і охарактеризована лише дев‘ять років по тому Джоном Стенхаусом. Сам фуран вперше був синтезований Генрихом Лімпріхтом в 1870 році, хоча той і назвав його "тетрафенолом”.[2][3]
Отримання[ред. | ред. код]
В промисловості фуран отримують декарбонілюванням фурфуролу, чи окисленням бутадієну в присутності мідного каталізатора:[4]
Також фуран отримують декарбоксилюванням 2-фуранкарбонової кислоти[5]:
Хімічні властивості[ред. | ред. код]
Завдяки своїй ароматичності, поведінка фурану досить різноманітна, на відміну від більшості типових гетероциклічних етерів, наприклад тетрагідрофурану.
Електрофільне заміщення[ред. | ред. код]
Фуран більш реакційноздатний ніж бензен та тіофен в реакціях електрофільного заміщення, це пов'язано з електронно-донорним впливом гетероароматичного оксигену. Вивчення резонансних структур показує збільшення електронної густини в кільці, що призводить до зростання ймовірності електрофільного заміщення.
Разом з тим практично здійснити електрофільне заміщення в ядрі фурану дуже важко, оскільки він легко полімеризується (осмолюється) в присутності кислот. Так для нітрування фурану застосовують такі нетривіальні реагенти як тетранітрометан. Похідні, що містять акцепторні замісники (особливо у положенні 2) набагато стійкіші у кислому середовищі, зокрема фурфурол (2-форміл-фуран) може бути пробромований напряму.
Реакції приєднання[ред. | ред. код]
Фуран виступає дієном в реакції Дільса—Альдера з електронно-акцепторними дієнофілами, такими як етиловий ефір-(2E)-3-нітроакрилату.[6] Продуктом реакції є суміш ізомерів з переважанням ендо-ізомеру:
Також фуран може приєднувати і молекули які не є типовими дієнофілами, наприклад молекулу брому
У присутності нікелю приєднує водень з утворенням тетрагідрофурану[5].
Реакції окиснення[ред. | ред. код]
При окисненні фурану утворюється малеїновий ангідрид. Окиснення проводиться в нейтральному або слаболужному середовищі. В якості окисника використовується дихромат калію або оксид хрому(VI):
Спектральні властивості та будова молекули[ред. | ред. код]
В ЯМР спектрах фурану сигнали протонів спостерігаються в регіоні типовому для ароматичних сполук що може бути додатковим підтвердженням ароматичності молекули.

| ЯМР 1H (DMSO-d6), ppm | ЯМР 13C (DMSO-d6), ppm [7] |
|---|---|
| H2/5 7.46 | C2/5 143.6 |
| H3/4 6.36 | C3/4 110.4 |
Примітки[ред. | ред. код]
- ↑ Alexander Senning. Elsevier's Dictionary of Chemoetymology. Elsevier, 2006. ISBN 0444522395.
- ↑ H. Limpricht (1870). Ueber das Tetraphenol C4H4O. Berichte der deutschen chemischen Gesellschaft. 3 (1): 90—91. doi:10.1002/cber.18700030129.
- ↑ Ernest Harry Rodd. Chemistry of Carbon Compounds: A Modern Comprehensive Treatise. Elsevier, 1971.
- ↑ Hoydonckx, H. E.; Van Rhijn, W. M.; Van Rhijn, W.; De Vos, D. E.; Jacobs, P. A. (2005). Furfural and Derivatives. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a12_119.pub2.
- ↑ а б Ластухін, Воронов (2006). Органічна хімія. с. 776-779. ISBN 966-7022-19-6.
- ↑ Masesane I, Batsanov A, Howard J, Modal R, Steel P (2006). The oxanorbornene approach to 3-hydroxy, 3,4-dihydroxy and 3,4,5-trihydroxy derivatives of 2-aminocyclohexanecarboxylic acid. Beilstein Journal of Organic Chemistry. 2 (9). doi:10.1186/1860-5397-2-9.
{{cite journal}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ Theophil Eicher, Siegfried Hauptmann (2003). The Chemistry of Heterocycles. ISBN 3-527-30720-6.
Посилання[ред. | ред. код]
| Це незавершена стаття про органічну сполуку. Ви можете допомогти проєкту, виправивши або дописавши її. |








