Хітозан
| Хітозан | |
|---|---|
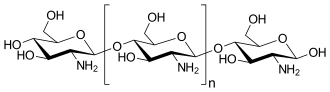 Структура повністю деацетильованого хітозану
| |
| Інші назви | Деацетилхітин, Полі-D-глюкозамін |
| Ідентифікатори | |
| Номер CAS | 9012-76-4 |
| Номер EINECS | 618-480-0 |
| KEGG | C00734 |
| Назва MeSH | D05.750.078.139.500 і D09.698.211.500 |
| ChEBI | 16261 |
| SMILES | COC(=O)N[C@@H]1[C@H]([C@@H]([C@H](O[C@H]1O[C@@H]2[C@H](O[C@H]([C@@H]([C@H]2O)N)O[C@@H]3[C@H](O[C@H]([C@@H]([C@H]3O)N)O)CO)CO)CO)O[C@H]4[C@@H]([C@H]([C@@H]([C@H](O4)CO)O[C@H]5[C@@H]([C@H]([C@@H]([C@H](O5)CO)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O[C@H]7[C@@H]([C@H]([C@@H]([C@H](O7)CO)O[C@H]8[C@@H]([C@H]([C@@H]([C@H](O8)CO)O[C@H]9[C@@H]([C@H]([C@@H]([C@H](O9)CO)O)O)N)O)N)O)N)O)N)O)N)O)N)O |
| InChI | InChI=1S/C56H103N9O39/c1-87-56(86)65-28-38(84)46(19(10-74)96-55(28)104-45-18(9-73)95-49(27(64)37(45)83)97-39-12(3-67)88-47(85)20(57)31(39)77)103-54-26(63)36(82)44(17(8-72)94-54)102-53-25(62)35(81)43(16(7-71)93-53)101-52-24(61)34(80)42(15(6-70)92-52)100-51-23(60)33(79)41(14(5-69)91-51)99-50-22(59)32(78)40(13(4-68)90-50)98-48-21(58)30(76)29(75)11(2-66)89-48/h11-55,66-85H,2-10,57-64H2,1H3,(H,65,86)/t11-,12-,13-,14-,15-,16-,17-,18-,19-,20-,21-,22-,23-,24-,25-,26-,27-,28-,29-,30-,31-,32-,33-,34-,35-,36-,37-,38-,39-,40-,41-,42-,43-,44-,45-,46-,47-,48+,49+,50+,51+,52+,53+,54+,55+/m1/s1 |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Хітозан — молекула хітину без ацетильних груп; амінополісахарид 2-аміно-2-дезокси-b-D-глюкан, що утворюється при дезацетилюванні хітину.
Як і хітин, хітозан являє собою аморфно-кристалічний полімер, для якого також характерне явище поліморфізму, причому кількість структурних модифікацій при переході від хітину до хітозану збільшується до 6.[1]
На відміну від хітину, одержуваний при його дезацетилюванні хітозан розчиняється навіть у розбавлених органічних кислотах, наприклад у водному розчині оцтової кислоти. При цьому для розчинів хітозану, як і інших полімерів, характерна істотна залежність в'язкості від концентрації (при збільшенні концентрації розчину хітозану в 1-2%-ном розчині оцтової кислоти з 2 до 4% в'язкість розчину збільшується приблизно в 30 разів).[1]
Виробництво хітозану
Виробництво хітозану здійснюється шляхом деацетилювання хітину концентрованим розчином гідроксиду натрію за високих температур. Хітин є структурним елементом екзоскелету ракоподібних (наприклад, крабів та креветок) та клітинних стін грибів. Ступінь деацетилювання (СД) визначають за допомогою ЯМР-спектроскопії, ІЧ-спектроскопії, кислотно-основного титрування. У комерційних хітозанах СД коливається від 60 до 100%. В середньому, молекулярна маса комерційно хітозану становить від 3800 до 20 000 далтонів. Аміногрупа в хітозані має значення pKa ~ 6,5, та, на відміну від хітину, розчиняється у розбавлених розчинах хлористоводневої та різноманітних органічних кислот, наприклад, у розчині оцтової кислоти. При цьому для розчинів хітозану, як і інших полімерів, характерна істотна залежність в'язкості від концентрації (при збільшенні концентрації розчину хітозану в 1-2%-ном розчині оцтової кислоти з 2 до 4% в'язкість розчину збільшується приблизно в 30 разів)[1]. Це робить хітозан водорозчинним і біоадгезивним, який легко зв'язується з негативно зарядженими поверхнями[2][3]. Хітозан покращує транспортування полярних лікарських засобів через епітеліальні поверхні, є біосумісним і біологічно розкладається.
Хімічні властивості. Застосування хітозану
За хімічними властивостями не відрізняється від хітину, але має одну перевагу — на аміногрупах, не обтяжених ацетильними групами, накопичується надлишковий позитивний заряд. Завдяки йому, за даними біохіміків, до зламаної кістки збігаються макрофаги крові і пришвидшується процес дозрівання нових клітин кісткової тканини, що призводить до пришвидшеного загоєння пошкоджених кісток.[4] Частковий позитивний заряд аміногруп в молекулах хітозана, допомагає кровотворенню і перешкоджає рубцюванню ран, затримуючи вироблення фібрину.[4] З допомогою хітинових пов'язок добре лікуються складні і важкі рани. Нанесеним на шкіру і волосся, хітозан, завдяки позитивному заряду, утворює тонку плівку, внаслідок чого креми на хітозановій основі знайшли застосування в косметиці.
У медицині для лікування і профілактики тромбозів використовується природний антикоагулянт крові — гепарин, за хімічною будовою є змішаним полісахаридом. Найбільш близький його структурний аналог — сульфат хітозану також володіє антикоагулянтною активністю, зростаючою при збільшенні ступеня сульфатування.[1] Можливість реалізації синергічного ефекту (посилення активності гепарину при введенні добавок сульфату хітозану) робить це з'єднання перспективним для створення лікарських препаратів антикоагулянтної і антисклеротичної дії.[джерело?]
N-і О-сульфатовані похідні частково дезацетильованого карбоксиметилхітина не тільки перешкоджають згортанню крові завдяки селективній адсорбції антитромбіну, а й різко зменшують інтенсивність поділу ракових клітин.[1]
Ще однією можливістю використання хітину, хітозану та їх похідних (карбоксиметилхітина, карбоксиметилхітозану, сукцинілхітозану) — створення біодеградабельних носіїв фармацевтичних препаратів (антибіотиків, антивірусних, протипухлинних та антиалергенних препаратів) у вигляді плівок (мембран). Застосування таких плівок створює умови для виділення лікарських засобів, забезпечуючи ефект пролонгування їх дії.
Хітозан ефективно зв'язує феноли (точніше хінони — продукт їх з'єднання з киснем в присутності ферменту тирозинази).[4]
Полімерні комплексоутворювачі, в тому числі хітин, хітозан та їх похідні, наприклад карбоксиметиловіе ефіри, можуть розглядатися як реальна альтернатива традиційним методам очищення стічних вод промислових підприємств від сполук металів, використовуваних для нанесення захисних покриттів (нікель, хром, цинк), а також від таких металів, як ртуть і кадмій, здатних акумулюватися живими організмами. Наявність електронодонорних аміно- і гідроксильних груп, широкі можливості введення різних іоногенних груп кислотного і основного характеру роблять похідні хітину і хитозану вельми перспективними для використання в хроматографії при поділі і очищенню біологічно активних сполук (нуклеїнових кислот і продуктів їх гідролізу, стероїдів, амінокислот).
Вельми перспективне використання хітозану в паперовій промисловості: завдяки більшій міцності при водних обробках іонних зв'язків, що утворюються при нанесенні хітозану на целюлозне волокно при формуванні паперу, в порівнянні з існуючими в звичайному папері водневими зв'язками помітно зростає міцність паперового листа, особливо в мокрому стані. При цьому одночасно поліпшуються і інші важливі властивості (опір продавлюванню, зламу, стабільність зображення).
Примітки
- ↑ а б в г д Гальбрайх Л.С. Хитин и хитозан: строение, свойства, применение // Соровский образовательный журнал. 2001
- ↑ Lee, Dong Woog; Lim, Chanoong; Israelachvili, Jacob N.; Hwang, Dong Soo (19 листопада 2013). Strong Adhesion and Cohesion of Chitosan in Aqueous Solutions. Langmuir. Т. 29, № 46. с. 14222—14229. doi:10.1021/la403124u. ISSN 0743-7463. Процитовано 24 березня 2018.
- ↑ Lim, Chanoong; Lee, Dong Woog; Israelachvili, Jacob N.; Jho, YongSeok; Hwang, Dong Soo. Contact time- and pH-dependent adhesion and cohesion of low molecular weight chitosan coated surfaces. Carbohydrate Polymers. Т. 117. с. 887—894. doi:10.1016/j.carbpol.2014.10.033. Процитовано 24 березня 2018.
- ↑ а б в Фома Аксенов «Экспансия хитина» / «Техника — молодежи», 1995, №1. ISBN 0320-33IX