Гексанітрогексаазаізовюрцитан
| Гексанітрогексаазаізовюрцитан | |
|---|---|

| |
| Систематична назва | (2,4,6,8,10,12-гексанітрогексаазатетрацікло[5.5.0.03,11.05,9]Додекан |
| Інші назви | ГНІВ, HNIW, CL-20 |
| Ідентифікатори | |
| Номер CAS | 135285-90-4 |
| Номер EINECS | 603-913-8 |
| ChEBI | 77327 |
| SMILES | C12C3N(C4C(N3[N+](=O)[O-])N(C(N1[N+](=O)[O-])C(N2[N+](=O)[O-])N4[N+](=O)[O-])[N+](=O)[O-])[N+](=O)[O-][1] |
| InChI | InChI=1S/C6H6N12O12/c19-13(20)7-1-2-8(14(21)22)5(7)6-9(15(23)24)3(11(1)17(27)28)4(10(6)16(25)26)12(2)18(29)30/h1-6H |
| Номер Бельштейна | 4834707 |
| Властивості | |
| Молекулярна формула | C6N12H6O12 |
| Молярна маса | 438,186 г/моль |
| Зовнішній вигляд | безбарвна речовина |
| Густина | 2,044 г/см3 |
| Небезпеки | |
| Класифікація ЄС | Токсичний (T) Канцероген категорії 3 Небезпечний для довкілля (N) Легкозаймистий(F) |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Гексанітрогексаазаізовюрцитан (ГНІВ, HNIW, CL-20) — поліциклічний нітрамін, потужна вибухова речовина.
Хоча CL-20 в основному розроблявся в корпорації Thiokol, ВМС США також були зацікавлені у CL-20 для використання як ракетного палива, наприклад, для ракет, оскільки він має більш низькі характеристики помітності, такі, як менш помітний дим.[2]
Гексанітрогексаазаізовюрцитан був отриманий в 1987 році в США в Naval Air Wifave Center[3] і проявив себе як потужна вибухова речовина. Корпорація Thiokol (США) в 1990 році розробила пілотну установку з отримання гексанітрогексаазаізовюрцитана, що видавала до 200 кг продукту за 1 завантаження.
Гексанітрогексаазаізовюритан являє собою безбарвну кристалічну речовину. Розчиняється у холодній воді, малорозчинний в етанолі, але добре розчиняється в ацетоні (94,6 г/100 г при 25 ° С), ацетонітрилі, етилацетаті (45,0 г/100 г при 25 ° С), крижаній оцтовій кислоті. Порівняно хімічно стійкий, однак легко розкладається гідроксидами, амідами та ціанідами лужних металів.
Гексанітрогексаазаізовюрцитан за нормальних умов складається з чотирьох стійких поліморфних модифікацій, які називаються α-, β-, γ-, δ-і ε-формами. Вони різняються між собою просторовою орієнтацією нітрогруп, типом кристалічної ґратки та числом молекул у кристалічній решітці. Ці форми здатні переходити один в одного: β-форма (орторомбічна кристалічна комірки) переходить в γ-форму (моноклінна кристалічна комірка) при 185 ° C, яка при нагріванні до 230 ° C змінює свою кристалічну структуру. α-Форму одержують осадженням гексанітрогексаазаізовюрцитана хлороформом з сульфоланових розчинів. δ-Форма є лабільною та існує лише в умовах високого тиску. Найбільш щільною структурою та найвищою термічною стійкістю є ε-форма.
Синтез гексанітрогексаазаізовюрцитану є багатостадійним процесом. На перших стадіях синтезу отримують каркас молекули конденсацією гліоксалю з похідними бензиламінів за такою схемою:
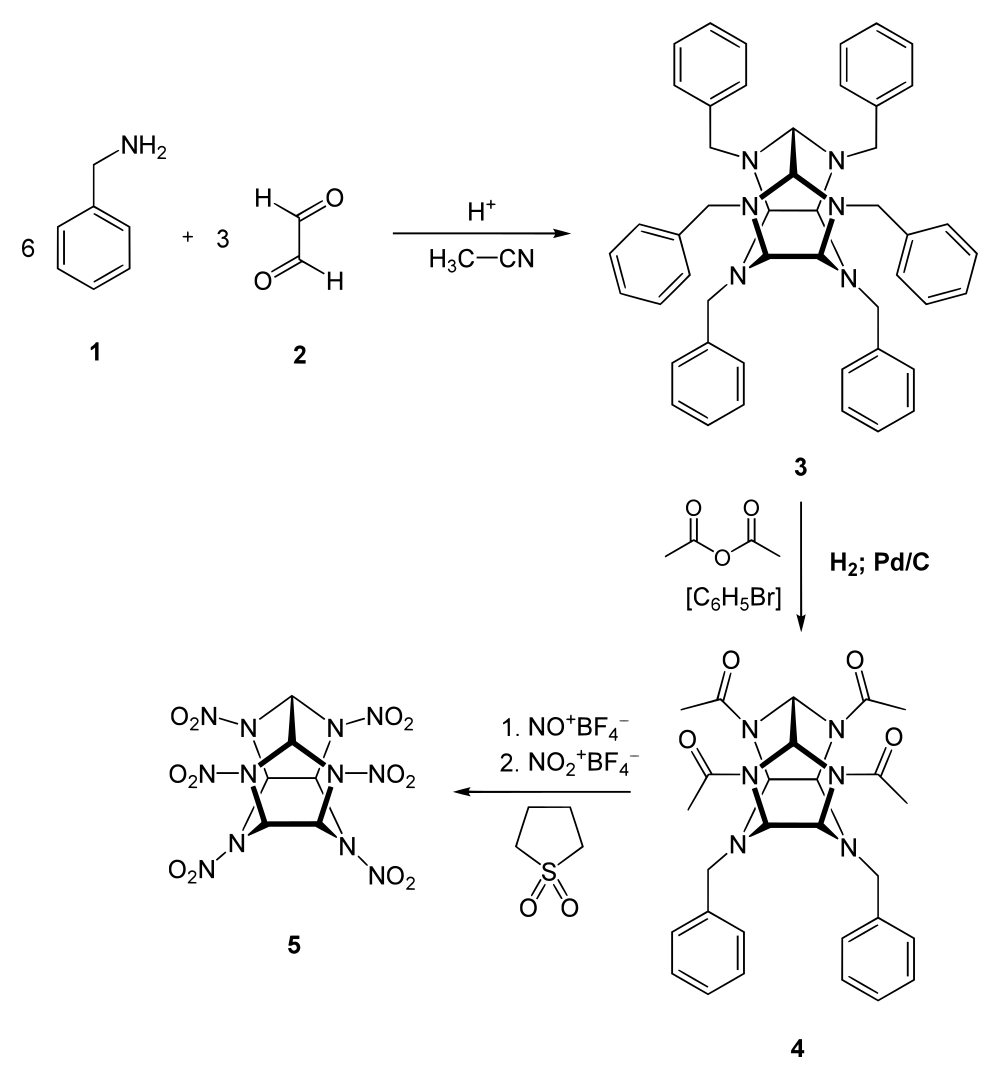
На такій стадії отримана речовина піддається нітролізу. Як Нітра-сполуки використовуються тетрафторборат нітронія в розчині сульфолану, тетраоксид нітрогену N2O4, суміш сірчаної та азотної кислот, суміш нітрогенної кислоти та нітрату амонію. Реакція нітролізу протікає за складним механізмом. При цьому, крім цільового продукту, утворюється багато проміжних нітропохідних гексанітрогексаазаізовюрцитана. Високий вихід цільового продукту досягається при витримці реакційної суміші протягом 7-14 годин при температурі 115—120 ° C.
Найщільнішу ε-форму гексанітрогексаазаізовюрцитана отримують осадковою або випарювальною кристалізацією. При осадковій кристалізації до розчинів гексанітрогексаазаізовюрцитану в етилацетаті або ацетоні додають аліфатичні або ароматичні вуглеводні, в яких розчинність сполуки невелика. При випарювальній кристалізації використовують суміш летючого розчинника, в якому гексанітрогексаазаізовюрцитан розчиняється добре (ацетон, етилацетат, ізопропілацетат, метилацетат, тетрагідрофуран, ацетонітрил, метилетилкетон) і менш летючого розчинника, в якому гексанітрогексаазаізовюрцитан розчинний погано (толуол, 1,2-дихлоретан, ксилол). Відгонка летючого розчинника призводить до поступового випадання ε-форми, при цьому варіюванням умови кристалізації можна досягти частинок ε-форми різного розміру та постійного гранулометричного складу.
Гексанітрогексаазаізовюрцитан — одна з найефективніших вибухових речовин на 2014 рік, він ефективніший, ніж октоген: його швидкість детонації та густина вище (9660 м/с і 2,044 г/см3 проти 9100 м/с і 1,84 г/см3 відповідно).
Гексанітрогексаазаізовюрцитан може використовуватися як потужна вибухова речовина, однак його застосування перешкоджає висока ціна в 1300 доларів за кілограм внаслідок невеликих обсягів виробництва, а також низька стійкість до удару. У сумішей гексанітрогексаазаізовюрцитана з пластифікаторами одночасно з підвищенням стійкості знижується ефективність.
Суміш гексанітрогексаазаізовюрцитану та октогену у співвідношенні 2:1, запропонована американським професором Адамом Матцгером (англ. Adam Matzger) має високу стабільність, велику щільність та високу швидкість детонації (9480 м/с).
Продовжують вестися дослідження на предмет застосування CL-20 як основного компонента ТПРД[2], істотними перевагами виступають малопомітність траси та висока енергогустина, істотним (на сьогодні) недоліком — відсутність промислових масштабів виробництва і, як наслідок, висока вартість сполуки.
- ↑ HNIW
- ↑ а б Yirka, Bob (9 вересня 2011). University chemists devise means to stabilize explosive CL-20. Physorg.com. Архів оригіналу за 25 січня 2021. Процитовано 8 липня 2012.
- ↑ С. В. Сысолятин, А. А. Лобанова, Ю. Т. Черникова, Г. В. Сакович (2005). Методы синтеза и свойства гексанитрогексаазаизовюрцитана. Успехи химии. 74 (8): 830—838.
- Гексанитрогексаазаизовюрцитан, HNIW, CL-20 (рос.). Exploder. Архів оригіналу за 3 жовтня 2016. Процитовано 14 вересня 2013.
- Разработано мощнейшее взрывчатое вещество в истории человечества (рос.). km.ru. 1 жовтня 2012. Архів оригіналу за 6 листопада 2012. Процитовано 14 вересня 2013.
- Убийца номер один: взрывной кристалл (рос.). Популярная механика. 24 вересня 2012. Архів оригіналу за 16 серпня 2013. Процитовано 14 вересня 2013.
- С. В. Сысолятин, А. А. Лобанова, Ю. Т. Черникова, Г. В. Сакович (2005). Методы синтеза и свойства гексанитрогексаазаизовюрцитана. Успехи химии. 74 (8): 830—838.