Потенціал дії


Потенціал дії (ПД), також спайк (від англ. spike, гострий пік на графіку), нервовий імпульс (для нейронних потенціалів дії) — короткочасні амплітудні зміни мембранного потенціалу спокою (МПС), що виникають зі збудженням живої клітини. По суті це електричний розряд — швидка короткочасна зміна потенціалу на невеликій ділянці мембрани збудливої клітини (нейрона або м'язового волокна), в підсумку якого зовнішня поверхня цієї ділянки, стає негативно зарядженою стосовно сусідніх ділянок мембрани, тоді як його внутрішня поверхня стає позитивно зарядженою щодо сусідніх ділянок мембрани. Потенціал дії є фізичною основою нервового або м'язового імпульсу, який відіграє сигнальну (регуляторну) роль.
Загальна характеристика[ред. | ред. код]
Потенціалами дії називають швидку, відносно короткотривалу та високоамплітудну, зміну мембранного потенціалу в клітинах живих організмів. Потенціали дії можуть відрізнятися за своїми параметрами залежно від типу клітини і навіть на різних ділянках мембрани тієї самої клітини. Найчастіше говорять про потенціали дії збудливих тканин тварин — нервових та м'язових, проте до їх генерації здатні й інші клітини, як тваринні, так і клітини грибів та рослин, і навіть клітини протистів. В основі будь-якого потенціалу дії лежать такі явища:
- 'Мембрана живої клітини поляризована' — її внутрішня поверхня заряджена негативно щодо зовнішньої, завдяки тому, що в розчині біля її зовнішньої поверхні перебуває більша кількість позитивно заряджених частинок (катіонів), а біля внутрішньої поверхні — більша кількість негативно заряджених часток (аніонів).
- 'Мембрана має вибіркову проникність' — її проникність для різних частинок (атомів або молекул) залежить від їхніх розмірів, електричного заряду і хімічних властивостей.
- 'Мембрана збудливої клітини здатна швидко змінювати свою проникність' для певного виду катіонів, викликаючи перехід позитивного заряду з зовнішнього боку на внутрішній.
Основною математичною моделлю, що описує вироблення та передавання потенціалу дії в нервових та м'язових клітинах тварин, є модель Ходжкіна-Хакслі.
Фази[ред. | ред. код]
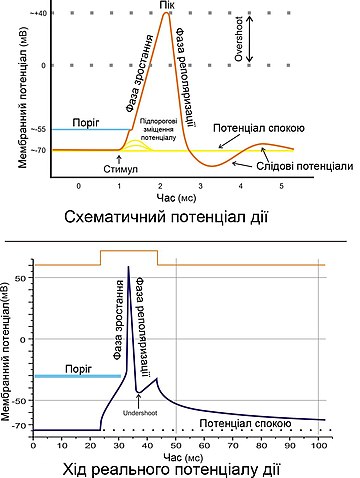
Можна чітко вирізнити п'ять фаз розвитку потенціалу дії (ПД)[1][2]:
Наростання (деполяризація)[ред. | ред. код]
Виникнення ПД пов'язане зі збільшенням проникності мембрани для іонів натрію (у 20-еро порівняно із проникністю для К+, і в 500 разів порівняно з вихідною проникністю Na+), і наступним посиленням дифузії цих іонів по концентраційному градієнту всередину клітини, що приводить до зміни (зменшення) мембранного потенціалу. Зменшення мембранного потенціалу забезпечує збільшення проникності мембрани для натрію, шляхом відкриття потенціал-залежних натрієвих каналів, а збільшення проникності супроводжується посиленням дифузії натрію в цитоплазму, що викликає ще більш значну деполяризацію мембрани. Завдяки наявності позитивного зворотного зв'язку, деполяризація мембрани під час збудження відбувається із прискоренням, і потік іонів натрію в клітину увесь час зростає.
Інтенсивність потоку іонів калію, спрямованого із клітини назовні, у перші моменти після виникнення збудження залишається такою самою, як в стані спокою. Посилений потік позитивно заряджених іонів натрію усередину клітини викликає спочатку зникнення надлишкового негативного заряду на внутрішній поверхні мембрани, а згодом призводить до перезарядження мембрани.
Надходження іонів натрію відбувається доти, поки внутрішня поверхня мембрани не набуде позитивного заряду, достатнього для урівноваження градієнта концентрації натрію і припинення його подальшого переходу усередину клітини.
Натрієвий механізм виникнення ПД підтверджують досліди зі зміною зовнішньої і внутрішньої концентрації цього іону. Було показано, що десятикратній зміні концентрації іонів натрію у зовнішньому або внутрішньому середовищі клітини, відповідає зміна ПД на 58 мВ[3]. У разі повного видалення іонів натрію з оточуючої клітину рідини, ПД не виникав.
Отож, встановлено, що ПД виникає в результаті надлишкової, порівняно зі спокоєм, дифузії іонів натрію з навколишньої рідини усередину клітини. Період, протягом якого проникність мембрани для іонів натрію з відкриттям натрієвих каналів зростає, є невеликим (0,5-1 мс); одразу за цим спостерігається підвищення проникності мембрани для іонів калію завдяки відкриттю потенціал-залежних калієвих каналів, й, отже, посилення дифузії цих іонів із клітини назовні.
- Принцип «все або нічого»
Потенціал дії виникає лише у тому разі, коли деполяризація перевищує деякий, свій для кожної клітини, граничний рівень. Це явище отримало назву «все, або нічого». Відповідно до закону «все-або-нічого» мембрана клітини збудливої тканини або не відповідає на подразник зовсім, або відповідає з якнайбільш можливою для неї на дану мить силою. Дія подразника зазвичай, призводить до локальної деполяризації мембрани, що викликає відкриття натрієвих каналів.
Однак, якщо деполяризація становить 50-75 % від граничної величини, то в клітині може виникнути локальна відповідь, амплітуда якої є значно нижчою за амплітуду потенціалу дії. Відсутність потенціалу дії на підграничному рівні деполяризації пояснюється тим, що у цьому разі недостатньо збільшується натрієва проникність, щоб викликати регенеративну деполяризацію. Рівень деполяризації, який виникає при цьому, не викликає відкриття нових натрієвих каналів, тож натрієва провідність швидко зменшується, і в клітині знову встановлюється потенціал спокою.[4]
Овершут[ред. | ред. код]
Деполяризація мембрани призводить до реверсії мембранного потенціалу (МП стає позитивним). У фазу овершута Na+-струм починає стрімко знижуватися, що пов'язано з інактивацією потенціал-залежних Na+-каналів (час відкритого стану — долі мілісекунди) і зникненням електрохімічного градієнта Na+.[5]
- Рефрактерність
- Одним з наслідків зникнення градієнта Na+ є рефрактерність мембрани — тимчасова нездатність відповідати на подразник. Якщо подразник виникає одразу після проходження потенціалу дії, то збудливість не виникне ані при силі подразника на рівні порогу, ані при значно сильнішому подразнику. Такий стан повної незбудливості називається абсолютним рефрактерним періодом. За ним іде відносний рефрактерний період, коли надпороговий подразник може викликати потенціал дії із значно меншою амплітудою ніж в нормі. Потенціал дії звичної амплітуди при дії порогового подразника, можна викликати лише після кількох мілісекунд після попереднього потенціалу дії. Абсолютний рефрактерний період обмежує максимальну частоту генерування потенціалів дії.[2]
Реполяризація[ред. | ред. код]
Збільшення потоку іонів калію, спрямованого із клітини назовні, призводить до зменшення мембранного потенціалу, що, своєю чергою, обумовлює зменшення проникності мембрани для іонів натрію.
Отож, другий етап відзначається тим, що потік іонів калію із клітини назовні зростає, а зустрічний потік іонів натрію зменшується. Така реполяризація мембрани триває, доки не відбудеться відновлення потенціалу спокою — реполяризація мембрани. Після цього проникність для іонів калію також спадає до вихідної величини. Зовнішня поверхня мембрани завдяки позитивно зарядженим іонам калію, що вийшли в середовище, знову набуває позитивного потенціалу відносно внутрішнього.
Слідові деполяризація і гіперполяризація[ред. | ред. код]
У кінцевій фазі відбувається уповільнення відновлення мембранного потенціалу спокою, і водночас реєструються слідові реакції у вигляді деполяризації та гіперполяризації, обумовлені повільним відновленням вихідної проникності для іонів К+.
Розповсюдження[1][ред. | ред. код]
Розповсюдження в немієлінізованому волокні[ред. | ред. код]
У немієлінізованому (безм'якотному) нервовому волокні ПД поширюється, охоплюючи послідовно всі ділянки волокна починаючи від місця виникнення. Іони натрію, що входять всередину збудженної ділянки, є носіями електричного заряду, необхідного для виникнення ПД у прилеглих ділянках. У цьому разі, імпульс виникає між деполяризованою ділянкою мембрани і її незбудженою ділянкою. Різниця потенціалів, при цьому, буває у багато разів вища, ніж необхідна для того, щоб деполяризація мембрани досягла граничного рівню. Швидкість поширення імпульсу в таких волокнах 0,5-2 м/с[6]
Розповсюдження в мієлінізованому волокні[ред. | ред. код]

Аксони більшості соматичних нервів мієлінізовані. Лише дуже незначні їхні ділянки, так звані перехвати вузла (Кільця Ранв'є[en]), укриті звичайною клітинною мембраною. Такі нервові волокна відзначаються тим, що на мембрані лише в перехватах, розміщенні потенціал-залежні іонні канали. До того ж, ця оболонка підвищує електричний опір мембрани. Тому при зрушенні мембранного потенціалу, струм проходить через мембрану перехоплювальної ділянки, тобто стрибками (сальтаторно) від одного перехоплення до іншого, що дозволяє збільшити швидкість проведення нервового імпульсу, яка становить від 5 до 120 м/с[6]. Водночас потенціал дії, який виник в одному з перехватів Ранв'є, викликає потенціали дії в сусідніх перехватах за рахунок виникнення електричного поля, яке викликає початкову деполяризацію в цих перехватах. Параметри електрорушійної сили поля та віддаль його ефективної дії, залежать від провідних властивостей аксона.
| Тип | Діаметр (мкм) | Мієлінізація | Швидкість проведення (м/с) | Функціональне призначення |
|---|---|---|---|---|
| А alpha | 12–20 | сильна | 70–120 | Рухливі волокна соматичної НС; чутливі волокна пропріорецепторів |
| А beta | 5–12 | сильна | 30–70 | Чутливі волокна рецепторів шкіри |
| А gamma | 3–16 | сильна | 15–30 | Чутливі волокна пропріорецепторів |
| А delta | 2–5 | сильна | 12–30 | Чутливі волокна терморецепторів, ноцицепторів |
| В | 1–3 | слабка | 3–15 | Прегангліонарні волокна симпатичної НС |
| С | 0,3–1,3 | відсутня | 0,5–2,3 | Постгангліонарні волокна симпатичної НС; чутливі волокна терморецепторів, ноцицепторів, деяких механорецепторів |
Поширення потенціалу дії між клітинами[ред. | ред. код]
В хімічному синапсі після того, як хвиля потенціалу дії доходить нервового закінчення, вона викликає вивільнення нейротрансмітерів з пресинаптичних пухирців в синаптичну щілину. Молекули медіатора, що вивільняються з пресинапсу, зв'язуються з рецепторами на постсинаптичній мембрані, в результаті чого в рецепторних макромолекулах відкриваються іонні канали. Іони, що починають надходити всередину постсинаптичної клітини через відкриті канали, змінюють заряд її мембрани, що призводить до часткової деполярізації мембрани і, як наслідок, провокування генерації постсинаптичною клітиною потенціалу дії.
В електричному синапсі відсутній «посередник» передачі у вигляді нейромедіатора. Натомість клітини поєднані між собою за допомогою специфічних протеїнових тунелів — конексонів, тому іонні токи, з пресинаптичної клітини можуть стимулювати постсинаптичну клітину, викликаючи зародження в ній потенціалу дії. Завдяки такій будові, потенціал дії може поширюватися в обидва боки і значно швидше ніж через хімічний синапс.
-
Схема процесу передачі нервового сигналу в хімічному синапсі
-
Передача потенціалу дії через хімічний синапс. Червоним показані іони кальцію, жовтим — натрію, зеленим — нейромедіатори
-
Схема будови електричного синапсу
Потенціал дії в різних типах клітин[ред. | ред. код]
Потенціал дії в м'язових тканинах[ред. | ред. код]
Потенціал дії в скелетних м'язових клітинах подібний потенціалу дії в нейронах. Потенціал спокою в них, переважно -90мВ, що більше, ніж потенціал спокою типових нейронів (-60 -70мВ). Потенціал дії м'язових клітин триває приблизно 2-4 мс, абсолютний рефрактерний період становить приблизно 1-3 мс, а швидкість провідності вздовж м'язів приблизно 5 м/сек.
Потенціал дії в серцевих тканинах[ред. | ред. код]
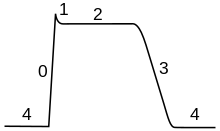
Потенціал дії клітин робочого міокарду складається з фази швидкої деполяризації, початкової швидкої реполяризації, яка переходить в фазу повільної реполяризації (фаза плато), і фази швидкої кінцевої реполяризації. Фаза швидкої деполяризації зумовлена різким підвищенням проникності мембрани для іонів натрію, що викликає швидкий вхідний натрієвий струм, який при досягненні мембранного потенціалу 30—40 мВ інактивується і надалі головну роль відіграє кальцієвий іонний струм. Деполяризація мембрани викликає активацію кальцієвих каналів, внаслідок чого виникає додатковий деполяризуючий вхідний кальцієвий струм.
Потенціал дії в серцевій тканині відіграє важливу роль в узгодженні скорочень серця.[7]
Молекулярні механізми виникнення потенціалу дії[ред. | ред. код]

Активні властивості мембрани, що забезпечують виникнення потенціалу дії, ґрунтуються здебільшого на поведінці потенціал-залежних натрієвих (Na+) і калієвих (K+) каналів. Початкова фаза ПД утворюється вхідним натрієвим струмом, згодом відкриваються калієві канали і вихідний K+-струм повертає потенціал мембрани до вихідного рівня. Початкову концентрацію іонів потім відновлює натрій-калієвий насос.
По ходу ПД канали переходять зі стану в стан: у Na+-каналів основних стани три — закритий, відкритий і інактивований (насправді все складніше, але цих трьох станів достатньо для опису), у K+ каналів два — закритий і відкритий.
Поведінка каналів, що беруть участь в утворенні ПД, описується через провідність і розраховується через коефіцієнти переносу (трансферу).
Коефіцієнти переносу були виведені Алан Ллойд Ходжкіном та Ендрю Хакслі.[8][9]
- Провідність для калію GK на одиницю площі [S/cm²]
| , |
| де: |
| - коефіцієнт трансферу з закритого у відкритий стан для K+ каналів [1/s]; |
| - коефіцієнт трансферу з відкритого в закритий стан для K+ каналів [1/s]; |
| - фракція К+ каналів у відкритому стані; |
| - фракція К+ каналів в закритому стані |
- Провідність для натрію GNa на одиницю площі [S/cm²]
розрахувати складніше, оскільки, як вже було згадано, у потенціал-залежних Na+ каналів, окрім закритого/відкритого станів, перехід між якими параметром , є ще інактивований/не-інактивований стани, перехід між якими описується через параметр
| , | , |
| де: | де: |
| - коефіцієнт трансферу з закритого у відкритий стан для Na+ каналів [1/s]; | - коефіцієнт трансферу з інактивованого в не-інактивований стан для Na+ каналів [1/s]; |
| - коефіцієнт трансферу з відкритого в закритий стан для Na+ каналів [1/s]; | - коефіцієнт трансферу з не-інактивованого в інактивований стан для Na+ каналів [1/s]; |
| - фракція Na+ каналів в відкритому стані; | - фракція Na+ каналів в не-інактивованому стані; |
| - фракція Na+ каналів в закритому стані | - фракція Na+ каналів в інактивованому стані. |
Методи дослідження[ред. | ред. код]
Історія[ред. | ред. код]
Основні положення мембранної теорії збудження сформульовані німецьким нейрофізіологом Ю.Бернштейном
У 1902 році Юліус Бернштейн висунув гіпотезу, згідно з якою клітинна мембрана пропускає всередину клітини іони К+, і вони накопичуються в цитоплазмі. Розрахунок величини потенціалу спокою за рівнянням Нернста для калієвого електрода задовільно збігся з виміряним потенціалом між саркоплазмою м'яза і навколишнім середовищем, який становив близько — 70 мВ. Відповідно до теорії Ю.Бернштейна, зі збудженням клітини її мембрана ушкоджується, і іони К+ виходять з клітини по концентраційному градієнту доти, поки потенціал мембрани не стає рівним нулю. Потім мембрана відновлює свою цілісність, і потенціал повертається до рівня потенціалу спокою.
Цю модель розвинули у своїй роботі 1952 року Алан Ллойд Годжкін та Ендрю Гакслі, в якій описали електричні механізми, що зумовлюють генерацію та передавання нервового сигналу в гігантському аксоні кальмара. За це автори моделі отримали Нобелівську премію в галузі фізіології або медицини за 1963 рік. Модель дістала назву Модель Годжкіна-Гакслі
2005 року, Томасом Геймбургом і Анрю Д. Джексоном була запропонована солітонна модель, яка ґрунтується на припущенні, що сигнал по нейронах поширюється у вигляді солітонів — стійких хвиль, що розповсюджуються по клітинній мембрані.[10]
Вплив деяких речовин на потенціал дії[ред. | ред. код]

Деякі речовини органічного, або синтетичного походження можуть блокувати утворення або проходження ПД:
- Батрахотоксин знайдений у деяких представників роду Листолаз. Стійко і необоротно підвищує проникність мембран для іонів Натрію.[11]
- Понератоксин був знайдений в мурахах роду Paraponera. Блокує натрієві канали.[6]
- Тетродотоксин знайдений в тканинах риб родини Скелезубові, з яких готують японський делікатес Фугу. Блокує натрієві канали.
- Спосіб дії більшості анестетиків (Прокаїн, Лідокаїн) оснований на блокуванні натрієвих каналів і відповідно на блокуванні проведення імпульсів чутливими нервовими волокнами.
- 4-Амінопиридин — зворотньо блокує калієві канали, що подовжує тривалість потенціалу дії. Може використовуватися в терапії розсіяного склерозу.[12]
- ADWX 1 — зворотньо блокує калієві канали. В умовах досліду полегшував перебіг гострого розсіяного енцефаломієліту у щурів.[13]
Див. також[ред. | ред. код]
- Мембранний потенціал спокою
- Мембранний транспорт
- Натрій-калієвий насос
- Модель Годжкіна-Гакслі
- Солітонна модель
Література[ред. | ред. код]
- ↑ а б Фізіологія людини: підручник / В.І. Філімонов. -- К.: ВСВ "Медицина", 2011
- ↑ а б Физиология человека. В 3-х томах. Под ред. Р. Шмидта и Г. Тевса
- ↑ В.В.Ревин. Биофизика. Саранск: Изд-во Мордов. ун-та, 2002
- ↑ Л.І. Григор’єва, Ю.А. Томілін Основи біофізики і біомеханіки
- ↑ Орлов Р.С., Ноздрачёв А.Д. Нормальная физиология : Учебник. - М.: ГЭОТАР-Медиа, 2009. 688 с. - Глава 5. Физиология нейронов. - Потенциал действия. С. 73-78.
- ↑ а б в Физиология человека : Учебник / Под редакцией В.М.Покровского, Г.Ф.Коротько. 2-е изд., перераб. и доп.- М.: ОАО «Издательство «Медицина», 2007 г
- ↑ Kléber AG, Rudy Y (April 2004). Basic mechanisms of cardiac impulse propagation and associated arrhythmias. Physiol. Rev. 84 (2): 431—88. doi:10.1152/physrev.00025.2003. PMID 15044680.
- ↑ Hodgkin AL, Huxley AF (1952) A quantitative description of membrane current and its application to conduction and excitation in nerve. J. Physiol. (Lond.) 117: 500—544. PMID 12991237 free full text(англ.)
- ↑ J.Malmivuo, R.Plonsey. Bioelectromagnetism. Oxford University Press. New York, Oxford. 1995.free full text [Архівовано 26 травня 2010 у Wayback Machine.](англ.)
- ↑ Thomas Heimburg, Andrew D. Jackson. On soliton propagation in biomembranes and nerves. PNAS, vol 102, no. 2. 12 July 2005
- ↑ Орлов Б.Н., Гелашвили Д.Б. "Зоотоксинология: ядовитые животные и их яды" М.:Высшая школа 1985 стр. 190-192
- ↑ Judge S, Bever C (2006). Potassium channel blockers in multiple sclerosis: neuronal Kv channels and effects of symptomatic treatment. Pharmacol. Ther. 111 (1): 224—59. doi:10.1016/j.pharmthera.2005.10.006. PMID 16472864.
- ↑ PMID 22761436 (PMID 22761436)
Бібліографічний опис з'явиться автоматично через деякий час. Ви можете підставити цитату власноруч або використовуючи бота.
Посилання[ред. | ред. код]
Анімація
- Action potential propagation in myelinated and unmyelinated axons at Blackwell Publishing
- Generation of AP in cardiac cells [Архівовано 6 вересня 2010 у Wayback Machine.] and generation of AP in neuron cells [Архівовано 27 липня 2011 у Wayback Machine.]
- Resting membrane potential from Life: The Science of Biology, by WK Purves, D Sadava, GH Orians, and HC Heller, 8th edition, New York: WH Freeman, ISBN 978-0-7167-7671-0.
- Ionic motion and the Goldman voltage for arbitrary ionic concentrations [Архівовано 8 серпня 2010 у Wayback Machine.] at University of Arizona
- A cartoon illustrating the action potential
Статті та інші матеріали
- The Action Potential John Kinnamon, University of Denver
- Resting and Action Membrane Potentials [Архівовано 23 грудня 2007 у Wayback Machine.] Teaching Resources Center, UC Davis. Animated tutorials
- Open-source software to simulate neuronal and cardiac action potentials [Архівовано 27 квітня 2006 у Wayback Machine.] at SourceForge.net
|