APAF1

APAF1 (англ. Apoptotic peptidase activating factor 1) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 12-ї хромосоми.[3] Довжина поліпептидного ланцюга білка становить 1 248 амінокислот, а молекулярна маса — 141 840[4].
Білок можна розділити на три домени: N-кінцевий домен CARD (англ. caspase recruitment domain) - необхідний для функції APAF1; альтернативно, він може зв'язувати домен WD40 або цитохром С. Домен C-terminal WD40 є негативним регулятором, який складається з 12 або 13 повторів WD40: він може зв'язувати домен CARD, але може взаємодіяти з іншими білками апоптотичного регулятора[5].
Задіяний у таких біологічних процесах, як апоптоз, альтернативний сплайсинг. Білок має сайт для зв'язування з АТФ, нуклеотидами, іоном кальцію. Локалізований у цитозолі.
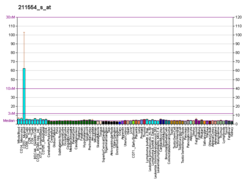
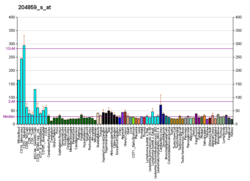
Експресія
Найвищі рівні експресії у дорослих лейкоцитів селезінки і периферичної крові, а також у мозку, нирках і легенях. Ізоформ 1 експресується в серці, нирках і печінці.[6] Apaf-1 являє собою пряму транскрипційну мішень р53, який може сенсибілізувати клітини до апоптозу за рахунок підвищення рівнів Apaf-1. [7]
Функції
APAF1 є структурним ядром апоптосоми. Коли активується мітохондріальний шлях апоптозу, цитохром С вивільняється з мітохондрій до цитозолу, а потім зв'язується з доменом APAF1 CARD, змінюючи його конформацію. Подальше зв'язування молекул АТФ опосередковує другу конформаційну зміну, що призводить до відкритої конформації APAF1. За допомогою домену CARD сім молекул APAF1 зв'язуються один з одним і до семи молекул ініціатора Caspase-9, що утворюють апоптосому і викликають активацію ефекторних каспаз. Утворення апоптосоми і активація каспаз регулюються численними взаємодіючими білками[5].
Основні функції білка:
- функціонує в якості адаптера в багатопротеїновому комплексі 700 кДа (названому апоптосомою), щоб опосередкувати активацію каспази-9
- активує апоптозний комплекс апоптозу каспази 9 і APF1 в присутності цитохрому С і АТФ, що призводить до активації каспази 3 і, таким чином, до апоптозу
- рецептор поглинача гемоглобіну
- впливає на зупинку клітинного циклу, викликаного пошкодженням ДНК
- відіграє необхідну роль для розщеплення або активації всіх пропаз і сприяє мітохондріальним апоптотичним подіям, індукованими генотоксичними препаратами
- відіграє роль у підтримці геномної стабільності незалежно від її функції в механізмі загибелі клітин
- не вимагає енергії від нуклеотидного гідролізу до кінцевої форми апоптосоми
- має неапоптозну роль у патології нейродегенеративних захворювань, залежних від білків-агрегації, таких як хвороба Хантінгтона
- необхідний для міноциклін-залежного інгібування загибелі клітин
- може служити прямим або непрямим датчиком або модулятором метаболічного стану ER / мітохондрій
- передає сигнал смерті в мітохондріальному шляху апоптозу
- основний компонент апоптосоми і вирішальний фактор в мітохондрій-залежному шляху смерті
- грає вирішальну роль ядерної релокалізації APAF1 в опосередкуванні зупинки клітинного циклу, індукованого генотоксичним стресом[8]
Ген
Локалізація
12q23[8]
ДНК / РНК
Ген APAF1 складається з 27 екзонів, причому область кодування охоплює 26 екзонів
Транскрипція
П'ять ізоформ кДНК APAF1 були виявлені у Homo sapiens
- оригінальний APAF1 (також званий Apaf-1S) довжиною 3585 bp (він містить 12 повторів WD40);
- ізоформа APAF1-1M (3618 п.о.) містить вставку 33 nt після позиції 295 першої опублікованої послідовності;
- ізоформа APAF-1XS (3516 п.н.) містить таку ж вставку Apaf-1M форми, не має пар основ від 3171 до 3296 форми Apaf-1S (делеція в домені WD40), але має вставку 24 nt в положенні 1725
- APAF-1L (3714 bp) містить вставку 129 nt в положенні 2466 (містить 13 повторів WD40);
- ізоформа APAF-1XL (3747 bp) містить таку ж інсерцію форми APAF-1M і додаткову інсерцію 129 bp (містить 13 повторів WD40)[5].
Регуляція
Не інгібується зв'язуванням з BCL2. Репресований міноцикліном,який інгібує власну активацію апоптозу (опосередковану мітохондріями), але не зовнішню, через інгібуючу дію на активність APAF1.[8] Клітини, оброблені міноцикліном стійкі до розвитку мутантної агрегації білка.[9] Фізіологічні концентрації іонів кальцію негативно впливають на збірку апоптосом шляхом інгібування нуклеотидного обміну в мономерній формі.[6]
Залучений до
- Раку шкіри (меланома, карцинома базальних клітин, плоскоклітинний рак)
- Пухлин головного мозку (нейронні пухлини, гліальні пухлини)
- Раку голови та шиї, а також одонтогенних пухлин
- Раку шлунково-кишкового тракту (рак стравоходу, рак шлунка, рак жовчного міхура, рак черевоподібного відростка, рак товстої кишки, рак прямої кишки, рак ануса)
- Раку підшлункової залози
- Раку печінки і метастазів в печінці
- Раку легенів
- Пухлин жіночих статевих органів (карцинома яєчників, новоутворення фаллопієвої труби, ендометрія)
- Пухлин чоловічих статевих органів (семінома, пухлини статевих клітин, статеві пухлини, інші раки яєчка, новоутворення простати, пухлина статевого члена)
- Пухлин сечовивідних шляхів (нирково-клітинна карцинома, новоутворення ниркової миски, сечоводу, сечового міхура, уретри)
- Пухлин кровотворної системи [5]
Взаємодії
Показано, що APAF1 взаємодіє з:
Значення
APAF-1 відіграє важливу роль у запрограмованій загибелі клітин і допомагає підтримувати різні гомеостатичні функції. Враховуючи здатність APAF-1 активувати або пригнічувати апоптоз, вивчення APAF-1 може призвести до серйозних успіхів у сучасній медицині. По-перше, подальше дослідження APAF-1 може призвести до нових досягнень у розумінні та лікуванні раку. Ракові клітини мають незвичайну здатність ухилятися від апоптозу, і вони отримують цю здатність від мутацій до прото-онкогенів, які зазвичай підтримують і контролюють апоптоз. Вивчення APAF-1 могло б забезпечити краще розуміння того, як апоптоз може бути індукований або навіть відновлений в ракових клітинах для цільових пухлин. Подальші дослідження APAF-1 могли б навіть призвести до більшого розуміння того, як рак походить з інших нормальних клітин. APAF-1 також може бути вивчений для розвитку нашого розуміння нейродегенеративних розладів, таких як хвороба Альцгеймера і хвороба Паркінсона. Обидві ці зміни, що змінюють життя, є результатом дегенерації різних компонентів центральної нервової системи. Таким чином, апоптоз активний, коли він повинен бути в стані спокою. Можливо, подальші дослідження APAF-1 можуть допомогти виправити ці захворювання або навіть виявити основні причини[16].
Література
- Zou H., Henzel W.J., Liu X., Lutschg A., Wang X. (1997). Apaf-1, a human protein homologous to C. elegans CED-4, participates in cytochrome c-dependent activation of caspase-3. Cell. 90: 405—413. PMID 9267021 DOI:10.1016/S0092-8674(00)80501-2
- Hahn C., Hirsch B., Jahnke D., Duerkop H., Stein H. (1999). Three new types of Apaf-1 in mammalian cells. Biochem. Biophys. Res. Commun. 261: 746—749. PMID 10441496 DOI:10.1006/bbrc.1999.1124
- Saleh A., Srinivasula S.M., Acharya S., Fishel R., Alnemri E.S. (1999). Cytochrome c and dATP-mediated oligomerization of Apaf-1 is a prerequisite for procaspase-9 activation. J. Biol. Chem. 274: 17941—17945. PMID 10364241 DOI:10.1074/jbc.274.25.17941
- Hu Y., Benedict M.A., Ding L., Nunez G. (1999). Role of cytochrome c and dATP/ATP hydrolysis in Apaf-1-mediated caspase-9 activation and apoptosis. EMBO J. 18: 3586—3595. PMID 10393175 DOI:10.1093/emboj/18.13.3586
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Srinivasula S.M., Ahmad M., Fernandes-Alnemri T., Alnemri E.S. (1998). Autoactivation of procaspase-9 by Apaf-1-mediated oligomerization. Mol. Cell. 1: 949—957. PMID 9651578 DOI:10.1016/S1097-2765(00)80095-7
Примітки

- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:576 (англ.) . Процитовано 11 вересня 2017.
- ↑ UniProt, O14727 (англ.) . Процитовано 11 вересня 2017.
- ↑ а б в г APAF1 (Apoptotic protease activating factor 1). atlasgeneticsoncology.org. Процитовано 10 січня 2019.
- ↑ а б APAF1 - Apoptotic protease-activating factor 1 - Homo sapiens (Human) - APAF1 gene & protein. www.uniprot.org. Процитовано 14 січня 2019.
- ↑ Helin, Kristian; Müller, Heiko; Cecconi, Francesco; Elena Colli; Caprara, Greta; Denchi, Eros Lazzerini; Hickman, Emma S.; Moroni, M. Cristina (2001-06). Apaf-1 is a transcriptional target for E2F and p53. Nature Cell Biology (англ.). Т. 3, № 6. с. 552—558. doi:10.1038/35078527. ISSN 1476-4679. Процитовано 14 січня 2019.
- ↑ а б в Genatlas sheet. genatlas.medecine.univ-paris5.fr. Процитовано 10 січня 2019.
- ↑ Sancho, Mónica; Herrera, Andrés E.; Gortat, Anna; Carbajo, Rodrigo J.; Pineda-Lucena, Antonio; Orzáez, Mar; Pérez-Payá, Enrique (15 вересня 2011). Minocycline inhibits cell death and decreases mutant Huntingtin aggregation by targeting Apaf-1. Human Molecular Genetics. Т. 20, № 18. с. 3545—3553. doi:10.1093/hmg/ddr271. ISSN 1460-2083. PMID 21659333. Процитовано 14 січня 2019.
- ↑ а б Jung, Yong-Keun; Mak, Tak W.; Pyo, Jong-Ok; Woo, Ha-Na; Lee, Ho-June; Hong, Yeon-Mi; Cho, Dong-Hyung (17 вересня 2004). Induced Inhibition of Ischemic/Hypoxic Injury by APIP, a Novel Apaf-1-interacting Protein. Journal of Biological Chemistry (англ.). Т. 279, № 38. с. 39942—39950. doi:10.1074/jbc.M405747200. ISSN 1083-351X. PMID 15262985. Процитовано 10 січня 2019.
{{cite news}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ а б Núñez, Gabriel; Inohara, Naohiro; Wu, Dayang; Benedict, Mary A.; Hu, Yuanming (14 квітня 1998). Bcl-XL interacts with Apaf-1 and inhibits Apaf-1-dependent caspase-9 activation. Proceedings of the National Academy of Sciences (англ.). Т. 95, № 8. с. 4386—4391. doi:10.1073/pnas.95.8.4386. ISSN 1091-6490. PMID 9539746. Процитовано 10 січня 2019.
- ↑ а б Dixit, Vishva M.; O’Rourke, Karen; Pan, Guohua (6 березня 1998). Caspase-9, Bcl-XL, and Apaf-1 Form a Ternary Complex. Journal of Biological Chemistry (англ.). Т. 273, № 10. с. 5841—5845. doi:10.1074/jbc.273.10.5841. ISSN 1083-351X. PMID 9488720. Процитовано 10 січня 2019.
{{cite news}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ а б Reed, John C.; Godzik, Adam; Krajewski, Stan; Krajewska, Maryla; Welsh, Kate; Xie, Zhihua; Pio, Frederick; Chu, Zhi-Liang (23 березня 2001). A Novel Enhancer of the Apaf1 Apoptosome Involved in Cytochrome c-dependent Caspase Activation and Apoptosis. Journal of Biological Chemistry (англ.). Т. 276, № 12. с. 9239—9245. doi:10.1074/jbc.M006309200. ISSN 1083-351X. PMID 11113115. Процитовано 10 січня 2019.
{{cite news}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ Wang, Xiaodong; Alnemri, Emad S.; Ahmad, Manzoor; Srinivasula, Srinivasa M.; Budihardjo, Imawati; Nijhawan, Deepak; Li, Peng (14 листопада 1997). Cytochrome c and dATP-Dependent Formation of Apaf-1/Caspase-9 Complex Initiates an Apoptotic Protease Cascade. Cell (English) . Т. 91, № 4. с. 479—489. doi:10.1016/S0092-8674(00)80434-1. ISSN 1097-4172. PMID 9390557. Процитовано 10 січня 2019.
- ↑ Alnemri, Emad S.; Robbins, Paul D.; Balkir, Levent; Srinivasula, Srinivasa M.; Saleh, Ayman (2000-08). Negative regulation of the Apaf-1 apoptosome by Hsp70. Nature Cell Biology (англ.). Т. 2, № 8. с. 476—483. doi:10.1038/35019510. ISSN 1476-4679. Процитовано 10 січня 2019.
- ↑ APAF_1. collab.its.virginia.edu. Процитовано 10 січня 2019.
Див. також
| Це незавершена стаття про білки. Ви можете допомогти проєкту, виправивши або дописавши її. |