Ксилени
 |
 |

|
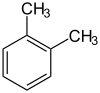
| о-ксилен | м-ксилен | п-ксилен |
Ксиле́ни, ксило́ли (від грец. ξύλον, xylon — деревина) — органічні сполуки ряду аренів, ізомери складу C6H4(CH3)2. Залежно від взаємного розташування метильних груп у бензеновому ядрі розрізняють: орто-ксилен (1,2-диметилбензен), мета-ксилен (1,3-диметилбензен) і пара-ксилен (1,4-диметилбензен).
Історія[ред. | ред. код]
Ксилени вперше були виділені 1850 року французьким хіміком Огюстом Кауром з неочищеного деревного спирту. В 1855 році їх отримали з кам'яновугільної смоли німецький біохімік Карл Генріх Ріттхаузен і британський хімік Артур Герберт Черч.
У проміжку з 1865 по 1869 роки Фіттіг та Ернст з'ясували, що виділена зі смоли речовина «ксилен» не є однією сполукою. Для перевірки цієї теорії вони синтезували ксилен з толуену, назвавши його метилтолуен (пізніше стало відомо, що ним є пара-ксилен). Після порівняння властивостей отриманого «метилтолуену» та «ксилену» дослідники дійшли до висновку, що присутні сполуки мають різні положення метильної групи.
У 1865 році Фіттіг розробив метод синтезу ксилену, що полягав у перегонці кальцієвої солі 2,4,6-триметилбензойної (мезитойної) кислоти. І хоча отримана сполука виявляла властивості, подібні до раніше отриманих «ксилену» та «метилтолуену», вона не була ідентичною до них. Її назвали ізоксилен (мета-ксилен). В ході подальших досліджень Фіттіг ідентифікував третій ізомер — орто-ксилен, що був виділений з кам'яновугільної смоли Оскаром Якобсоном у 1877 році.
Поширення у природі[ред. | ред. код]
| Цей розділ потребує доповнення. (березень 2016) |
Основним джерелом ксиленів у природі є нафта. Також для їхнього добування застосовується вугілля.
Фізичні властивості[ред. | ред. код]
| орто-Ксилен | мета-Ксилен | пара-Ксилен | |
|---|---|---|---|
| Зовнішній вигляд | безбарвна рідина | ||
| Густина, г/см³ | 0,8760 | 0,8599 | 0,8567 |
| Температура плавлення, °C | -25,2 | -47,8 | 13,25 |
| Температура кипіння, °C | 144,4 | 139,1 | 138,4 |
| Розчинність у воді, г/л | 0,171 | 0,161 | 0,181 |
| В'язкість, мПа·с | 1,084 (0 °C) 0,760 (25 °C) 0,561 (50 °C) |
0,795 (0 °C) 0,581 (25 °C) 0,445 (50 °C) |
0,603 (25 °C) 0,457 (50 °C) 0,359 (75 °C) |
| Показник заломлення | 1,5054 | 1,4971 | 1,4958 |
| Діелектрична проникність | 2,562 | 2,359 | 2,2735 |
| Температура спалаху, °C | 32 | 27 | 27 |
| Вибухові границі, % | 1—7 | ||
| Температура самозаймання, °C | 463 | 527 | 528 |
| Якщо не зазначено інше, дані приведені для речовин у стандартному стані (за 25 °C, 100 кПа) | |||
Отримання[ред. | ред. код]
Каталітичний риформінг[ред. | ред. код]
Ксилени (переважно пара- та орто) отримують з легких фракцій (температурою 65—170 °C).
Отримання з толуену[ред. | ред. код]
Толуен диспропорціонує з утворенням бензену і ксилену (переважно пара- та орто-):
Також він отримує метильну групу внаслідок трансалкілювання при взаємодії з алкілбензенами, що мають більший бічний ланцюг, в тому числі з етилбензеном.
Інші методи[ред. | ред. код]
Ксилени можна синтезувати шляхом алкілювання бензенового ядра за реакцією Фріделя — Крафтса:
Введення другої метильної групи здійснюється за орто- або пара-положеннями, оскільки перший метильний замісник є орієнтантом першого роду.
Складність синтезу шляхом алкілювання полягає в тому, що продукти мають здатність ізомеризуватися, особливо за великого надлишку каталізаторів. Так, п- і о-ксилени можуть ізомеризуватися до м-ксилену[1].
Хімічні властивості[ред. | ред. код]
Хімічні властивості ксиленів більшою мірою визначаються наявність метильних груп.
Окиснення[ред. | ред. код]
При окисненні ксиленів відбуваються переважно перетворення CH3-груп. Так, при взаємодії з сильними окисниками типу дихроматів, перманганатів, метильні групи окиснюються до карбоксильних. Ця реакція має широке значення в отриманні промислово важливої терефталевої кислоти (бензен-1,4-діової) з п-ксилену.
Окрім того є можливим проведення неповного окиснення метильних груп — за допомогою суміші оксиду хрому(VI) та оцтового ангідриду. Окиснення проходить лише до стадії отримання альдегідних груп, оскільки подальший процес є неможливим через приєднання до атомів Карбону ацильних груп, які за даних умов є стійкими. Подальшим кислотним гідролізом отримують ароматичний діальдегід[2].
Окремий випадок складає каталітичне окиснення о-ксилену до фталевого ангідриду:
До випадків окиснення бензенового кільця можна віднести озоноліз ксиленів — відбувається розрив подвійних зв'язків та утворення простіших оксосполук. Наприклад, при озонолізі о-ксилену утворюються гліоксаль, метилгліоксаль і діацетил у співвідношенні 3:2:1[3].
Відновлення[ред. | ред. код]
Повне відновлення (гідрування) ксиленів іде з утворенням диметилциклогексанів. При цьому утворюється суміш цис- і транс-ізомерів, що відрізняються положенням CH3-груп по відношенню до площини бензенового кільця. При гідруванні на твердих каталізаторах переважними є цис-ізомери — це пов'язано із цис-розташуванням метильних груп при закріпленні на поверхні каталізатору. Так, продуктами гідрування на родієвому каталізаторі (при 100 °C, 30 атм) є цис- і транс-ізомери у співвідношенні 9:1[4].
Неповне відновлення ксиленів проходить із утворенням заміщених циклогексадієнів. Таку реакцію можна здійснити відновленням натрієм в рідкому аміаці (відновлення за Берчем)[5]:
У промисловості відновлення ксиленів як нафтової сировини застосовують для отримання бензену: при високих температурах відбувається деметилювання, що веде до утворення бензену і метану[6]:
Галогенування[ред. | ред. код]
Подібно до толуену, галогенування ксиленів відбувається за вільнорадикальним механізмом, у бічний ланцюг. Взаємодія з хлором та бромом при наявності сонячного світла веде до утворення моно- і дигалогенопохідних[7].
Токсичність[ред. | ред. код]
Потрапляння ксиленів до організму можливе шляхом інгаляції або резорбції крізь шкіру.
Їхня повторювана дія спричинює подразнення дихальних шляхів та слизових оболонок. Контактуючи зі шкірою, вони можуть залишати пухирці і провокувати дерматит. При концентрації у повітрі від 100 до 1000 см³/м³ ксилени подразнюють ЦНС, наслідками чого можуть бути сповільнена реакція, головний біль, нудота. Також спостерігаються зміни кров'яного тиску. Дія ксиленів у великих дозах (близько 10 000 см³/м³) призводить до набряку легень і подальшої смерті.
Тривала дія ксиленів призводить до сильного пошкодження ЦНС, внаслідок чого з'являється порушення сну, диспепсія. Усі симптоми є зворотніми. Окрім поступового збільшення толерантності до подразника, може також спостерігатися звикання (ксилени демонструють пренаркотичну і наркотичну дії).
Ксилени не проявляють явних канцерогенних і мутагенних властивостей. У довготермінових експериментах з пацюками дія ксиленів мала незначний вплив на розвиток плоду.
Застосування[ред. | ред. код]
Основна частина ксиленів (які здебільшого отримують за допомогою риформінгу) застосовується як додатки до пального. пара-Ксилен має найбільше практичне значення — з нього синтезують терефталеву кислоту, що йде на виробництво диметилтерефталату і поліетилентерефталату. Отримуваний орто-ксилен є прекурсором для отримання фталевого ангідриду — компоненту пластифікаторів. Також з орто-ксилену синтезують фталонітрил, котрий використовується в отриманні барвників фталоціанів. Мета-ксилен може використовуватися для синтезу ізофталевої кислоти, що йде на отримання поліестерів, ізофталонітрилу та його похідної — фунгіциду тетрахлороізофталонітрилу, однак загалом він не має значного застосування, тому основну його частину ізомеризують з метою добування інших ксиленів.
Ксилени можуть використовуватися в ролі розчинників та компонентів покриттів, але це застосування не є поширеним через їхню небезпеку для довкілля.
Розчин ксилену використовують для депарафінізації при виділення ДНК з архівних тканин, що були фіксовані в формальдегіді та залучені в парафіновий блок.
Див. також[ред. | ред. код]
| Вікісховище має мультимедійні дані за темою: Ксилени |
Примітки[ред. | ред. код]
- ↑ Робертс, Дж., Касерио, М. Основы органической химии / Под ред. А. Н. Несмеянова. — М. : Мир, 1978. — Т. 2. — С. 193—194. (рос.)
- ↑ Реутов, Курц, Бутин, 1999, с. 386.
- ↑ Чирва В. Я., Ярмолюк С. М., Толкачова Н. В., Земляков О. Є. Органічна хімія. — Львів : БаК, 2009. — С. 662. — ISBN 966-7065-87-4.
- ↑ Реутов, Курц, Бутин, 1999, с. 389.
- ↑ Травень В. Ф. Органическая химия. Учебник для вузов. — М. : ИКЦ «Академкнига», 2004. — Т. 1. — С. 478. — ISBN 5-94628-068-6. (рос.)
- ↑ Ластухін Ю. О., Воронов С. А. Органічна хімія : підручник. — Вид. 3-тє, стереотипне. — Львів : Центр Європи, 2006. — С. 620. — ISBN 966-7022-19-6.
- ↑ Реутов, Курц, Бутин, 1999, с. 381—382.
Джерела[ред. | ред. код]
- CRC Handbook of Chemistry and Physics / Lide, D. R., editor. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Cannella, William J. Xylenes and Ethylbenzene // Kirk-Othmer Encyclopedia of Chemical Technology. — 4th. — New York : John Wiley & Sons, 2004. — Vol. Supplement. — P. 410—424. — ISBN 978-0-471-48517-9. — DOI: (англ.)
- Lange's Handbook of Chemistry / Dean, John A., editor. — 15th. — New York : McGraw-Hill, 1999. — ISBN 0-07-016384-7. (англ.)
- Fabri, J., Graeser, U., Simo, Thomas A. Xylenes // Ullmann's Encyclopedia of Industrial Chemistry. — 6th. — Weinheim : Wiley-VCH, 2005. — 21 p. — DOI: (англ.)
- Реутов О. А., Курц А. Л., Бутин К. П. Органическая химия. — М. : Изд. МГУ, 1999. — Т. 2. — С. 386. — ISBN 5-211-03491-0. (рос.)




