Цистеїн
| L-Цистеїн | |
|---|---|

| |

| |
| Інші назви | 2-аміно-3-меркаптопропанова кислота |
| Ідентифікатори | |
| Абревіатури | C, Cys |
| Номер CAS |
52-89-1 (гідрохлорид) 52-90-4 52-89-1 (гідрохлорид) |
| PubChem | 5862 |
| Номер EINECS | 200-158-2 |
| DrugBank | 00151 |
| KEGG | D00026 і C00097 |
| Назва MeSH | D02.886.030.230, D02.886.489.155, D12.125.154.299 і D12.125.166.230 |
| ChEBI | 17561 |
| SMILES | C(C(C(=O)O)N)S |
| InChI | InChI=1S/C3H7NO2S/c4-2(1-7)3(5)6/h2,7H,1,4H2,(H,5,6)/t2-/m0/s1 |
| Номер Бельштейна | 1721408 |
| Номер Гмеліна | 49992 |
| Властивості | |
| Молекулярна формула | C3H7NO2S |
| Молярна маса | 121,16 г/моль |
| Зовнішній вигляд | білий порошок, або білі кристали |
| Тпл | 240 °C (розкладається) |
| Розчинність (вода) | розчинний у воді |
| Ізоелектрична точка | 5,02[1] |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
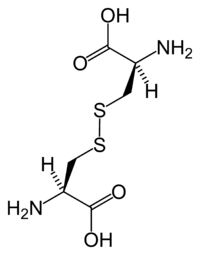
Цистеї́н — одна з амінокислот, L-ізомер якої входить до складу білків. Надзвичайно важливий для формування третинної структури білків завдяки здатності утворювати дисульфідні містки й фіксувати наближеними у просторі ділянки протеїну віддалені по послідовності. Цистеїн — аліфатична амінокислота, яка містить SH-групу.[2] Позначення: Cys, C. Кодони: UGU, UGC.
Біосинтез цистеїну[ред. | ред. код]
Виявлення[ред. | ред. код]
Нагрівання цистеїну або білку із діацетатом свинцю у лужному середовищі супроводжується утворенням чорного осаду сульфіду свинцю Таку саму реакцію дає метіонін. Метіонін більш стійкий і при слабкому лужному гідролізі не руйнується.
При взаємодії цистеїну із лугом утворюється діаніон, у якому є три нуклеофільних центри: Те саме відбувається із серином, однак у цьому випадку у діаніоні наявні інші нуклеофільні центри: Нуклеофіли тіолят-аніон (цистеїн) та фенолят-аніон (серин) реагують із молекулою диметилсульфату.
Якщо розчин білку прокип'ятити із лугом та після охолодження додати свіжоприготовлений розчин нітропрусиду натрію (), рідина забарвлюється у червоний колір.
Дерацемація (R,S)-цистеїну[ред. | ред. код]
Дерацемація може бути здійсненою за наступною схемою. Спочатку (R,S)-цистеїн (1) дією ацетону у оцтовій кислоті перетворюють у 2,2-диметилазолідин-4-карбонову кислоту (2), які потім нагрівають із (R,R)-винною кислотою у присутності саліцилового альдегіду. При цьому з розчину кристалізується сіль, гідроліз якої приводить до (S)-цистеїну.

Див. також[ред. | ред. код]
Примітки[ред. | ред. код]
- ↑ Архівована копія. Архів оригіналу за 10 листопада 2016. Процитовано 3 травня 2012.
{{cite web}}: Обслуговування CS1: Сторінки з текстом «archived copy» як значення параметру title (посилання) - ↑ Н. Давиденко, Є. Ковальчук, М. Гладиш. Синтез функціоналізованих наночастинок срібла[недоступне посилання з липня 2019] // Вісник Львівського університету. Серія хімічна. — 2011, Випуск 52[недоступне посилання з липня 2019]. С.: 352—357. ISSN 2078-5615.
Література[ред. | ред. код]
- Фармацевтична хімія : [арх. 11 березня 2021] : підручник / ред. П. О. Безуглий. — Вінниця : Нова Книга, 2008. — 560 с. — ISBN 978-966-382-113-9. (С.?)

|
Це незавершена стаття з хімії. Ви можете допомогти проєкту, виправивши або дописавши її. |
| |||||||||||





