Інженерія нервової тканини: відмінності між версіями
| [неперевірена версія] | [неперевірена версія] |
мНемає опису редагування |
|||
| Рядок 70: | Рядок 70: | ||
Було показано, що успіх включення 3D каркасів у ЦНС залежить від стадії, на якій клітини [[Диференціація клітин|диференціювалися]]. Пізніші стадії забезпечують більш ефективну імплантацію, тоді як клітини на більш ранніх стадіях повинні бути піддані впливу факторів, які змушують клітини диференціюватись і, таким чином, належним чином реагувати на сигнали, які клітини отримуватимуть у місці пошкодження ЦНС. <ref name="Sheen">{{Cite journal|last=Sheen|first=V. L.|last2=Arnold, M. W.|last3=Wang, Y.|last4=Macklis, J. D.|date=July 1999|title=Neural precursor differentiation following transplantation into neocortex is dependent on intrinsic developmental state and receptor competence|journal=Experimental Neurology|volume=158|issue=1|pages=47–62|doi=10.1006/exnr.1999.7104|pmid=10448417}}</ref> [[BDNF|Нейротрофічний фактор, отриманий з мозку,]] є потенційним кофактором для сприяння функціональній активації нейронів, отриманих з клітин ES, у місцях пошкодження ЦНС. <ref name="Copi">{{Cite journal|last=Copi|first=A|last2=Jungling, K.|last3=Gottmann, K.|date=November 2005|title=Activity- and BDNF-induced plasticity of miniature synaptic currents in ES cell-derived neurons integrated in a neocortical network|journal=Journal of Neurophysiology|volume=94|issue=6|pages=4538–43|doi=10.1152/jn.00155.2005|pmid=16293594}}</ref> |
Було показано, що успіх включення 3D каркасів у ЦНС залежить від стадії, на якій клітини [[Диференціація клітин|диференціювалися]]. Пізніші стадії забезпечують більш ефективну імплантацію, тоді як клітини на більш ранніх стадіях повинні бути піддані впливу факторів, які змушують клітини диференціюватись і, таким чином, належним чином реагувати на сигнали, які клітини отримуватимуть у місці пошкодження ЦНС. <ref name="Sheen">{{Cite journal|last=Sheen|first=V. L.|last2=Arnold, M. W.|last3=Wang, Y.|last4=Macklis, J. D.|date=July 1999|title=Neural precursor differentiation following transplantation into neocortex is dependent on intrinsic developmental state and receptor competence|journal=Experimental Neurology|volume=158|issue=1|pages=47–62|doi=10.1006/exnr.1999.7104|pmid=10448417}}</ref> [[BDNF|Нейротрофічний фактор, отриманий з мозку,]] є потенційним кофактором для сприяння функціональній активації нейронів, отриманих з клітин ES, у місцях пошкодження ЦНС. <ref name="Copi">{{Cite journal|last=Copi|first=A|last2=Jungling, K.|last3=Gottmann, K.|date=November 2005|title=Activity- and BDNF-induced plasticity of miniature synaptic currents in ES cell-derived neurons integrated in a neocortical network|journal=Journal of Neurophysiology|volume=94|issue=6|pages=4538–43|doi=10.1152/jn.00155.2005|pmid=16293594}}</ref> |
||
=== Дослідження ''in vivo'' === |
|||
Трансплантація кортикальних стовбурових клітин показала багатообіцяючий потенціал для відновлення мозку. Однак ефективність сучасних моделей трансплантації в кодуванні корисної функції для хазяїна через отримані від трансплантації нейрони все ще обмежена. Це пояснюється відсутністю деяких типів клітин у трансплантатах, аномальними пропорціями типів клітин, аномальною цитоархітектурою та неефективною [[Васкулогенез|васкуляризацією]]. |
|||
Щоб усунути ці обмеження, була розроблена платформа трансплантації для тестування прототипів неокортикальної тканини<ref>{{Cite web|url=https://www.mdpi.com/2306-5354/10/2/263|title=An In Vivo Platform for Rebuilding Functional Neocortical Tissue|last=Quezada Alexandra, Claire Ward, Edward R. Bader, Pavlo Zolotavin, Esra Altun, Sarah Hong, Nathaniel J. Killian, Chong Xie, Renata Batista-Brito, and Jean M. Hébert.|date=16 Лютого 2023|publisher=Bioengineering|language=eng|doi=10.3390/bioengineering10020263}}</ref>. Платформа включала трансплантацію дисоційованих мишачих ембріональних теленцефальних клітин у рідкому каркасі в уражену аспірацією кору кори дорослої миші. Попередники донорських нейронів диференціювалися на нейрони верхнього та глибокого шарів, які демонстрували синаптичні точки, проектувалися за межі трансплантата у відповідні ділянки мозку, ставали електрофізіологічно активними протягом одного місяця після трансплантації та реагували на візуальні стимули. [[Інтернейрони]] та [[Олігодендроцит|олігодендроцити]] були присутні в трансплантатах з нормальною щільністю. |
|||
Трансплантати повністю васкуляризувалися через тиждень після трансплантації. Клітини також були організовані в шари. Ця платформа ''in vivo'' пропонує підтвердження концепції розробки та тестування прототипів тканин, схожих на [[Неокортекс|неокорку]], які можуть мати наслідки для відновлення мозку та [[Регенеративна медицина|регенеративної медицини]]. |
|||
== Периферична нервова система (ПНС) == |
== Периферична нервова система (ПНС) == |
||
| Рядок 120: | Рядок 127: | ||
* [https://onlinelibrary.wiley.com/doi/full/10.1002/EXP.20210035 Neural tissue engineering: From bioactive scaffolds and in situ monitoring to regeneration — B. Gong et al. (2022)] |
* [https://onlinelibrary.wiley.com/doi/full/10.1002/EXP.20210035 Neural tissue engineering: From bioactive scaffolds and in situ monitoring to regeneration — B. Gong et al. (2022)] |
||
* [https://www.mdpi.com/2079-4983/13/3/146/pdf Tissue-Engineered Models of the Human Brain: State-of-the-Art Analysis and Challenges (review, pdf) — G. Tarricone et al. (2022)] |
* [https://www.mdpi.com/2079-4983/13/3/146/pdf Tissue-Engineered Models of the Human Brain: State-of-the-Art Analysis and Challenges (review, pdf) — G. Tarricone et al. (2022)] |
||
* [[doi:10.3390/bioengineering10020263|An In Vivo Platform for Rebuilding Functional Neocortical Tissue — Quezada A, Ward C, Bader ER, Zolotavin P, Altun E, Hong S, Killian NJ, Xie C, Batista-Brito R, Hébert JM. (2023)]] |
|||
== Примітки == |
== Примітки == |
||
Версія за 10:55, 20 лютого 2023
Інженерія нервової тканини (або нейротканинна інженерія) — це галузь тканинної інженерії, яка зосереджена на розробці функціональних замінників нервової тканини для заміни або відновлення пошкодженої або хворої тканини центральної нервової системи (ЦНС) або периферичної нервової системи (ПНС). Метою інженерії нервової тканини є відновлення втраченої функції нервової системи за допомогою матеріалів, клітин і факторів росту.[2][3]
Ця область дослідження включає в себе принципи матеріалознавства, біології та інженерії для проектування та розробки пристроїв, каркасів і 3D-культур, які сприяють росту, виживанню та функціональній інтеграції нейронів і гліальних клітин. Деякі із застосувань нейротканинної інженерії включають лікування травм спинного мозку, черепно-мозкових травм, інсульту, хвороби Паркінсона та інших станів, які призводять до пошкодження нервової системи.
Розвиток нейротканинної інженерії потребує міждисциплінарного підходу, який передбачає співпрацю між інженерами, неврологами та клініцистами для перетворення лабораторних результатів у клінічне застосування.
Огляд
Нервова система поділяється на два відділи: ЦНС і ПНС. ЦНС складається з головного та спинного мозку, тоді як ПНС складається з нервів, які походять від головного та спинного мозку та іннервують решту тіла.[4]
Потреба в інженерії нервової тканини, як окремої галузі, виникає через складність нервових клітин і нервової тканини відновлюватися самостійно після пошкодження нервової системи. ПНС має певну, але обмежену регенерацію нервових клітин. Було виявлено, що нейрогенез дорослих стовбурових клітин у ЦНС відбувається в гіпокампі, субвентрикулярній зоні (SVZ) і спинному мозку.[5]
Пошкодження ЦНС можуть бути викликані інсультом, нейродегенеративними розладами, травмою або енцефалопатією. Нині досліджуються кілька методів лікування пошкоджень ЦНС[6]:
- імплантація стовбурових клітин безпосередньо в місце пошкодження
- доставка морфогенів до місця пошкодження
- вирощування нервової тканини in vitro з нейронними стовбуровими або клітинами-попередниками в 3D каркасі.
Запропоноване використання електропрядених полімерних волокнистих каркасів для нейронних субстратів відновлення датується щонайменше 1986 роком у заявці NIH SBIR від Simon.[7]
Для ПНС відірваний нерв можна повторно з’єднати та повторно іннервувати за допомогою трансплантатів або спрямування існуючого нерва через канал.[4]
Нещодавні дослідження створення мініатюрної кори головного мозку, відомої як кортикопоез, і моделей мозку, відомих як церебральні органоїди, є методами, які можуть сприяти розвитку регенерації нервової тканини. Природні кортикальні попередники кортикопоезу — це нервові тканини, які можуть бути ефективно вбудовані в мозок.[8]
Церебральні органоїди — це тривимірні плюрипотентні стовбурові клітини людини, розвинені в секції кори головного мозку, що свідчить про наявність потенціалу для ізоляції та розвитку певних нервових тканин за допомогою нейронних попередників.[9]
Іншою ситуацією, що вимагає імплантації чужорідної тканини, є використання записуючих електродів. Хронічні електродні імплантати – це інструмент, який використовується в дослідницьких програмах для запису сигналів із областей кори головного мозку . Дослідження стимуляції нейронів ПНС у пацієнтів з паралічем і протезуванням може розширити знання про реіннервацію нервової тканини як у ПНС, так і в ЦНС. Це дослідження здатне зробити один складний аспект інженерії нервової тканини — функціональну іннервацію нервової тканини — більш керованою.[10]
Центральна нервова система (ЦНС)
Причини ураження ЦНС
Є три основні причини ураження ЦНС: інсульт, черепно-мозкова травма (ЧМТ) або ускладнення розвитку. Інсульти класифікуються як геморагічні (коли судина пошкоджена до ступеня крововиливу в мозок) або ішемічні (коли тромб блокує кровотік через судину в мозку). Коли відбувається крововилив, кров просочується в навколишні тканини, що призводить до відмирання тканин, тоді як ішемічні крововиливи призводять до відсутності кровотоку до певних тканин. Черепно-мозкова травма викликається зовнішніми силами, що впливають на череп або спинний мозок. Проблеми з розвитком ЦНС призводять до аномального росту тканин під час розвитку, таким чином знижуючи функцію ЦНС. [6]
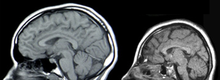
Лікування та дослідження ЦНС
Імплантація стовбурових клітин на місце пошкодження

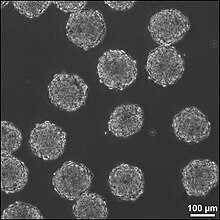
Один із потенційних методів лікування ураження ЦНС включає культивування стовбурових клітин in vitro та імплантацію їх у місце ураження мозку. Імплантація стовбурових клітин безпосередньо в місце пошкодження запобігає утворенню гліальних рубців і сприяє нейрогенезу, що походить від пацієнта, але також створює деякі ризики — ризик розвитку пухлини, запалення та міграції стовбурових клітин з місця пошкодження. Пухлиноутворення може виникнути через неконтрольований характер диференціації стовбурових клітин, запалення може виникнути через відторгнення імплантованих клітин клітинами-господарями, а висока міграційна природа стовбурових клітин призводить до того, що клітини віддаляються від місця пошкодження, тому не надає бажаний вплив на місце пошкодження.
Інші проблеми інженерії нервової тканини включають створення безпечних джерел стовбурових клітин і отримання відтворюваних результатів від лікування до лікування.[6]
Крім того, ці стовбурові клітини можуть діяти як носії для інших методів лікування, хоча позитивні ефекти використання стовбурових клітин як механізму доставки не підтверджені. Пряма доставка стовбурових клітин має підвищений корисний ефект, якщо вони запрограмовані як нейронні клітини in vitro.[6]
Доставка молекул до місця пошкодження
Молекули, які сприяють регенерації нервової тканини, включаючи фармацевтичні препарати, фактори росту, відомі як морфогени, і мікроРНК також можуть бути безпосередньо введені в місце пошкодження пошкодженої тканини ЦНС.
Нейрогенез спостерігався також у тварин, яких лікували психотропними препаратами, через пригнічення зворотного захоплення серотоніну та індукцію нейрогенезу в мозку.
Коли стовбурові клітини диференціюються, клітини виділяють морфогени, такі як фактори росту, щоб сприяти здоровому розвитку. Ці морфогени допомагають підтримувати гомеостаз і нейронні сигнальні шляхи, і вони можуть бути доставлені в місце пошкодження для сприяння росту пошкоджених тканин. В даний час доставка морфогену має мінімальні переваги через взаємодію морфогенів з ушкодженою тканиною. Щоб лікування було ефективним, морфогени повинні бути присутніми в місці пошкодження в певній і постійній концентрації.
Було також показано, що мікроРНК впливає на нейрогенез, керуючи диференціюванням недиференційованих нейронних клітин.[6]
Імплантація нервової тканини, розробленої in vitro
Третій метод лікування пошкоджень ЦНС полягає у штучному створенні тканини поза тілом для імплантації в місце пошкодження. Цей метод може лікувати травми, які складаються з великих порожнин, де більша кількість нервової тканини потребує заміни та регенерації. Нервова тканина вирощується in vitro з нейронними стовбуровими клітинами або клітинами-попередниками в 3D каркасі, утворюючи ембріоїдні тіла. Ці ембріоїдні тіла складаються зі сфери стовбурових клітин, де внутрішні клітини є недиференційованими нервовими клітинами, а навколишні клітини стають все більш диференційованими. Тривимірні каркаси використовуються для трансплантації тканини до місця пошкодження та створення відповідного інтерфейсу між штучною та тканиною мозку.
Каркаси мають бути: біосумісними, біологічно розкладаними, відповідати за розміром та формою місцю пошкодження, подібними до існуючої тканини за еластичністю та жорсткістю та підтримувати зростання клітин і тканин.
Поєднання використання спрямованих стовбурових клітин і каркасів для підтримки нервових клітин і тканин збільшує виживання стовбурових клітин у місці пошкодження, підвищуючи ефективність лікування.[6]

Існує 6 різних типів каркасів, які досліджуються для використання в цьому методі лікування ушкоджень нервової тканини:
- Рідкі гідрогелі — це зшиті гідрофобні полімерні ланцюги, в яких нейронні стовбурові клітини вирощуються на поверхні гелю або інтегруються в гель під час зшивання полімерних ланцюгів. Основним недоліком рідких гідрогелів є обмежений захист клітин, які трансплантуються.
- Підтримуючі каркаси (Supportive scaffolds) — виготовлені з твердих кулькоподібних або мікропористих структур і можуть діяти як носії для трансплантованих клітин або факторів росту, які стовбурові клітини виділяють під час диференціювання. Клітини прилипають до поверхні матриці двовимірними шарами. Підтримуючі каркаси легко трансплантуються в місце пошкодження головного мозку через розміри скаффолдів. Вони забезпечують матрицю, що сприяє клітинній адгезії та агрегації, таким чином збільшуючи культуру здорових клітин.
- Каркаси для вирівнювання (Aligning scaffolds) — можуть бути на основі шовку, полісахаридів або на основі інших матеріалів, таких як багатий колагеном гідрогель. Ці гелі тепер покращені мікровізерунками на поверхні для сприяння розвитку нейронних відростків. Ці каркаси в основному використовуються для регенерації, яка має відбуватися в певній орієнтації, наприклад, при травмах спинного мозку.
- Інтегративні каркаси — в основному використовуються для захисту трансплантованих клітин від механічних пошкоджень, яким вони піддаються в процесі імплантації в місце пошкодження. Ці каркаси також зменшують ймовірність того, що запальні клітини, розташовані в місці пошкодження, мігрують у каркас зі стовбуровими клітинами. Помічено, що кровоносні судини проростають через каркас, таким чином каркас і клітини інтегруються в тканину господаря.
- Комбінація сконструйованих каркасів представляє варіант 3D-каркасу, який може мати як необхідні візерунки для адгезії клітин, так і гнучкість для адаптації до постійно мінливого середовища в місці пошкодження.
- Децелюляризовані каркаси ECM є варіантом для каркасів, оскільки вони більш точно імітують нативну тканину, але наразі ці каркаси можна зібрати лише з ампутацій і трупів.[6]
Ці тривимірні каркаси можуть бути виготовлені за допомогою методів вилуговування частинок, газового спінювання, з’єднання волокон, лиття з розчинника або електроформування; кожна техніка створює каркас із властивостями, відмінними від інших технік.[11]
Було показано, що успіх включення 3D каркасів у ЦНС залежить від стадії, на якій клітини диференціювалися. Пізніші стадії забезпечують більш ефективну імплантацію, тоді як клітини на більш ранніх стадіях повинні бути піддані впливу факторів, які змушують клітини диференціюватись і, таким чином, належним чином реагувати на сигнали, які клітини отримуватимуть у місці пошкодження ЦНС. [12] Нейротрофічний фактор, отриманий з мозку, є потенційним кофактором для сприяння функціональній активації нейронів, отриманих з клітин ES, у місцях пошкодження ЦНС. [13]
Дослідження in vivo
Трансплантація кортикальних стовбурових клітин показала багатообіцяючий потенціал для відновлення мозку. Однак ефективність сучасних моделей трансплантації в кодуванні корисної функції для хазяїна через отримані від трансплантації нейрони все ще обмежена. Це пояснюється відсутністю деяких типів клітин у трансплантатах, аномальними пропорціями типів клітин, аномальною цитоархітектурою та неефективною васкуляризацією.
Щоб усунути ці обмеження, була розроблена платформа трансплантації для тестування прототипів неокортикальної тканини[14]. Платформа включала трансплантацію дисоційованих мишачих ембріональних теленцефальних клітин у рідкому каркасі в уражену аспірацією кору кори дорослої миші. Попередники донорських нейронів диференціювалися на нейрони верхнього та глибокого шарів, які демонстрували синаптичні точки, проектувалися за межі трансплантата у відповідні ділянки мозку, ставали електрофізіологічно активними протягом одного місяця після трансплантації та реагували на візуальні стимули. Інтернейрони та олігодендроцити були присутні в трансплантатах з нормальною щільністю.
Трансплантати повністю васкуляризувалися через тиждень після трансплантації. Клітини також були організовані в шари. Ця платформа in vivo пропонує підтвердження концепції розробки та тестування прототипів тканин, схожих на неокорку, які можуть мати наслідки для відновлення мозку та регенеративної медицини.
Периферична нервова система (ПНС)
Причини ураження ПНС
Травма ПНС може спричинити таке серйозне пошкодження, як розрив нерва, розщеплення нерва на проксимальну та дистальну частини. Дистальний нерв з часом дегенерує через бездіяльність, тоді як проксимальний кінець з часом набрякає. Дистальний кінець не дегенерує відразу, а набряк проксимального кінця не робить його нефункціональним, тому досліджуються методи відновлення зв’язку між двома кінцями нерва.[4]
Лікування та дослідження ПНС
Хірургічне з'єднання
Одним із методів лікування пошкодження ПНС є хірургічне відновлення відірваного нерва шляхом взяття двох кінців нерва та їх зшивання. Під час зшивання нервів кожен пучок нерва знову з’єднується, з’єднуючи нерв разом. Хоча цей метод працює для розривів, які створюють невеликий проміжок між проксимальним і дистальним закінченнями нервів, цей метод не працює на проміжках більшої відстані через напругу, яку необхідно застосувати до нервових закінчень. Ця напруга призводить до дегенерації нерва, і тому нерв не може відновитися та сформувати функціональний нейронний зв’язок.[4]
Пересадки тканин
Тканинні трансплантати використовують нерви або інші матеріали для з'єднання двох кінців відірваного нерва. Існує три категорії тканинних трансплантатів: трансплантати аутологічної тканини, трансплантати неавтологічної тканини та ацелюлярні трансплантати.
- Трансплантати аутологічної тканини пересаджують нерви з іншої частини тіла пацієнта, щоб заповнити проміжок між обома кінцями пошкодженого нерва. Ці нерви, як правило, є шкірними нервами, але й інші нерви були досліджені з обнадійливими результатами. Ці аутологічні нервові трансплантати є поточним золотим стандартом для трансплантації нервів ПНС через високу біосумісність аутологічних трансплантатів нервів, але існують проблеми щодо вилучення нерва у самих пацієнтів і можливості зберігати велику кількість аутологічних трансплантатів на майбутнє використовування.
- Неавтологічні та ацелюлярні трансплантати (включаючи матеріали на основі позаклітинного матриксу) — це тканини, які не походять від пацієнта, а можуть бути зібрані з трупів (відомі як алогенні тканини) або тварин (відомі як ксеногенні тканини). Хоча ці тканини мають перевагу перед аутологічними тканинними трансплантатами, оскільки тканину не потрібно брати у пацієнта, виникають труднощі з потенційною передачею захворювання та, отже, імуногенними проблемами. Наразі досліджуються методи усунення імуногенних клітин, залишаючи позаклітинно-матричні-компоненти тканини, щоб підвищити ефективність трансплантатів неаутологічної тканини.[4]
Наведення
Методи керування регенерацією ПНС використовують нервові направляючі канали, щоб допомогти аксонам відновити правильний шлях, і можуть спрямовувати фактори росту, що виділяються обома кінцями нерва, для сприяння росту та повторному з’єднанню. Методи наведення зменшують утворення рубців на нервах, збільшуючи функціональність нервів для передачі потенціалів дії після повторного підключення. У керівних методах регенерації ПНС використовуються два види матеріалів: натуральні та синтетичні.[15]
- Матеріали на натуральній основі – це модифіковані каркаси, що походять від компонентів позаклітинного матриксу і глікозаміногліканів. Ламінін, колаген і фібронектин, які є компонентами позаклітинного матриксу, направляють розвиток аксонів і сприяють нервовій стимуляції та активності. Інші молекули, які можуть сприяти відновленню нервів, це: гіалуронова кислота, фібриноген, фібринові гелі, самозбірні пептидні каркаси, альгінат, агароза та хітозан.
- Синтетичні матеріали забезпечують метод регенерації тканин, за допомогою якого можна контролювати хімічні та фізичні властивості трансплантата. Оскільки властивості матеріалу можуть бути визначені для ситуації, в якій він використовується, синтетичні матеріали є привабливим варіантом для регенерації ПНС. Використання синтетичних матеріалів пов’язане з певними проблемами, такими як: формування матеріалу трансплантата до необхідних розмірів, здатність до біологічного розкладання, стерилізація, стійкість до розривів, легкість у роботі, низький ризик інфікування та низька реакція на запалення завдяки матеріалу. Матеріал також повинен підтримувати канал під час регенерації нерва. В даний час найбільш часто досліджувані матеріали зосереджені на поліефірах, але також досліджуються біорозкладаний поліуретан, інші полімери та біорозкладне скло . Іншими можливостями для синтетичних матеріалів є електропровідні полімери та полімери, біологічно модифіковані для сприяння росту аксонів клітин і підтримки аксонного каналу.[4]
Пов'язані дослідження
Моделювання розвитку тканин мозку in vitro
Двома моделями розвитку тканин мозку є церебральні органоїди та кортикопоез.
Ці моделі забезпечують «in vitro» модель нормального розвитку мозку [9], але ними можна маніпулювати, щоб дослідити нейронні дефекти. Таким чином, дослідники можуть вивчати механізми здорового та неправильного розвитку за допомогою цих моделей. [9] Ці тканини можна виготовити або з мишачих ембріональних стовбурових клітин (ЕСК), або з людських. Мишачі ЕСК культивують у білку, який називається 'інгібітор Sonic Hedgehog', щоб сприяти розвитку дорсального переднього мозку та вивчати долю кори.[8] Показано, що цей метод створює аксональні шари, які імітують широкий спектр кортикальних шарів.[9] Тканини, отримані з ЕСК людини, використовують плюрипотентні стовбурові клітини для формування тканин на каркасі, утворюючи людські ембріоїдні тіла. Ці тканини, отримані з ЕСК людини, утворюються шляхом культивування плюрипотентних ембріоїдних тіл людини в обертовому біореакторі. [9]
Цілеспрямована реіннервація
Цілеспрямована реіннервація (Targeted reinnervation) — це метод реіннервації нейронних зв’язків у ЦНС та ПНС, зокрема у паралізованих пацієнтів та осіб з ампутованими кінцівками, які використовують протези кінцівок. Зараз досліджуються пристрої, які сприймають і записують електричні сигнали, що поширюються через нейрони у відповідь на намір людини рухатися. Це дослідження може пролити світло на те, як реіннервувати нейронні зв’язки між розірваними нервами ПНС і зв’язки між пересадженими 3D каркасами в ЦНС. [10]
Див.також
Посилання
- Can the damaged brain repair itself? — Siddharthan Chandran. TED (2013)
- Biomaterials for Neural Tissue Engineering — L.R. Doblado et al. (2021)
- Neural tissue engineering: From bioactive scaffolds and in situ monitoring to regeneration — B. Gong et al. (2022)
- Tissue-Engineered Models of the Human Brain: State-of-the-Art Analysis and Challenges (review, pdf) — G. Tarricone et al. (2022)
- An In Vivo Platform for Rebuilding Functional Neocortical Tissue — Quezada A, Ward C, Bader ER, Zolotavin P, Altun E, Hong S, Killian NJ, Xie C, Batista-Brito R, Hébert JM. (2023)
Примітки
- ↑ Doerr, Jonas; Schwarz, Martin Karl; Wiedermann, Dirk; Leinhaas, Anke; Jakobs, Alina; Schloen, Florian; Schwarz, Inna; Diedenhofen, Michael; Braun, Nils Christian (19 січня 2017). Whole-brain 3D mapping of human neural transplant innervation. Nature Communications (англ.). Т. 8, № 1. с. 14162. doi:10.1038/ncomms14162. ISSN 2041-1723. Процитовано 11 лютого 2023.
- ↑ Giulia Tarricone, Irene Carmagnola, and Valeria Chiono (2022). Tissue-Engineered Models of the Human Brain: State-of-the-Art Analysis and Challenges. https://doi.org/10.3390/jfb13030146 (eng) . Journal of Functional Biomaterials 13, 146.
- ↑ Doblado, Laura Rodríguez; Martínez-Ramos, Cristina; Pradas, Manuel Monleón (2021). Biomaterials for Neural Tissue Engineering. Frontiers in Nanotechnology. Т. 3. doi:10.3389/fnano.2021.643507/full. ISSN 2673-3013. Процитовано 14 лютого 2023.
{{cite news}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ а б в г д е Schmidt, Christine E.; Leach, Jennie Baier (2003-08). Neural Tissue Engineering: Strategies for Repair and Regeneration. Annual Review of Biomedical Engineering (англ.). Т. 5, № 1. с. 293—347. doi:10.1146/annurev.bioeng.5.011303.120731. ISSN 1523-9829. Процитовано 11 лютого 2023.
- ↑ Temple, Sally (November 2001). The development of neural stem cells. Nature. 414 (6859): 112—117. Bibcode:2001Natur.414..112T. doi:10.1038/35102174. PMID 11689956.
- ↑ а б в г д е ж Forraz, N; Wright, Ke; Jurga, M; McGuckin, Cp (2013-07). Experimental therapies for repair of the central nervous system: stem cells and tissue engineering: Experimental therapies: brain tissue engineering. Journal of Tissue Engineering and Regenerative Medicine (англ.). Т. 7, № 7. с. 523—536. doi:10.1002/term.552. Процитовано 11 лютого 2023.
- ↑ Simon, Eric M. (1986). NIH SBIR PHASE I GRANT APPLICATION: FIBROUS SUBSTRATES FOR CELL CULTURE (PDF Download Available). ResearchGate (англ.). Процитовано 22 травня 2017.
- ↑ а б Gaspard, Nicolas; Gaillard, Afsaneh; Vanderhaeghen, Pierre (15 серпня 2009). Making cortex in a dish: In vitro corticopoiesis from embryonic stem cells. Cell Cycle. Т. 8, № 16. с. 2491—2496. doi:10.4161/cc.8.16.9276. ISSN 1538-4101. PMID 19597331. Процитовано 11 лютого 2023.
- ↑ а б в г д Lancaster, Madeline A.; Renner, Magdalena; Martin, Carol-Anne; Wenzel, Daniel; Bicknell, Louise S.; Hurles, Matthew E.; Homfray, Tessa; Penninger, Josef M.; Jackson, Andrew P. (2013-09). Cerebral organoids model human brain development and microcephaly. Nature (англ.). Т. 501, № 7467. с. 373—379. doi:10.1038/nature12517. ISSN 1476-4687. Процитовано 11 лютого 2023.
- ↑ а б Tenore, Francesco; Vogelstein, Jacob (2011). Revolutionizing Prothetics: Devices for Neural Integration. Johns Hopkins APL Technical Digest. 30 (3): 230—39.
- ↑ Ko, J; Mohtaram NK; Ahmed F та ін. (September 2013). Fabrication of poly (ϵ-caprolactone) microfiber scaffolds with varying topography and mechanical properties for stem cell-based tissue engineering applications. Journal of Biomaterials Science, Polymer Edition. 25 (1): 1—17. doi:10.1080/09205063.2013.830913. PMID 23998440.
{{cite journal}}:|hdl-access=вимагає|hdl=(довідка) - ↑ Sheen, V. L.; Arnold, M. W.; Wang, Y.; Macklis, J. D. (July 1999). Neural precursor differentiation following transplantation into neocortex is dependent on intrinsic developmental state and receptor competence. Experimental Neurology. 158 (1): 47—62. doi:10.1006/exnr.1999.7104. PMID 10448417.
- ↑ Copi, A; Jungling, K.; Gottmann, K. (November 2005). Activity- and BDNF-induced plasticity of miniature synaptic currents in ES cell-derived neurons integrated in a neocortical network. Journal of Neurophysiology. 94 (6): 4538—43. doi:10.1152/jn.00155.2005. PMID 16293594.
- ↑ Quezada Alexandra, Claire Ward, Edward R. Bader, Pavlo Zolotavin, Esra Altun, Sarah Hong, Nathaniel J. Killian, Chong Xie, Renata Batista-Brito, and Jean M. Hébert. (16 Лютого 2023). An In Vivo Platform for Rebuilding Functional Neocortical Tissue (eng) . Bioengineering. doi:10.3390/bioengineering10020263.
{{cite web}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ Gong, Bowen; Zhang, Xindan; Zahrani, Ahmed Al; Gao, Wenwen; Ma, Guolin; Zhang, Liqun; Xue, Jiajia (2022-06). Neural tissue engineering: From bioactive scaffolds and in situ monitoring to regeneration. Exploration (англ.). Т. 2, № 3. с. 20210035. doi:10.1002/EXP.20210035. ISSN 2766-2098. Процитовано 14 лютого 2023.