Молекулярна медицина: відмінності між версіями
| [неперевірена версія] | [неперевірена версія] |
Alessot (обговорення | внесок) Заміна прямого міжмовного посилання на {{iw}} |
Оновлено, Доповнено |
||
| Рядок 1: | Рядок 1: | ||
[[Файл:CRISPR illustration gif animation 1.gif|альт=Фрагмент відео «Новий пристрій на базі CRISPR виявляє генетичні мутації за лічені хвилини»|міні| |
[[Файл:CRISPR illustration gif animation 1.gif|альт=Фрагмент відео «Новий пристрій на базі CRISPR виявляє генетичні мутації за лічені хвилини»|міні|[[Редагування генома]] технологією [[CRISPR/cas9|CRISPR/Cas9]]]] |
||
'''Молекулярна медицина'''<ref>{{Cite book |
'''Молекулярна медицина'''<ref>{{Cite book |
||
|title=Molecular Medicine: How Science Works |
|title=Molecular Medicine: How Science Works |
||
| Рядок 9: | Рядок 9: | ||
|doi=10.1007/978-3-031-27133-5 |
|doi=10.1007/978-3-031-27133-5 |
||
|isbn=978-3-031-27132-8 |
|isbn=978-3-031-27132-8 |
||
}}</ref> — це міждисциплінарна галузь [[Медицина|медицини]] й [[Охорона здоров'я|охорони здоров’я]], зосереджена на розумінні та застосуванні молекулярних процесів для [[Діагностика (медицина)|діагностики]], [[лікування]] та [[Профілактика (медицина)|профілактики]] [[Захворювання|захворювань]]. Вона охоплює вивчення біологічних механізмів на [[Молекулярна біологія|молекулярному]] рівні, об’єднуючи принципи з різних [[Наукова дисципліна|дисциплін]], таких як [[біологія]], [[генетика]], [[біохімія]], [[біомедицина]], [[біотехнологія]] та [[біоінженерія]]. |
|||
}}</ref> — сукупність сучасних методів корекції [[Патологічний стан|патологічних станів]] [[Організм людини|організму]] за допомогою молекулярних агентів, наприклад систем [[Генотерапія|редагування геному]] та [[наномедицина]].{{Джерело}} |
|||
Молекулярна медицина досліджує, як [[Молекула|молекули]] взаємодіють у [[Клітина|клітинах]] і [[Організм|організмах]], розгадуючи заплутані шляхи, що лежать в основі [[Здоров'я|здоров’я]] та хвороб. Розшифровуючи молекулярну основу захворювань, біомедичні [[Науковець|науковці]] та [[Дослідник|дослідники]] можуть розробляти цільову терапію, [[Персоналізована медицина|персоналізовані]] підходи до медицини та інноваційні діагностичні інструменти. |
|||
== Історія == |
|||
У 1855 році німецький лікар і вчений [[Рудольф Вірхов]], один із засновників [[Клітинна теорія|клітинної теорії]] у [[Біологія|біології]] і [[Медицина|медицині]], ввів поняття «<nowiki/>[[Целюлярна патологія|целюлярної патології]]<nowiki/>», згідно з яким будь-яка [[хвороба]] може бути зведена до поразки відповідних [[Клітина|клітин]]<ref>{{Стаття|автор=Virchow, R.|тип=|том=8|номер=1|issn=|doi=10.1007/BF01935312}}</ref>. Реалізація даного принципу у практичній медицині до початку бурхливого розвитку [[Молекулярна біологія|молекулярної]] і [[Клітинна біологія|клітинної біології]] у XX віці була ускладнена відсутністю інструментів, специфічних до конкретних клітин та їхніх функцій. |
|||
Ця сфера відіграє ключову роль у розвитку охорони здоров’я завдяки використанню передових технологій, таких як [[оміксні технології]], [[біоінформатика]], [[Біосенсор|біосенсори]], [[генетична інженерія]]. За допомогою цих інструментів вчені можуть аналізувати [[геном]], структури [[Білки|білків]], широкий спектр [[Метаболіти|метаболітів]] і молекулярні сигнальні шляхи, що веде до глибшого розуміння захворювань на молекулярному рівні. |
|||
== Молекулярна хірургія = молекулярна медицина == |
|||
Хірургічні принципи, що об'єднані поняттям «функціональна хірургія»<ref>{{Cite news|title=Молекулярная и ферментативная функциональная хирургия будущего|url=https://istina.msu.ru/publications/article/53943257/|work=Альманах Института хирургии им. А.В. Вишневского|date=2017|accessdate=2020-04-27|pages=1514–1515|issue=1|language=ru|first=И. Д.|last=Клабуков|first2=П. Ю.|last2=Волчков|first3=А. В.|last3=Люндуп|first4=Т. Г.|last4=Дюжева|archive-date=8 травня 2021|archive-url=https://web.archive.org/web/20210508214529/https://istina.msu.ru/publications/article/53943257/}}</ref><ref>{{Cite web|url=https://papers.ssrn.com/sol3/papers.cfm?abstract_id=2943526|title=Foundations for Molecular Surgery|last=|first=Ilya Klabukov|date=30 березня 2017|website=|publisher=I.M. Sechenov First Moscow State Medical University|language=en|accessdate=27.04.2020|archive-date=19 липня 2018|archive-url=https://web.archive.org/web/20180719084016/https://papers.ssrn.com/sol3/papers.cfm?abstract_id=2943526}}</ref>, мають на меті виконання органозберігаючих операцій, частіше малоінвазивних, і направлених на корекцію систем організму при збереженні анатомії та відновленні нормальних функцій. У XX столітті прикладами реалізації таких принципів стали [[Лапароскопія|лапароскопічні техніки]], [[Роботизована хірургія|робот-асистовані операції]], методи [[Хірургія прискореної реабілітації|хірургії прискореної реабілітації]] (''ERAS'' або ''Fast Track Surgery'')<ref>{{Cite web|url=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5650458/|title=The application of enhanced recovery after surgery (ERAS)/fast-track surgery in gastrectomy for gastric cancer: a systematic review and meta-analysis|last=Jie Ding, Benlong Sun, Peng Song, Song Liu, Hong Chen, Min Feng|first=|date=2017 Jun 20|website=|publisher=|language=en|accessdate=27.04.2020}}</ref> та ін. Сучасна молекулярна біологія та [[біофізика]] дозволяє розширити ці приклади на виконання функціональних операцій також на молекулярному рівні<ref>Клабуков І. Д., Волчков П. ЗАГИНУ., Люндуп А. У., Дюжева Т. Г. Молекулярна і ферментативна функциональна хірургія майбутнього. Альманах Інституту хірургії ім. А. У. Вишневського. 2017. № S1. З. 1514—1515.</ref>. |
|||
== Загальні принципи == |
|||
Ідею хірургії на молекулярному рівні вперше висунув у 1959-му році нобелівський лауреат [[Річард Філіпс Фейнман|Річард Фейнман]] у лекції, прочитаній на засіданні [[Американське фізичне товариство|Американського фізичного товариства]], як приклад потенційного використання нанорозмірних механізмів у медичних цілях: «Ви вводите такого мініатюрного механічного хірурга до артерії, і він проникає до серця і обстежує його. Він помічає несправний клапан, підходить до нього та відсікає його мікроскальпелем»<ref>{{cite journal |
|||
Молекулярна медицина є наріжним каменем сучасної охорони здоров’я, заглиблюючись у складну сферу молекулярних і клітинних процесів, що керують життям. Ця дисципліна розкриває фундаментальні принципи молекулярної біології, досліджує молекулярні шляхи та об’єднує різноманітні наукові сфери, щоб розшифрувати механізми здоров’я та хвороби. |
|||
|author = Feynman, R. P. |
|||
|year = 1960 |
|||
|url = http://web.pa.msu.edu/people/yang/RFeynman_plentySpace.pdf |
|||
|title = There’s plenty of room at the bottom |
|||
|journal = Engineering and science |
|||
|language = en |
|||
|volume = 23 |
|||
|number = 5 |
|||
|pages = 22-36 |
|||
|accessdate = 18 квітня 2019 |
|||
|archive-date = 8 квітня 2019 |
|||
|archive-url = https://web.archive.org/web/20190408192131/https://web.pa.msu.edu/people/yang/RFeynman_plentySpace.pdf |
|||
}}</ref>. Надалі концепція втручань на молекулярному і тканинному рівні для зміни фенотипу тканин отримала своє інструментальне рішення у вигляді [[Генетична інженерія|генно-інженерних конструкцій]]. |
|||
=== Молекулярні та клітинні процеси === |
|||
Термін «молекулярна хірургія» вперше був сформульований у 1966 році для опису втручання у роботу клітин на рівні [[Дезоксирибонуклеїнова кислота|ДНК]]<ref>Denkewalter, R. G., & Tishler, M. (1966). [https://link.springer.com/chapter/10.1007%2F978-3-0348-7059-7_1 Drug research—whence and whither.] {{Webarchive|url=https://web.archive.org/web/20180611104026/https://link.springer.com/chapter/10.1007%2F978-3-0348-7059-7_1 |date=11 червня 2018 }} In Fortschritte der Arzneimittelforschung/Progress in Drug Research/Progrès des recherches pharmaceutiques (pp. 11-31). Birkhäuser Basel.</ref>. Розроблені останнім часом системи [[Редагування генома|редагування геному]] ([[CRISPR/cas9|CRISPR/Cas9]], {{iw|Transcription activator-like effector nuclease|TALEN|en|Transcription activator-like effector nuclease}}, ZFN) для терапевтичних цілей дозволяють відновлювати або відтворювати нормальний клітинний фенотип і, як наслідок, нормальний функціонал патологічно змінених тканин. У теперішню пору проходять випробування системи молекулярної хірургії для лікування [[Кардіоміопатія|кардіоміопатії]]<ref>Im, W., Moon, J., & Kim, M. (2016). Applications of CRISPR/Cas9 for Gene Editing in Hereditary Movement Disorders. ''Journal of Movement Disorders'', 9(3), 136.</ref>, [[Серпоподібноклітинна анемія|серпоподібноклітинної анемії]] та деяких онкологічних захворювань<ref>Ledford, H. (2015). CRISPR, the disruptor. ''Nature'', 522(7554), 20.</ref>. |
|||
==== Генетика та епігенетика ==== |
|||
=== Ферментативна хірургія === |
|||
[[Файл:Eukaryote_DNA-en.svg|міні|Схематичне зображення [[Дезоксирибонуклеїнова кислота|ДНК]] в [[Еукаріоти|еукаріотів]]: [[клітина]] — [[клітинне ядро]] — [[хромосома]] — ДНК.]] |
|||
Виправлення масштабних дефектів тканин є ціллю іншого напрямку — ферментативної хірургії ({{lang-en|enzymatic surgery}})<ref>Paterson, M. C., Bech-Hansen, N. T., & Smith, P. J. (1981). [https://link.springer.com/chapter/10.1007%2F978-1-4684-7956-0_40 Heritable radiosensitive and DNA repair-deficient disorders in] {{Webarchive|url=https://web.archive.org/web/20180602222848/https://link.springer.com/chapter/10.1007%2F978-1-4684-7956-0_40 |date=2 червня 2018 }} man. In Chromosome damage and repair (pp. 335—354). Springer US.</ref>. Хоча сьогодні ферменти в основному використовують для терапії захворювань органів травлення, але використання специфічних систем доставки дозволяє виконувати вплив зовсім іншого роду, наприклад масштабні втручання з ре-моделювання патологічно змінених тканин, у тому числі шляхом доставки [[Металопротеїни|металопротеїназ]] для руйнування [[Сполучна тканина|фіброзної тканини]], що розростається. Розвиток направлення ферментативної хірургії пов'язаний не тільки з ретельним підбором високоспецифічних засобів доставки (клітини, [[моноклональні антитіла]], одноланцюгові антитіла і їхні фрагменти), але також і з програмованим виводом та деактивацією токсичних продуктів, та їхньою подальшою утилізацією з допомогою наявних у організмі людини систем органів (печінка, шлунково-кишковий тракт, нирки, легені, потові залози). Ефективність і специфічність систем молекулярної та ферментативної хірургії пов'язані з вдосконаленням векторів доставки, а також можливостями з зовнішнього управління їхньої активності. Наприклад, високоспецифічна доставка до цільових тканин може здійснюватися за допомогою векторів на основі клітин, вірусних систем ([[Аденоасоційований вірус|AAV]], [[Вірус імунодефіциту людини|HIV]], [[Герпесвіруси|HSV]]), РНК-білкових комплексів, бактофекцій{{r|Тарантул2018|page=213}}, а зовнішнє керування — виконуватися методами [[Біофотоника|біофотоніки]] і {{нп|є=Optogenetics|треба=Оптогенетика|текст=оптогенетики}}<ref>Wu, X., Zhang, Y., Takle, K., Bilsel, O., Li, Z., Lee, H., … & Chan, E. M. (2016). Dye-sensitized core/active shell upconversion nanoparticles for optogenetics and bioimaging applications. ''ACS nano'', 10(1), 1060—1066. doi:10.1021/acsnano.5b06383</ref>. |
|||
У мікроскопічному світі [[Клітина|клітин]] [[нуклеїнові кислоти]] та [[білки]] є головними архітекторами, що керують клітинними процесами. Нуклеїнові кислоти, зокрема [[Дезоксирибонуклеїнова кислота|ДНК]] і [[Рибонуклеїнова кислота|РНК]], зберігають [[генетичний код]], тоді як білки виконують життєво важливі функції в клітинах. Ця взаємодія молекул формує основу життя. ДНК, основне сховище генетичної інформації, що міститься в [[Клітинне ядро|клітинному ядрі]], проходить низку процесів — [[Транскрипція (біологія)|транскрипції]] та [[Трансляція (біологія)|трансляції]], що завершується [[Біосинтез білків|синтезом білків]]. Ця [[Центральна догма молекулярної біології|центральна догма]] пояснює потік генетичної інформації в клітинах, керуючи їх поведінкою та функціями. Генетичний код, представлений [[Кодон|кодонами]], яким відповідають конкретні [[амінокислоти]], пояснює, як інструкції ДНК транслюються в білкові послідовності. Генетичні [[Мутація|мутації]], охоплюючі точкові мутації, вставки та делеції можуть порушити цей код, потенційно призводячи до аномальних білків і захворювань. Сукупність всієї генетичної інформації називаються [[геном]], [[геноміка]] досліджує весь геном організму, а [[медична генетика]] патолології геному [[Людина розумна|людини]]. Різні біотехнологічні й біомедичні методики, такі як [[генотерапія]] та [[Редагування генома|редагування геному]], дозволяють впливати на геном людини. |
|||
Крім того, активність певних генів регулюється різними механізмами, зокрема — [[Епігенетика|епігенетичними]]. Сукупність всіх епігенетичних надстроєк геному називається [[епігеном]]. [[Епігеноміка]] вивчає епігеном і практичні методики впливу на епігеном, такі як [[Епігенетичне перепрограмування|епігенетичне перерпрограмування]] та {{Не перекладено|Редагування епігеному|редагування епігеному|en|Epigenome editing}}. |
|||
== Перспективи == |
|||
Використання сукупності кодуючих ([[Дезоксирибонуклеїнова кислота|ДНК]], [[РНК]]) та сигнальних (білки і нуклеїнові кислоти) молекул з регуляції функціоналу організму для редагування геному та зміни клітинної організації дозволяє розглядати можливість персоналізації хірургічних втручань на основі «<nowiki/>[[Оміксні технології|оміксних]]<nowiki/>» даних організму пацієнта (геном, [[Транскрипція (біологія)|транскриптон]], [[метаболон]], [[Епігенетика|епігеном]]) для досягнення індивідуальної фізіологічної відповіді. Аналогічна високотехнологічна реалізація принципів функціональної молекулярної і ферментативної хірургії, враховуючи системи редагування [[Геном|геному]], тераностичних агентів ([[Англійська мова|англ.]] ''theranostic agent'' — які забезпечують як діагностику, так і лікування)<ref>{{Cite news|title=Nanoparticle-based theranostic agents|volume=62|first3=Xiaoyuan|last2=Lee|first2=Seulki|last=Xie|first=Jin|issue=11|pages=1064–1079|url=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2988080/|doi=10.1016/j.addr.2010.07.009|pmid=20691229|pmc=2988080|issn=0169-409X|accessdate=2020-04-27|date=2010-08-30|work=Advanced drug delivery reviews|last3=Chen|archive-date=8 березня 2021|archive-url=https://web.archive.org/web/20210308105348/https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2988080/}}</ref>, представляють собою розвиток методичних прийомів «фізіологічної хірургії» [[Павлов Іван Петрович|І. П. Павлова]] (1902) і сучасного представлення про [[Персоналізована медицина|персоналізований підхід]] до хірургічного лікування пацієнта<ref>J. P. Pawlow (1902). [https://link.springer.com/article/10.1007/BF02188382 Die physiologische Chirurgie des Verdauungskanals.] {{Webarchive|url=https://web.archive.org/web/20171021165041/https://link.springer.com/article/10.1007/BF02188382 |date=21 жовтня 2017 }} ''Ergebnisse der Physiol.'', vol. 1, no. 1, pp. 246—284, 1902.</ref>. |
|||
==== Сигнальні шляхи ==== |
|||
Клітинна сигналізація організовує динамічну взаємодію між молекулами в клітинах, дозволяючи їм спілкуватися та реагувати на внутрішні та зовнішні сигнали. Ці сигнальні шляхи утворюють складну мережу, сприяючи точним і скоординованим клітинним реакціям, що має вирішальне значення для підтримки здоров’я. Порушення в цих шляхах можуть призвести до збоїв, сприяючи виникненню та прогресуванню різних захворювань. Розуміння та аналіз цих сигнальних механізмів має першорядне значення для розшифровки [[Етіологія (медицина)|етіології]] захворювання та розробки цільових терапевтичних втручань. Деякі з сигнальних шляхів наведені нижче. |
|||
{{multiple image||width1=180|image1=MAPKpathway.jpg|caption1=Шляхи MAPK|width2=180|image2=MAPK-pathway-mammalian.png|caption2=Спрощений огляд шляхів MAPK у ссавців|align=|direction=|total_width=|alt1=}} |
|||
1. Шляхи MAPK ([[протеїнкінази, що активуються мітогенами]]) (ERK, JNK, p38)<ref>{{Cite news|title=MAP Kinase Pathways|url=http://cshperspectives.cshlp.org/content/4/11/a011254|work=Cold Spring Harbor Perspectives in Biology|date=2012-11-01|accessdate=2023-12-30|issn=1943-0264|pmc=PMC3536342|pmid=23125017|doi=10.1101/cshperspect.a011254|pages=a011254|volume=4|issue=11|language=en|first=Deborah K.|last=Morrison}}</ref>: |
|||
* Функція: регулють [[Проліферація|проліферацію]], [[Диференціація клітин|диференціювання]] та виживання клітин у відповідь на зовнішні подразники, такі як [[фактори росту]] та [[стрес]]. |
|||
* Порушення: |
|||
** Онкопатології: аномальна активація призводить до неконтрольованого росту клітин і прогресування пухлини. |
|||
** [[Неврологічний розлад|Неврологічні розлади]]: змінена сигналізація MAPK, пов’язана з нейродегенеративними станами, такими як [[хвороба Альцгеймера]] та [[Хвороба Паркінсона|Паркінсона]]. |
|||
** [[Серцево-судинні захворювання]]: відіграє роль у [[Гіпертрофія лівого шлуночка|гіпертрофії]] серця та [[Серцева недостатність|серцевій недостатності]]. |
|||
[[Файл:Summary of the phosphoinositide 3-kinase (PI3K) — protein kinase B (AKT) — mammalian target of rapamycin (mTOR) signaling pathway.png|міні|{{Не перекладено|Сигнальний шлях PI3K/AKT/mTOR|Сигнальний шлях PI3K/AKT/mTOR|en|PI3K/AKT/mTOR pathway}}<ref name=":0">{{Cite news|title=Targeting the PI3K/AKT/mTOR Signaling Pathway in Lung Cancer: An Update Regarding Potential Drugs and Natural Products|url=https://www.mdpi.com/1420-3049/26/13/4100|work=Molecules|date=2021-01|accessdate=2023-12-30|issn=1420-3049|doi=10.3390/molecules26134100|pages=4100|volume=26|issue=13|language=en|last=Iksen|first2=Sutthaorn|last2=Pothongsrisit|first3=Varisa|last3=Pongrakhananon}}</ref>]] |
|||
2. {{Не перекладено|Сигнальний шлях PI3K/AKT/mTOR|Сигнальний шлях PI3K/AKT/mTOR|en|PI3K/AKT/mTOR pathway}}: |
|||
* Функція: контролює ріст клітин, виживання та [[Обмін речовин|метаболізм]] у відповідь на фактори росту та [[інсулін]]. |
|||
* Порушення: |
|||
** Онкопатології: порушення регуляції сприяє проліферації клітин і пригніченню [[Апоптоз|апоптозу]].<ref name=":0" /><ref>{{Cite news|title=PI3K/Akt/mTOR Pathway and Its Role in Cancer Therapeutics: Are We Making Headway?|url=https://www.frontiersin.org/articles/10.3389/fonc.2022.819128|work=Frontiers in Oncology|date=2022|accessdate=2023-12-30|issn=2234-943X|pmc=PMC8987494|pmid=35402264|doi=10.3389/fonc.2022.819128|volume=12|first=Yan|last=Peng|first2=Yuanyuan|last2=Wang|first3=Cheng|last3=Zhou|first4=Wuxuan|last4=Mei|first5=Changchun|last5=Zeng}}</ref><ref>{{Cite news|title=PI3K/AKT/mTOR signaling transduction pathway and targeted therapies in cancer|url=https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-023-01827-6|work=Molecular Cancer|date=2023-08-18|accessdate=2023-12-30|issn=1476-4598|pmc=PMC10436543|pmid=37596643|doi=10.1186/s12943-023-01827-6|volume=22|issue=1|language=en|first=Antonino|last=Glaviano|first2=Aaron S. C.|last2=Foo|first3=Hiu Y.|last3=Lam|first4=Kenneth C. H.|last4=Yap|first5=William|last5=Jacot|first6=Robert H.|last6=Jones|first7=Huiyan|last7=Eng|first8=Madhumathy G.|last8=Nair|first9=Pooyan|last9=Makvandi}}</ref> |
|||
** Метаболічні розлади: бере участь у передачі сигналів інсуліну та причетний до [[Метаболічні захворювання|метаболічних захворювань]], таких як [[Діабет (види)|діабет]]. |
|||
** Неврологічні розлади: причетне до нейродегенеративних станів. |
|||
[[Файл:Canonical and non-canonical Wnt signaling pathways.png|міні|Канонічний та неканонічні {{Не перекладено|Сигнальний шлях Wnt|сигнальні шляхи Wnt|en|Wnt signaling pathway}}.<ref name=":1">{{Cite news|title=Wnt Signaling Pathways: From Inflammation to Non-Melanoma Skin Cancers|url=https://www.mdpi.com/1422-0067/24/2/1575|work=[[International Journal of Molecular Sciences]]|date=2023-01|accessdate=2023-12-30|issn=1422-0067|doi=10.3390/ijms24021575|pages=1575|volume=24|issue=2|language=en|first=Luca|last=Di Bartolomeo|first2=Federico|last2=Vaccaro|first3=Natasha|last3=Irrera|first4=Francesco|last4=Borgia|first5=Federica|last5=Li Pomi|first6=Francesco|last6=Squadrito|first7=Mario|last7=Vaccaro}}</ref>]] |
|||
3. {{Не перекладено|Сигнальний шлях Wnt|Сигнальний шлях Wnt|en|Wnt signaling pathway}}: |
|||
* Функція: регулює диференціацію клітин, проліферацію та [[гомеостаз]] [[Тканина (біологія)|тканин]] під час [[Розвиток людини|розвитку]]. |
|||
* Порушення: дисрегуляція, пов’язана з різними видами раку та розладами розвитку.<ref name=":1" /> |
|||
4. [[Сигнальний шлях Notch]]: |
|||
* Функція: бере участь у диференціації та формуванні тканинних структур під час розвитку та гомеостазу. |
|||
* Порушення: дисрегуляція пов’язана з онкопатологіями, розладами розвитку та серцево-судинними захворюваннями. |
|||
5.{{Не перекладено|Сигнальний шлях TGF-β|Сигнальний шлях TGF-β|en|TGF beta signaling pathway}}: |
|||
* Функція: регулює ріст клітин, диференціювання та [[Імунна відповідь|імунні відповіді.]] |
|||
* Порушення: дисрегуляція, пов’язана з онкопатологіями, [[Фіброз|фіброзом]] і захворюваннями, пов’язаними з імунною системою. |
|||
6. Сигнальний шлях {{Не перекладено|NF-κB|NF-κB|en|NF-κB}}: |
|||
* Функція: контролює імунні реакції, [[запалення]]<ref>{{Cite news|title=NF-κB signaling in inflammation|url=https://www.nature.com/articles/sigtrans201723|work=Signal Transduction and Targeted Therapy|date=2017-07-14|accessdate=2023-12-30|issn=2059-3635|doi=10.1038/sigtrans.2017.23|pages=1–9|volume=2|issue=1|language=en|first=Ting|last=Liu|first2=Lingyun|last2=Zhang|first3=Donghyun|last3=Joo|first4=Shao-Cong|last4=Sun}}</ref>, виживання клітин і проліферацію. |
|||
* Порушення регуляції, пов’язані з хронічними запальними захворюваннями, [[Автоімунні захворювання|аутоімунними розладами]] та деякими видами раку. |
|||
=== Міждисциплінарна співпраця === |
|||
==== Інтеграція дисциплін ==== |
|||
Молекулярна медицина об’єднує різні наукові дисципліни — біологію, генетику, біохімію, біомедицину, біоінформатику, біотехнологію, біоінженерію — інтегруючи знання, щоб розгадати тонкощі здоров’я та хвороби. Це підкреслює взаємозв’язок цих областей у розумінні молекулярних явищ. |
|||
==== Оміксні технології ==== |
|||
[[Файл:Longitudinal multi-omics and wearable data enabled deep phenotyping for precision health.jpg|міні|Інтеграція [[Біоінформатика|біоінформатичних]] даних [[Оміксні технології|оміксних технологій]] в [[Мультиоміка|мультиоміці]].]] |
|||
Передові [[оміксні технології]], як-от [[геноміка]], [[епігеноміка]], [[протеоміка]], [[метаболоміка]], [[Транскриптомні технології|транскриптоміка]], мікробіоміка та їх [[Мультиоміка|мультиоміксна]] інтеграція, дають дослідникам можливість формувати комплексне та деталізоване уявлення про молекулярні біологічні взаємодії всередині клітин та тканин. |
|||
==== Фармакогеноміка та розробка ліків ==== |
|||
На індивідуальні реакції на ліки впливають генетичні варіації. [[Фармакогеноміка]] спрямована на адаптацію терапії на основі геномної структури людини, сприяючи розвитку [[Персоналізована медицина|персоналізованої медицини]]. |
|||
==== Генетична інженерія ==== |
|||
[[Файл:Gene therapy.jpg|міні|[[Генотерапія]]]] |
|||
[[Генетична інженерія]] розширює можливості молекулярної медицини, уможливлюючи точні модифікації в генетичному коді, пропонуючи потенціал для виправлення генетичних дефектів, створення терапевтичних білків і розробки інноваційних методів [[Генотерапія|генної терапії]] та [[Редагування генома|редагування геному]], націлених на спадкові захворювання або складні розлади в їх молекулярному корінні. Ця технологія революціонізує стратегії лікування, сприяючи створенню персоналізованих терапій і вдосконалюючи здатність маніпулювати молекулярними шляхами для отримання терапевтичних переваг. |
|||
==== Молекулярна діагностика та біосенсори ==== |
|||
Молекулярні [[Біомаркер|біомаркери]] є специфічними маяками, що полегшують ранню діагностику захворювання. Різноманітні методики оміксних технологій, такі як [[Секвенування ДНК|секвенування геному]] чи [[мас-спектрометрія]], довзоляють ідентифікувати біомаркери для діагностики. |
|||
[[Файл:Schematic diagram of typical biosensor.webp|міні|Типова схема [[Біосенсор|біосенсору]]]] |
|||
[[Біосенсор|Біосенсори]] відіграють ключову роль у молекулярній медицині, виявляючи та кількісно оцінюючи конкретні біологічні молекули або маркери, забезпечуючи точне розуміння молекулярних процесів у живих системах у реальному часі. Ці пристрої полегшують швидку діагностику, персоналізоване лікування та безперервний моніторинг, покращуючи розуміння захворювань і уможливлюючи цілеспрямовані втручання на молекулярному рівні. |
|||
==== Наномедицина ==== |
|||
[[Наномедицина]] використовує [[Нанонаука|нанорозмірні]] матеріали та пристрої для точної діагностики, цільової доставки ліків і терапевтичного втручання на молекулярному рівні в організмі. Завдяки нанорозмірним платформам, таким як [[Наночастинка|наночастинки]] та нанопристрої, вона забезпечує безпрецедентну точність у лікуванні, підвищує ефективність ліків при мінімізації побічних ефектів, революціонізуючи лікування захворювань у молекулярному масштабі. |
|||
==== Біофотоніка ==== |
|||
[[Біофотоніка]], на стику [[Фотоніка|фотоніки]], біології та медицини, революціонізує молекулярну медицину завдяки передовим технологіям на основі [[Світло|світла]]. Методики біофотоніки дають змогу використовувати такі методи [[Медична візуалізація|візуалізації]] з високою роздільною здатністю, як [[Флуоресцентна мікроскопія|флуоресцентна]] та [[конфокальна мікроскопія]], полегшують [[Оптична спектроскопія|оптичну спектроскопію]] для молекулярного аналізу та підтримують методи оптичної маніпуляції та біосенсорів для діагностики та терапії, пропонуючи потужний набір інструментів для вивчення та втручання на молекулярному рівні в біологічні системи.<ref>{{Cite news|title=Paradigm shift in future biophotonics for imaging and therapy: Miniature living lasers to cellular scale optoelectronics|url=https://www.thno.org/v12p7335.htm|work=Theranostics|date=2022-10-17|accessdate=2023-12-30|issn=1838-7640|pmc=PMC9691355|pmid=36438477|doi=10.7150/thno.75905|pages=7335–7350|volume=12|issue=17|language=en|first=Paromita|last=Sarbadhikary|first2=Blassan P.|last2=George|first3=Heidi|last3=Abrahamse}}</ref> Сюди ж відносяться дослідження, що охоплюють оптико-акустичну візуалізацію, оптичну когерентну томографію та дворежимний ультразвук/фотоакустику, що забезпечує глибокий моніторинг тканин і портативне біомедичне зображення. Інші інновації включають плазмонічні екзосомні біосенсори, оптичну ендоскопію з [[Наночастинка|наночастинками]] та лазерну спектроскопічну техніку для медичної діагностики, що розширює межі діагностики та лікування, наприклад, у рамках [[Лапароскопічна хірургія|лапароскопічної хірургії]].<ref>{{Cite book |
|||
|url=https://link.springer.com/10.1007/978-981-287-627-0 |
|||
|title=Frontiers in Biophotonics for Translational Medicine: In the Celebration of Year of Light (2015) |
|||
|date=2016 |
|||
|editor-last=Olivo |
|||
|editor-first=Malini |
|||
|editor2-last=Dinish |
|||
|editor2-first=U. S. |
|||
|series=Progress in Optical Science and Photonics |
|||
|publisher=Springer Singapore |
|||
|volume=3 |
|||
|location=Singapore |
|||
|language=en |
|||
|doi=10.1007/978-981-287-627-0 |
|||
|isbn=978-981-287-626-3 |
|||
}}</ref> |
|||
==== Молекулярна хірургія ==== |
|||
Молекулярна хірургія — це застаріла назва концепції молекулярної медицини, яка передбачає точні, цілеспрямовані втручання на молекулярному рівні для діагностики, лікування або запобігання захворюванням. Під «хірургією» в цьому розумінні малось на увазі процеси, як-от редагування генома чи наномедична доставка ліків. |
|||
Але крім того, в [[2010-ті|2010-х]] та [[2020-ті|2020-х]] зароджується концепція молекулярної хірургії в контексті [[Хірургія|хірургії]]. Наприклад, «молекулярна [[нейрохірургія]]<nowiki/>» представляє новаторський медичний підхід, що передбачає точне усунення цільових [[Нейрон|нейронів]] за допомогою потужних [[Ліганд (біохімія)|лігандів]], які взаємодіють зі специфічними [[Рецептор (білок)|рецепторами]], що призводить до вибіркової смерті клітин. Ця процедура, прикладом якої є надпотужні {{Не перекладено|Ванілоїд|ванілоїди|en|Vanilloid}}, такі як RTX, спрямовані на нейрони, що експресують [[TRPV1]], пропонує багатообіцяючий шлях для лікування [[Біль|больових]] станів і потенційно революціонізує лікування окнопатологій шляхом цілеспрямованої елімінації клітин.<ref>{{Cite news|title=Molecular Surgery Concept from Bench to Bedside: A Focus on TRPV1+ Pain-Sensing Neurons|url=http://journal.frontiersin.org/article/10.3389/fphys.2017.00378/full|work=Frontiers in Physiology|date=2017-06-02|accessdate=2023-12-30|issn=1664-042X|pmc=PMC5455100|pmid=28626428|doi=10.3389/fphys.2017.00378|volume=8|first=László|last=Pecze|first2=Béla|last2=Viskolcz|first3=Zoltán|last3=Oláh}}</ref><ref>{{Cite news|title=Synthesis of endohedral fullerenes by molecular surgery|url=https://www.nature.com/articles/s42004-022-00738-9|work=[[Communications Chemistry]]|date=2022-10-08|accessdate=2023-12-30|issn=2399-3669|doi=10.1038/s42004-022-00738-9|pages=1–14|volume=5|issue=1|language=en|first=Sally|last=Bloodworth|first2=Richard J.|last2=Whitby}}</ref> |
|||
== Див. також == |
== Див. також == |
||
* [[Біомедицина]] |
|||
* [[Біомедична інженерія]] |
|||
* [[Біотехнологія]] |
|||
* [[Наномедицина]] |
* [[Наномедицина]] |
||
* [[Генотерапія]] |
|||
* [[Редагування генома]] |
|||
* [[Молекулярна біологія]] |
* [[Молекулярна біологія]] |
||
* [[Молекулярна нейронаука]] |
* [[Молекулярна нейронаука]] |
||
* [[Біомолекулярна електроніка]] |
* [[Біомолекулярна електроніка]] |
||
* [[Профілактична медицина]] |
|||
* [[Мультиоміка|Мультоміка]] |
|||
* [[Персоналізована медицина]] |
* [[Персоналізована медицина]] |
||
* [[Медицина]] |
* [[Медицина]] |
||
| Рядок 56: | Рядок 131: | ||
=== Книги === |
=== Книги === |
||
* Carsten Carlberg, Eunike Velleuer, Ferdinand Molnár (2023). ''[https://link.springer.com/book/10.1007/978-3-031-27133-5 Molecular Medicine: How Science Works]'' (eng). Springer Cham, [[Springer Nature]]. с. 700. [[ISBN]] [[Спеціальна:Джерела книг/978-3-031-27132-8|978-3-031-27132-8]]. |
|||
* Kumar Dhavendra, ред. (2020). [https://shop.elsevier.com/books/clinical-molecular-medicine/kumar/978-0-12-809356-6 ''Clinical molecular medicine: principles and practice''.] London, San Diego, Cambridge: Academic Press, [[Elsevier]]. [[ISBN]] [[Спеціальна:Джерела книг/978-0-12-809356-6|978-0-12-809356-6]]. |
* Kumar Dhavendra, ред. (2020). [https://shop.elsevier.com/books/clinical-molecular-medicine/kumar/978-0-12-809356-6 ''Clinical molecular medicine: principles and practice''.] London, San Diego, Cambridge: Academic Press, [[Elsevier]]. [[ISBN]] [[Спеціальна:Джерела книг/978-0-12-809356-6|978-0-12-809356-6]]. |
||
* Carsten Carlberg, Eunike Velleuer, Ferdinand Molnár (2023). ''[https://link.springer.com/book/10.1007/978-3-031-27133-5 Molecular Medicine: How Science Works]'' (eng). [[Springer]] Cham. с. 700. [[ISBN]] [[Спеціальна:Джерела книг/978-3-031-27132-8|978-3-031-27132-8]]. |
|||
* Серія книг [https://www.routledge.com/Gene-and-Cell-Therapy/book-series/CRCGENCELTHE Gene and Cell Therapy] ([[Routledge]], 2016-2021+) |
* Серія книг [https://www.routledge.com/Gene-and-Cell-Therapy/book-series/CRCGENCELTHE Gene and Cell Therapy] ([[Routledge]], 2016-2021+) |
||
| Рядок 78: | Рядок 153: | ||
* Mayr J. A.; Feichtinger R. G.; Achleitner M. T. та ін. (2021). Molecular medicine: pathobiochemistry as the key to personalized treatment of inherited diseases. (нім.) ''Monatsschrift Kinderheilkunde'' '''169''' (9). [[Цифровий ідентифікатор об'єкта|doi]]:[[doi:10.1007/s00112-021-01252-3|10.1007/s00112-021-01252-3]]. |
* Mayr J. A.; Feichtinger R. G.; Achleitner M. T. та ін. (2021). Molecular medicine: pathobiochemistry as the key to personalized treatment of inherited diseases. (нім.) ''Monatsschrift Kinderheilkunde'' '''169''' (9). [[Цифровий ідентифікатор об'єкта|doi]]:[[doi:10.1007/s00112-021-01252-3|10.1007/s00112-021-01252-3]]. |
||
* Orkin Stuart H. (2021). Molecular Medicine: Found in Translation. ''Med'' '''2''' (2). [[Цифровий ідентифікатор об'єкта|doi]]:[[doi:10.1016/j.medj.2020.12.011|10.1016/j.medj.2020.12.011]]. |
* Orkin Stuart H. (2021). Molecular Medicine: Found in Translation. ''Med'' '''2''' (2). [[Цифровий ідентифікатор об'єкта|doi]]:[[doi:10.1016/j.medj.2020.12.011|10.1016/j.medj.2020.12.011]]. |
||
* Doherty, R. (2006). Molecular surgery in the treatment of rheumatoid arthritis. ''Nature Reviews. Rheumatology'', 2(2), 61. {{doi|10.1038/ncprheum0078}} |
|||
* Roth, J. A. (1992). Molecular surgery for cancer. ''Archives of Surgery'', 127(11), 1298—1302. {{doi|10.1001/archsurg.1992.01420110040010}} |
|||
* Stone, R. (1992). Molecular 'surgery' for brain tumors. ''Science'', 256(5063), 1513—1514. {{doi|10.1126/science.1317967}} |
|||
* Hobom, B. (1980). With the scalpels of gene surgery against disease and hunger. ''Therapie der Gegenwart'', 119(2), 125—138. |
|||
{{Доробити}} |
|||
== Примітки == |
== Примітки == |
||
{{reflist| |
{{reflist|2}} |
||
{{Перспективні технології|біомед=так}} |
|||
<ref name="Тарантул2018">{{cite book |
|||
[[Категорія:Біомедицина]] |
|||
|author=Вячеслав Тарантул |
|||
|title=Толковый словарь по молекулярной и клеточной биотехнологии. Русско-английский |
|||
|url=https://books.google.com/books?id=kxZJDwAAQBAJ&pg=PA213 |
|||
|date=24 січня 2018 |
|||
|publisher=ЛитРес |
|||
|isbn=978-5-04-099417-5}}</ref> |
|||
}}{{Перспективні технології|біомед=так}} |
|||
[[Категорія:Молекулярна біологія]] |
[[Категорія:Молекулярна біологія]] |
||
[[Категорія: |
[[Категорія:Біотехнології]] |
||
[[Категорія: |
[[Категорія:Біомедична інженерія]] |
||
Версія за 12:15, 30 грудня 2023

Молекулярна медицина[1] — це міждисциплінарна галузь медицини й охорони здоров’я, зосереджена на розумінні та застосуванні молекулярних процесів для діагностики, лікування та профілактики захворювань. Вона охоплює вивчення біологічних механізмів на молекулярному рівні, об’єднуючи принципи з різних дисциплін, таких як біологія, генетика, біохімія, біомедицина, біотехнологія та біоінженерія.
Молекулярна медицина досліджує, як молекули взаємодіють у клітинах і організмах, розгадуючи заплутані шляхи, що лежать в основі здоров’я та хвороб. Розшифровуючи молекулярну основу захворювань, біомедичні науковці та дослідники можуть розробляти цільову терапію, персоналізовані підходи до медицини та інноваційні діагностичні інструменти.
Ця сфера відіграє ключову роль у розвитку охорони здоров’я завдяки використанню передових технологій, таких як оміксні технології, біоінформатика, біосенсори, генетична інженерія. За допомогою цих інструментів вчені можуть аналізувати геном, структури білків, широкий спектр метаболітів і молекулярні сигнальні шляхи, що веде до глибшого розуміння захворювань на молекулярному рівні.
Загальні принципи
Молекулярна медицина є наріжним каменем сучасної охорони здоров’я, заглиблюючись у складну сферу молекулярних і клітинних процесів, що керують життям. Ця дисципліна розкриває фундаментальні принципи молекулярної біології, досліджує молекулярні шляхи та об’єднує різноманітні наукові сфери, щоб розшифрувати механізми здоров’я та хвороби.
Молекулярні та клітинні процеси
Генетика та епігенетика

У мікроскопічному світі клітин нуклеїнові кислоти та білки є головними архітекторами, що керують клітинними процесами. Нуклеїнові кислоти, зокрема ДНК і РНК, зберігають генетичний код, тоді як білки виконують життєво важливі функції в клітинах. Ця взаємодія молекул формує основу життя. ДНК, основне сховище генетичної інформації, що міститься в клітинному ядрі, проходить низку процесів — транскрипції та трансляції, що завершується синтезом білків. Ця центральна догма пояснює потік генетичної інформації в клітинах, керуючи їх поведінкою та функціями. Генетичний код, представлений кодонами, яким відповідають конкретні амінокислоти, пояснює, як інструкції ДНК транслюються в білкові послідовності. Генетичні мутації, охоплюючі точкові мутації, вставки та делеції можуть порушити цей код, потенційно призводячи до аномальних білків і захворювань. Сукупність всієї генетичної інформації називаються геном, геноміка досліджує весь геном організму, а медична генетика патолології геному людини. Різні біотехнологічні й біомедичні методики, такі як генотерапія та редагування геному, дозволяють впливати на геном людини.
Крім того, активність певних генів регулюється різними механізмами, зокрема — епігенетичними. Сукупність всіх епігенетичних надстроєк геному називається епігеном. Епігеноміка вивчає епігеном і практичні методики впливу на епігеном, такі як епігенетичне перерпрограмування та редагування епігеному[en].
Сигнальні шляхи
Клітинна сигналізація організовує динамічну взаємодію між молекулами в клітинах, дозволяючи їм спілкуватися та реагувати на внутрішні та зовнішні сигнали. Ці сигнальні шляхи утворюють складну мережу, сприяючи точним і скоординованим клітинним реакціям, що має вирішальне значення для підтримки здоров’я. Порушення в цих шляхах можуть призвести до збоїв, сприяючи виникненню та прогресуванню різних захворювань. Розуміння та аналіз цих сигнальних механізмів має першорядне значення для розшифровки етіології захворювання та розробки цільових терапевтичних втручань. Деякі з сигнальних шляхів наведені нижче.
1. Шляхи MAPK (протеїнкінази, що активуються мітогенами) (ERK, JNK, p38)[2]:
- Функція: регулють проліферацію, диференціювання та виживання клітин у відповідь на зовнішні подразники, такі як фактори росту та стрес.
- Порушення:
- Онкопатології: аномальна активація призводить до неконтрольованого росту клітин і прогресування пухлини.
- Неврологічні розлади: змінена сигналізація MAPK, пов’язана з нейродегенеративними станами, такими як хвороба Альцгеймера та Паркінсона.
- Серцево-судинні захворювання: відіграє роль у гіпертрофії серця та серцевій недостатності.

2. Сигнальний шлях PI3K/AKT/mTOR:
- Функція: контролює ріст клітин, виживання та метаболізм у відповідь на фактори росту та інсулін.
- Порушення:

- Функція: регулює диференціацію клітин, проліферацію та гомеостаз тканин під час розвитку.
- Порушення: дисрегуляція, пов’язана з різними видами раку та розладами розвитку.[6]
- Функція: бере участь у диференціації та формуванні тканинних структур під час розвитку та гомеостазу.
- Порушення: дисрегуляція пов’язана з онкопатологіями, розладами розвитку та серцево-судинними захворюваннями.
- Функція: регулює ріст клітин, диференціювання та імунні відповіді.
- Порушення: дисрегуляція, пов’язана з онкопатологіями, фіброзом і захворюваннями, пов’язаними з імунною системою.
- Функція: контролює імунні реакції, запалення[7], виживання клітин і проліферацію.
- Порушення регуляції, пов’язані з хронічними запальними захворюваннями, аутоімунними розладами та деякими видами раку.
Міждисциплінарна співпраця
Інтеграція дисциплін
Молекулярна медицина об’єднує різні наукові дисципліни — біологію, генетику, біохімію, біомедицину, біоінформатику, біотехнологію, біоінженерію — інтегруючи знання, щоб розгадати тонкощі здоров’я та хвороби. Це підкреслює взаємозв’язок цих областей у розумінні молекулярних явищ.
Оміксні технології

Передові оміксні технології, як-от геноміка, епігеноміка, протеоміка, метаболоміка, транскриптоміка, мікробіоміка та їх мультиоміксна інтеграція, дають дослідникам можливість формувати комплексне та деталізоване уявлення про молекулярні біологічні взаємодії всередині клітин та тканин.
Фармакогеноміка та розробка ліків
На індивідуальні реакції на ліки впливають генетичні варіації. Фармакогеноміка спрямована на адаптацію терапії на основі геномної структури людини, сприяючи розвитку персоналізованої медицини.
Генетична інженерія
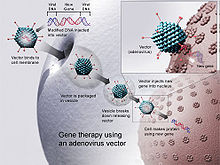
Генетична інженерія розширює можливості молекулярної медицини, уможливлюючи точні модифікації в генетичному коді, пропонуючи потенціал для виправлення генетичних дефектів, створення терапевтичних білків і розробки інноваційних методів генної терапії та редагування геному, націлених на спадкові захворювання або складні розлади в їх молекулярному корінні. Ця технологія революціонізує стратегії лікування, сприяючи створенню персоналізованих терапій і вдосконалюючи здатність маніпулювати молекулярними шляхами для отримання терапевтичних переваг.
Молекулярна діагностика та біосенсори
Молекулярні біомаркери є специфічними маяками, що полегшують ранню діагностику захворювання. Різноманітні методики оміксних технологій, такі як секвенування геному чи мас-спектрометрія, довзоляють ідентифікувати біомаркери для діагностики.

Біосенсори відіграють ключову роль у молекулярній медицині, виявляючи та кількісно оцінюючи конкретні біологічні молекули або маркери, забезпечуючи точне розуміння молекулярних процесів у живих системах у реальному часі. Ці пристрої полегшують швидку діагностику, персоналізоване лікування та безперервний моніторинг, покращуючи розуміння захворювань і уможливлюючи цілеспрямовані втручання на молекулярному рівні.
Наномедицина
Наномедицина використовує нанорозмірні матеріали та пристрої для точної діагностики, цільової доставки ліків і терапевтичного втручання на молекулярному рівні в організмі. Завдяки нанорозмірним платформам, таким як наночастинки та нанопристрої, вона забезпечує безпрецедентну точність у лікуванні, підвищує ефективність ліків при мінімізації побічних ефектів, революціонізуючи лікування захворювань у молекулярному масштабі.
Біофотоніка
Біофотоніка, на стику фотоніки, біології та медицини, революціонізує молекулярну медицину завдяки передовим технологіям на основі світла. Методики біофотоніки дають змогу використовувати такі методи візуалізації з високою роздільною здатністю, як флуоресцентна та конфокальна мікроскопія, полегшують оптичну спектроскопію для молекулярного аналізу та підтримують методи оптичної маніпуляції та біосенсорів для діагностики та терапії, пропонуючи потужний набір інструментів для вивчення та втручання на молекулярному рівні в біологічні системи.[8] Сюди ж відносяться дослідження, що охоплюють оптико-акустичну візуалізацію, оптичну когерентну томографію та дворежимний ультразвук/фотоакустику, що забезпечує глибокий моніторинг тканин і портативне біомедичне зображення. Інші інновації включають плазмонічні екзосомні біосенсори, оптичну ендоскопію з наночастинками та лазерну спектроскопічну техніку для медичної діагностики, що розширює межі діагностики та лікування, наприклад, у рамках лапароскопічної хірургії.[9]
Молекулярна хірургія
Молекулярна хірургія — це застаріла назва концепції молекулярної медицини, яка передбачає точні, цілеспрямовані втручання на молекулярному рівні для діагностики, лікування або запобігання захворюванням. Під «хірургією» в цьому розумінні малось на увазі процеси, як-от редагування генома чи наномедична доставка ліків.
Але крім того, в 2010-х та 2020-х зароджується концепція молекулярної хірургії в контексті хірургії. Наприклад, «молекулярна нейрохірургія» представляє новаторський медичний підхід, що передбачає точне усунення цільових нейронів за допомогою потужних лігандів, які взаємодіють зі специфічними рецепторами, що призводить до вибіркової смерті клітин. Ця процедура, прикладом якої є надпотужні ванілоїди[en], такі як RTX, спрямовані на нейрони, що експресують TRPV1, пропонує багатообіцяючий шлях для лікування больових станів і потенційно революціонізує лікування окнопатологій шляхом цілеспрямованої елімінації клітин.[10][11]
Див. також
- Біомедицина
- Біомедична інженерія
- Біотехнологія
- Наномедицина
- Молекулярна біологія
- Молекулярна нейронаука
- Біомолекулярна електроніка
- Профілактична медицина
- Персоналізована медицина
- Медицина
Додаткова література
Книги
- Carsten Carlberg, Eunike Velleuer, Ferdinand Molnár (2023). Molecular Medicine: How Science Works (eng). Springer Cham, Springer Nature. с. 700. ISBN 978-3-031-27132-8.
- Kumar Dhavendra, ред. (2020). Clinical molecular medicine: principles and practice. London, San Diego, Cambridge: Academic Press, Elsevier. ISBN 978-0-12-809356-6.
- Серія книг Gene and Cell Therapy (Routledge, 2016-2021+)
Журнали
- Experimental & Molecular Medicine (сайт, Nature Portfolio)
- Molecular Therapy (сайт, Cell Press, Elsevier)
- Trends in Molecular Medicine (Cell Press, Elsevier)
- Journal of Molecular Medicine (Springer)
- Molecular Aspects of Medicine (Elsevier)
- Current Molecular Medicine (Bentham Science Publishers)
- Expert Reviews in Molecular Medicine (Cambridge University Press)
- Journal of Cellular and Molecular Medicine (Wiley-Blackwell)
- International Journal of Molecular Medicine (Spandidos Publications)
- Frontiers in Molecular Medicine (Frontiers)
Статті
- Muraoka Takahiro; Ajioka Itsuki (2022). Self-assembling Molecular Medicine for the Subacute Phase of Ischemic Stroke. Neurochemical Research (англ.) 47 (9). doi:10.1007/s11064-022-03638-5.
- Mayr J. A.; Feichtinger R. G.; Achleitner M. T. та ін. (2021). Molecular medicine: pathobiochemistry as the key to personalized treatment of inherited diseases. (нім.) Monatsschrift Kinderheilkunde 169 (9). doi:10.1007/s00112-021-01252-3.
- Orkin Stuart H. (2021). Molecular Medicine: Found in Translation. Med 2 (2). doi:10.1016/j.medj.2020.12.011.
Примітки
- ↑ Carsten Carlberg, Eunike Velleuer, Ferdinand Molnár (2023). Molecular Medicine: How Science Works (eng) . Springer Cham. с. 700. doi:10.1007/978-3-031-27133-5. ISBN 978-3-031-27132-8.
- ↑ Morrison, Deborah K. (1 листопада 2012). MAP Kinase Pathways. Cold Spring Harbor Perspectives in Biology (англ.). Т. 4, № 11. с. a011254. doi:10.1101/cshperspect.a011254. ISSN 1943-0264. PMC 3536342. PMID 23125017. Процитовано 30 грудня 2023.
{{cite news}}: Обслуговування CS1: Сторінки з PMC з іншим форматом (посилання) - ↑ а б Iksen; Pothongsrisit, Sutthaorn; Pongrakhananon, Varisa (2021-01). Targeting the PI3K/AKT/mTOR Signaling Pathway in Lung Cancer: An Update Regarding Potential Drugs and Natural Products. Molecules (англ.). Т. 26, № 13. с. 4100. doi:10.3390/molecules26134100. ISSN 1420-3049. Процитовано 30 грудня 2023.
{{cite news}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ Peng, Yan; Wang, Yuanyuan; Zhou, Cheng; Mei, Wuxuan; Zeng, Changchun (2022). PI3K/Akt/mTOR Pathway and Its Role in Cancer Therapeutics: Are We Making Headway?. Frontiers in Oncology. Т. 12. doi:10.3389/fonc.2022.819128. ISSN 2234-943X. PMC 8987494. PMID 35402264. Процитовано 30 грудня 2023.
{{cite news}}: Обслуговування CS1: Сторінки з PMC з іншим форматом (посилання) Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ Glaviano, Antonino; Foo, Aaron S. C.; Lam, Hiu Y.; Yap, Kenneth C. H.; Jacot, William; Jones, Robert H.; Eng, Huiyan; Nair, Madhumathy G.; Makvandi, Pooyan (18 серпня 2023). PI3K/AKT/mTOR signaling transduction pathway and targeted therapies in cancer. Molecular Cancer (англ.). Т. 22, № 1. doi:10.1186/s12943-023-01827-6. ISSN 1476-4598. PMC 10436543. PMID 37596643. Процитовано 30 грудня 2023.
{{cite news}}: Обслуговування CS1: Сторінки з PMC з іншим форматом (посилання) Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ а б Di Bartolomeo, Luca; Vaccaro, Federico; Irrera, Natasha; Borgia, Francesco; Li Pomi, Federica; Squadrito, Francesco; Vaccaro, Mario (2023-01). Wnt Signaling Pathways: From Inflammation to Non-Melanoma Skin Cancers. International Journal of Molecular Sciences (англ.). Т. 24, № 2. с. 1575. doi:10.3390/ijms24021575. ISSN 1422-0067. Процитовано 30 грудня 2023.
{{cite news}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ Liu, Ting; Zhang, Lingyun; Joo, Donghyun; Sun, Shao-Cong (14 липня 2017). NF-κB signaling in inflammation. Signal Transduction and Targeted Therapy (англ.). Т. 2, № 1. с. 1—9. doi:10.1038/sigtrans.2017.23. ISSN 2059-3635. Процитовано 30 грудня 2023.
- ↑ Sarbadhikary, Paromita; George, Blassan P.; Abrahamse, Heidi (17 жовтня 2022). Paradigm shift in future biophotonics for imaging and therapy: Miniature living lasers to cellular scale optoelectronics. Theranostics (англ.). Т. 12, № 17. с. 7335—7350. doi:10.7150/thno.75905. ISSN 1838-7640. PMC 9691355. PMID 36438477. Процитовано 30 грудня 2023.
{{cite news}}: Обслуговування CS1: Сторінки з PMC з іншим форматом (посилання) - ↑ Olivo, Malini; Dinish, U. S., ред. (2016). Frontiers in Biophotonics for Translational Medicine: In the Celebration of Year of Light (2015). Progress in Optical Science and Photonics (англ.). Т. 3. Singapore: Springer Singapore. doi:10.1007/978-981-287-627-0. ISBN 978-981-287-626-3.
- ↑ Pecze, László; Viskolcz, Béla; Oláh, Zoltán (2 червня 2017). Molecular Surgery Concept from Bench to Bedside: A Focus on TRPV1+ Pain-Sensing Neurons. Frontiers in Physiology. Т. 8. doi:10.3389/fphys.2017.00378. ISSN 1664-042X. PMC 5455100. PMID 28626428. Процитовано 30 грудня 2023.
{{cite news}}: Обслуговування CS1: Сторінки з PMC з іншим форматом (посилання) Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ Bloodworth, Sally; Whitby, Richard J. (8 жовтня 2022). Synthesis of endohedral fullerenes by molecular surgery. Communications Chemistry (англ.). Т. 5, № 1. с. 1—14. doi:10.1038/s42004-022-00738-9. ISSN 2399-3669. Процитовано 30 грудня 2023.

