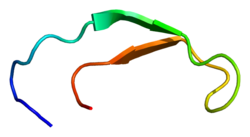Гепсидин
Гепсидин, HAMP (англ. Hepcidin antimicrobial peptide) – білок, який кодується геном HAMP, розташованим у людей на короткому плечі 19-ї хромосоми.[3] Довжина поліпептидного ланцюга препрогепсидину становить 84 амінокислот, а молекулярна маса — 9 408[4], проте біологічно активний зрілий пептид скдадається лише з 25 амінокислот[5].
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MALSSQIWAA | CLLLLLLLAS | LTSGSVFPQQ | TGQLAELQPQ | DRAGARASWM | ||||
| PMFQRRRRRD | THFPICIFCC | GCCHRSKCGM | CCKT |
Кодований геном білок за функціями належить до гормонів, антибіотиків, антимікробних білків, фунгіцидів.
Історія[ред. | ред. код]
Гепсидин відкритий у 2000 році і спочатку був названий LEAP-1 (експресований печінкою антимікробний пептид), але згодом на мишах було встановлено зворотну кореляцію між експресією гепсидину та абсорбцією заліза з кишечнику.
У подальшому докази зв'язку гепсидину з анемією запалення надійшли з лабораторії біолога Ненсі Ендрюс (Nancy Andrews), коли дослідники вивчали тканини двох пацієнтів з пухлинами печінки та важкою мікроцитарною анемією, яка не реагувала на введення заліза. Пухлинна тканина відзначалася надмірним синтезом гепсидину і містила велику кількість мРНК гепсидину. Хірургічне видалення пухлини вилікувало анемію.
Взяті разом ці відкриття дозволили зробити висновок про вплив гепсидину на регуляцію всмоктування заліза в організмі.
Структура[ред. | ред. код]
Біологічно активний гепсидин є пептидом, що складається з 25 амінокислот та містить 4 дисульфідні зв'язки[6]. Біосинтез гепсидину проходить шлях препрогепсидину (84 амінокислоти), прогепсидину (60 амінокислот) та зрілого біологічно активного гепсидину (25 амінокислот). У подальшому гепсидин-25 перетворюється на гепсидин-22 і гепсидин-20 (відповідно 22 та 20 амінокислот)[7].
Функція[ред. | ред. код]
Гепсидин – ключовий білок-регулятор метаболізму заліза у ссавців.
Гепсидин пригнічує транспортування заліза шляхом зв'язування з ферропортином, який розташований на поверхні ентероцитів кишечника і на плазматичній мембрані клітин ретикулоендотеліальної системи (макрофагів). Інгібування ферропортину припиняє експорт заліза і воно секвеструється в клітинах. Інгібуючи ферропортин, гепцидин також перешкоджає транспорту ентероцитами заліза до портальної кровоносної системи, тим самим зменшуючи засвоєння заліза з їжі. Вивільнення заліза з макрофагів також знижується за рахунок інгібування ферропортину. Підвищена активність гепсидину відповідає за знижену доступність заліза, що спостерігається при анемії хронічного запалення (наприклад, при хронічній хворобі нирок, ревматоїдному артриті тощо).
Клінічне значення[ред. | ред. код]
Мутація гена гепсидину може призвести до системного перевантаження залізом або гемохроматозу (ювенільний гемохроматоз).
У випадку хронічних запальних захворювань з розвитком системної запальної відповіді відбувається надмірна експресія гепсидину, пригнічення внаслідок цього абсорбції заліза з кишечника, пригнічення використання заліза з депо та виникає неефективний гемопоез. Лікування пероральними препаратами заліза анемії при хронічному запальному захворюванні буде неефективним через блокаду транспортної системи заліза у кишечнику.
На жаль, визначення концентрації гепсидину у крові або сечі станом на 2019 рік малодоступне. Сурогатним маркером наявності хронічного запалення може слугувати рівень C-реактивного білку крові.
Література[ред. | ред. код]
- Park C.H., Valore E.V., Waring A.J., Ganz T. (2001). Hepcidin: a urinary antimicrobial peptide synthesized in the liver. J. Biol. Chem. 276: 7806—7810. PMID 11113131 DOI:10.1074/jbc.M008922200
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Kluever E., Schulz A., Forssmann W.-G., Adermann K. (2002). Chemical synthesis of beta-defensins and LEAP-1/hepcidin. J. Pept. Res. 59: 241—248. PMID 12010514 DOI:10.1034/j.1399-3011.2002.00980.x
- Ganz T., Nemeth E. (2012). Hepcidin and iron homeostasis. Biochim. Biophys. Acta. 1823: 1434—1443. PMID 22306005 DOI:10.1016/j.bbamcr.2012.01.014
- Hunter H.N., Fulton D.B., Ganz T., Vogel H.J. (2002). The solution structure of human hepcidin, a peptide hormone with antimicrobial activity that is involved in iron uptake and hereditary hemochromatosis. J. Biol. Chem. 277: 37597—37603. PMID 12138110 DOI:10.1074/jbc.M205305200
Примітки[ред. | ред. код]
- ↑ Захворювання, генетично пов'язані з HAMP переглянути/редагувати посилання на ВікіДаних.
- ↑ Human PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:15598 (англ.) . Архів оригіналу за 27 березня 2016. Процитовано 12 вересня 2017.
- ↑ UniProt, P81172 (англ.) . Архів оригіналу за 20 липня 2017. Процитовано 12 вересня 2017.
- ↑ https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2211381/
- ↑ https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2782009/
- ↑ «Iron Metabolism: Hepcidin» by Gerald Litwack. Cambridge, MA: Academic Press. — 2019. — 264 p. ISBN 978-0-12-817842-3
Див. також[ред. | ред. код]
| Це незавершена стаття про білки. Ви можете допомогти проєкту, виправивши або дописавши її. |