Альбумін
Перейти до навігації
Перейти до пошуку
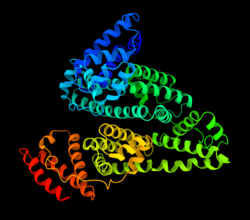
Альбумін (англ. Albumin) – білок, який кодується геном ALB, розташованим у людей на короткому плечі 4-ї хромосоми. [4] Довжина поліпептидного ланцюга білка становить 609 амінокислот, а молекулярна маса — 69 367[5].
Послідовність амінокислот
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MKWVTFISLL | FLFSSAYSRG | VFRRDAHKSE | VAHRFKDLGE | ENFKALVLIA | ||||
| FAQYLQQCPF | EDHVKLVNEV | TEFAKTCVAD | ESAENCDKSL | HTLFGDKLCT | ||||
| VATLRETYGE | MADCCAKQEP | ERNECFLQHK | DDNPNLPRLV | RPEVDVMCTA | ||||
| FHDNEETFLK | KYLYEIARRH | PYFYAPELLF | FAKRYKAAFT | ECCQAADKAA | ||||
| CLLPKLDELR | DEGKASSAKQ | RLKCASLQKF | GERAFKAWAV | ARLSQRFPKA | ||||
| EFAEVSKLVT | DLTKVHTECC | HGDLLECADD | RADLAKYICE | NQDSISSKLK | ||||
| ECCEKPLLEK | SHCIAEVEND | EMPADLPSLA | ADFVESKDVC | KNYAEAKDVF | ||||
| LGMFLYEYAR | RHPDYSVVLL | LRLAKTYETT | LEKCCAAADP | HECYAKVFDE | ||||
| FKPLVEEPQN | LIKQNCELFE | QLGEYKFQNA | LLVRYTKKVP | QVSTPTLVEV | ||||
| SRNLGKVGSK | CCKHPEAKRM | PCAEDYLSVV | LNQLCVLHEK | TPVSDRVTKC | ||||
| CTESLVNRRP | CFSALEVDET | YVPKEFNAET | FTFHADICTL | SEKERQIKKQ | ||||
| TALVELVKHK | PKATKEQLKA | VMDDFAAFVE | KCCKADDKET | CFAEEGKKLV | ||||
| AASQAALGL |
Білок має сайт для зв'язування з іоном міді, ліпідами, іонами металів, іоном цинку. Секретований назовні.
Література[ред. | ред. код]
- Dugaiczyk A., Law S.W., Dennison O.E. (1982). Nucleotide sequence and the encoded amino acids of human serum albumin mRNA. Proc. Natl. Acad. Sci. U.S.A. 79: 71—75. PMID 6275391 DOI:10.1073/pnas.79.1.71
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Meloun B., Moravek L., Kostka V. (1975). Complete amino acid sequence of human serum albumin. FEBS Lett. 58: 134—137. PMID 1225573 DOI:10.1016/0014-5793(75)80242-0
- Corbett J.M., Wheeler C.H., Baker C.S., Yacoub M.H., Dunn M.J. (1994). The human myocardial two-dimensional gel protein database: update 1994. Electrophoresis. 15: 1459—1465. PMID 7895732 DOI:10.1002/elps.11501501209
- Walker J.E. (1976). Lysine residue 199 of human serum albumin is modified by acetylsalicylic acid. FEBS Lett. 66: 173—175. PMID 955075 DOI:10.1016/0014-5793(76)80496-6
- Jacobsen C. (1978). Lysine residue 240 of human serum albumin is involved in high-affinity binding of bilirubin. Biochem. J. 171: 453—459. PMID 656055 DOI:10.1042/bj1710453
Примітки[ред. | ред. код]
- ↑ Захворювання, генетично пов'язані з Альбумін переглянути/редагувати посилання на ВікіДаних.
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:399 (англ.) . Архів оригіналу за 14 жовтня 2017. Процитовано 30 січня 2017.
- ↑ UniProt, P02768 (англ.) . Архів оригіналу за 6 лютого 2017. Процитовано 30 січня 2017.
Див. також[ред. | ред. код]
| Це незавершена стаття про білки. Ви можете допомогти проєкту, виправивши або дописавши її. |