Ротавірусна інфекція
| Ротавірусна інфекція | |
|---|---|
 Ротавірус A у фекаліях зараженої дитини | |
| Спеціальність | інфекційні хвороби, педіатрія і інтенсивна терапія[d] |
| Симптоми | діарея, зневоднення організму, дегідратаційний шок і блювання |
| Причини | Rotavirus |
| Метод діагностики | фізикальне обстеження і ІФА |
| Ведення | оральна регідратаційна терапія і внутрішньовенне заміщення рідиниd |
| Класифікація та зовнішні ресурси | |
| МКХ-11 | 1A22 |
| МКХ-10 | A08.0 |
| DiseasesDB | 11667 |
| MedlinePlus | 000252 |
| eMedicine | emerg/401 |
| MeSH | D012400 |
Ротаві́русна інфе́кція (англ. Rotaviral enteritis — ротавірусний ентерит) — інфекційна хвороба вірусного походження, яка перебігає з тяжкою діареєю. Є найчастішою причиною тяжкої діареї, нерідко смертельної, у немовлят і маленьких дітей[1].
Майже кожна дитина у світі до досягнення п'яти років заражається ротавірусом принаймні один раз.[2] Однак з кожним зараженням імунітет зростає, і наступні зараження є менш жорсткими; дорослі рідко хворіють на цю хворобу.[3] Існує п'ять видів ротавірусу, які називають A, B, C, D та E.[4] Найпоширенішим є ротавірус A — він є причиною понад 90 % випадків заражень людини.
Історичні відомості[ред. | ред. код]
У 1943 році Яків Лайт і Горацій Ходс довели, що фільтрівний агент у фекаліях дітей з інфекційною діареєю також спричинює її у великої рогатої худоби.[5] Через три десятиліття на збережених зразках агента показано, що то був ротавірус.[6] У наступні роки було доведено, що вірус у мишей[7] пов'язаний з вірусом, який спричинює діарею.[8] У 1973 році Рут Бішоп і її колеги описали зв'язок вірусів, які вони виявили у дітей, з гастроентеритом.[9]
У 1974 році Томас Генрі Флюветт запропонував назву ротавірус після того, як побачив через електронний мікроскоп, що ротавірусна частинка нагадує колесо (лат. rota)[10][11]; назва була офіційно визнана Міжнародним комітетом з таксономії вірусів через чотири роки.[12] У 1976 році такі віруси були описані у декількох інших видів тварин[8]. Ці віруси, які спричинюють гострий гастроентерит, були визнані патогеном, який уражає як людей, так і тварин у всьому світі.[10] Серотипи ротавірусу були вперше описані в 1980 році,[13] а в наступному році, ротавірус від людей був вперше вирощений в клітинних культурах, отриманих з нирки мавпи, шляхом додавання трипсину (фермент, виявлений в дванадцятипалій кишці ссавців, і, як тепер відомо, необхідний для реплікації ротавірусу) в культуральному середовищі.[14]
Можливість вирощення ротавірусу в культурі прискорила темпи досліджень, і до середини 1980-х перші кандидати у вакцини почали випробовування.[15] У 1998 році ротавірусна вакцина була ліцензована для використання в США. Клінічні дослідження в США, Фінляндії та Венесуелі виявили, що вона від 80 до 100 % ефективна в запобіганні гострої діареї, спричиненої ротавірусною інфекцією, і дослідники не виявили статистично значущих серйозних побічних ефектів.[16][17] Однак виробник зняв її з ринку в 1999 році, після того, як було виявлено, що вакцина, можливо, сприяла підвищеному ризику інвагінації, типу кишкової непрохідності, в одного з кожних 12 000 вакцинованих дітей.[18] Цей досвід спровокував напружені дебати про відносні ризики і переваги ротавірусної вакцини.[19] У 2006 році було продемонстровано, що дві нових вакцини проти ротавірусу А є безпечними і ефективними у дітей,[20] і в червні 2009 року Всесвітня організація охорони здоров'я рекомендувала включити вакцинацію проти ротавірусної інфекції у всі національні програми імунізації для забезпечення захисту від цього вірусу.[21] Вірус передається фекально-оральним механізмом передачі інфекції. Він заражає і пошкоджує ентероцити, які вистилають тонку кишку і спричинює гастроентерит (який часто називають «шлунковим грипом» попри те, що хвороба не має ніякого відношення до грипу). Хоча ротавірус був виявлений в 1973 році[9] і спричинює до 50 % випадків госпіталізацій з тяжкою діареєю у немовлят і дітей[22], його значення ще не широко відомо у спільноті охорони суспільного здоров'я, особливо в країнах, що розвиваються[23] На додаток до його впливу на здоров'я людини, ротавірусна інфекція також заражає тварин, і є патогеном для свійської худоби[24].
Актуальність[ред. | ред. код]

Ротавірус А, на частку якого припадає понад 90 % випадків ротавірусного гастроентериту у людини[25] є ендемічним по всьому світу. Кожен рік ротавірус спричинює мільйони випадків діареї в країнах, які розвиваються, майже 2 млн з яких приводять до госпіталізації[23] і приблизно 453 тисяч призводять до смерті дітей віком менше п'яти років.[26] Це близько 40 % усіх госпіталізацій, пов'язаних з діареєю у дітей у віці до п'яти років у всьому світі.[27]
В одних тільки Сполучених Штатах Америки — до початку програми вакцинації ротавірусу[28] — щорічно фіксували понад 2,7 млн випадків ротавірусного гастроентериту, з них 60 000 дітей госпіталізували і 37 із них померли від тяжкого зневоднення.[29] Велику роль ротавірусної інфекції у виникненні діареї не визнають багато працівників охорони громадського здоров'я,[30] особливо в країнах, які розвиваються[23], хоча майже кожна дитина була заражена ротавірусом до досягнення п'ятирічного віку[31] і ця інфекція є провідною причиною тяжкої діареї у немовлят і дітей (припадає близько 20 % випадків захворювань, і 50 % випадків, які потребували госпіталізації)[23]. Ротавірус спричинює 37 % випадків смерті внаслідок діареї і 5 % усіх смертей серед дітей віком до п'яти років[26]. Хворі на ротавірусну інфекцію хлопчики в два рази частіше за дівчаток потрапляють у лікарню.[22][32] Ротавірусна інфекція частіше розвивається під час холодних, сухих сезонів[33]. А от кількість випадків ротавірусної інфекції, які виникли через забруднення харчових продуктів, невідома.[34]
Спалахи діареї, яку спричинив ротавірус А, широко поширені серед госпіталізованих немовлят, дітей молодшого віку, які відвідують дитячі садки, і людей похилого віку в будинках престарілих.[35] У 2005 році найбільша за кількістю захворілих зареєстрована епідемія ротавірусного гастроентериту сталася в Нікарагуа. Цей надзвичайно великий і серйозний спалах був пов'язаний з мутаціями геному ротавірусу А, які можливо, допомогли вірусу подолати популяційний імунітет населення.[36] Аналогічний великий спалах відбувся в Бразилії 1977 року.[37]
Ротавірус B, який також має назву «ротавірус діареї дорослих» (ADRV), був причиною великих епідемій тяжкої діареї у тисячі людей різного віку в Китаї. Ці епідемії виникли через забруднення питної води стічними водами.[38][39] Спалахи ротавірусної інфекції також відбувалися в Індії 1998 року; каузативний штам був названий CAL і, на відміну від ADRV, цей штам є ендемічним.[40][41] Поки що епідемії, спричинені ротавірусом B, були обмежені материковим Китаєм, але обстеження вказують на відсутність імунітету до цього різновиду в інших країнах.[42] Ротавірусна інфекція зазвичай є легко керованим дитячим захворюванням, але у всьому світі майже 500 000 дітей у віці до п'яти років досі щорічно вмирають від неї[26], а майже два мільйони тяжко хворіють на неї.[23] У Сполучених Штатах, до початку програми вакцинації від ротавірусу, він щорічно спричиняв близько 2,7 млн випадків гострого гастроентериту в дітей, майже 60 000 госпіталізацій і близько 37 смертей[29] Кампанії охорони громадського здоров'я по боротьбі з ротавірусом зосереджуються на наданні пероральної регідратаційної терапії для інфікованих дітей та вакцинації, щоб запобігти захворюванню.[43] Частота і тяжкість ротавірусної інфекції значно знизились в країнах, які додали ротавірусну вакцину в свої звичайні протоколи дитячих щеплень.[44][45]
Етіологія[ред. | ред. код]
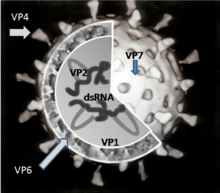
Причиною ротавірусної інфекції є різні види дволанцюжково-РНК вмістного роду Ротавірус родини Reoviridae. Ротавіруси стійкі в навколишньому середовищі й були знайдені в зразках води з гирла річок на рівні 0,26-1,3 інфекційних частинок на літр.[46] Санітарні заходи, достатні для усунення бактерій і паразитів, ймовірно є неефективними в контролі ротавірусу, оскільки поширеність ротавірусної інфекції у країнах з високими і низькими санітарними нормами схожа.[1]
Розмноження вірусу[ред. | ред. код]
Ротавіруси розмножуються в основному в кишці[47] і заражають ентероцити ворсинок у тонкій кишці, приводячи до структурних і функціональних змін епітелію.[48] Потрійна білкова оболонка робить їх стійкими до кислої PH шлунка і травних ферментів в кишцв.
Вірус проникає в клітини шляхом рецептор-опосередкованого ендоцитозу і утворює пухирець, відомий як ендосома. Білки третьої оболонки (VP7 і шип VP4) порушують мембрану ендосом, створюючи різницю в концентрації кальцію. Це спричинює руйнування тримерів VP7 на прості білкові субодиниці, залишаючи оболонки білків VP2 та VP6 навколо дволанцюжкової РНК (англ. dsRNA) вірусу, утворюючи дво-оболонкову частинку (англ. double-layered particle, DLP).[49]
Одинадцять ланцюжків дволанцюжкової РНК залишаються під захистом двох білкових оболонок, а вірусна РНК-залежна РНК-полімераза створює мРНК-записи дволанцюжкового вірусного генома. Залишаючись в ядрі, вірусна РНК ухиляється від вродженої імунної реакції, яка має назву РНК-інтерференції і зумовлюється наявністю дволанцюжкової РНК.
Під час інфекції, ротавірус виробляє мРНК і для біосинтезу білка, і для реплікації генів. Більшість ротавірусних білків накопичуються у віроплазмі, де реплікується РНК і збираються дво-оболонкові частинки. Віроплазма формується навколо клітинного ядра вже через дві години після зараження, і складається з вірусних фабрик, які, ймовірно, утворені двома вірусними неструктурними білками: NSP5 і NSP2. Інгібування NSP5 РНК-інтерференцією призводить до різкого зниження реплікації ротавірусу. Дво-оболонкові частинки мігрують до ендоплазматичного ретикулуму, де вони отримують свою третю, зовнішню оболонку (сформовану VP7 і VP4). Вірусне потомство виходить з клітини шляхом лізису.[50][51][52]
Види роду Ротавірус[ред. | ред. код]
Існує п'ять видів роду ротавірусу, які називають A, B, C, D та E. Люди переважно заражаються видами A, B і C, найчастіше видом А. Всі п'ять видів спричинюють захворювання у тварин.[53] Відомі різні штами ротавірусу А, так звані серотипи.[54] Як і для вірусу грипу, подвійна система класифікації використовується на основі двох білків на поверхні вірусу. Глікопротеїн VP7 визначає серотипи G, а протеазо-чутливий білок VP4 визначає серотипи P.[55] Оскільки два гени, які визначають G-типи і P-типи, можуть окремо передаватись потомству вірусів, відомі різні комбінації.[56]
Епідеміологічні особливості[ред. | ред. код]
Ротавірус передається фекально-оральним механізмом передачі інфекції, через контакт із забрудненими руками, поверхнями і об'єктами,[57] і, можливо, через виділення з поверхні епітелію ротоглотки з дихальним секретом.[1] Фекалії інфікованої людини можуть містити більше 10 трильйонів інфекційних частинок на грам;[58] і менше, ніж 100 з них, потрібні для передачі інфекції іншій людині.[3]
Патогенез[ред. | ред. код]

Діарею спричиняють декілька видів вірусу. Мальабсорбція виникає через руйнування клітин тонкої кишки — ентероцитів. Токсичний білок ротавірусу NSP4 індукує секрецію і кальцєвих іон-залежних хлоридів, порушує реабсорбцію води за допомогою SGLT1-транспортера, швидше за все знижує активність дісахарідазу граничних клітин ворсинок і, можливо, активує кальцій-іон-залежні секреторні рефлекси ентеральної нервової системи.[59] Здорові ентероцити секретують лактазу в тонкій кишці; непереносність молока внаслідок лактазної недостатності є симптомом ротавірусної інфекції,[60] який може зберігатися протягом тижнів.[61] Часто за поверненням молока в раціон дитини слідує повторення помірної діареї внаслідок бактеріальної ферментації дисахариду лактози в тонкій кишці[62].
Клінічні прояви[ред. | ред. код]
Ротавірусний гастроентерит є захворюванням, яке характеризується блюванням, водянистою діареєю і субфебрильним підвищенням температури тіла. Після зараження дитини вірусом, інкубаційний період до появи симптомів триває близько двох днів[63]. Хвороба часто починається з блювання, потім приєднується рясна діарея протягом чотирьох-восьми днів. Зневоднення є більш поширеним при ротавірусній інфекції, ніж у більшості тих, які спричинюють патогенні бактерії, і є найбільш частою причиною смерті при ротавірусній інфекції[64]. Зараження ротавірусом А може відбуватися протягом усього життя: перші зараження зазвичай є симптомними, але наступні інфекції, як правило, легкі або безсимптомні,[58][65] оскільки імунна система забезпечує деякий захист.[66][67] Відповідно, відсоток симптоматичного поширення інфекції є найбільш високим у дітей віком до двох років і поступово зменшуються у бік 45-річного віку.[68] Інфекція у новонароджених дітей, хоча і часто відбувається, часто аперебігає з легко або безсимптомно;[3] найбільш тяжкі прояви зазвичай виникають у дітей від шести місяців до двох років, літніх людей, і тих, у кого порушена або відсутня імунна система. За рахунок імунітету, придбаного в дитинстві, більшість дорослих несприйнятливі до ротавірусної інфекції; гастроентерит у дорослих зазвичай має інші причини, ніж ротавірусну, але безсимптомні інфекції у дорослих можуть підтримувати передачу ротавірусної інфекції в популяції.[69]
Діагностика[ред. | ред. код]
У більшості дітей, які потрапляють у лікарню з гастроентеритом, проводиться дослідження на ротавірус А.[70][71] Специфічна діагностика ротавірусної інфекції включає виявлення антигенів ротавірусу в дитячих фекаліях шляхом імуноферментного аналізу. На світовому ринку існує кілька ліцензованих тестових наборів, які є чутливими, специфічними і виявляють усі серотипи ротавірусу А.[72] Інші методи, такі як електронна мікроскопія та ПЛР, використовуються в науково-дослідних лабораторіях.[66] Зворотна транскрипція-полімеразна ланцюгова реакція (зт-ПЛР, англ. Reverse transcription-polymerase chain reaction) дозволяє виявити та ідентифікувати всі види і серотипи ротавірусу людини.[73]
Лікування[ред. | ред. код]
Лікування гострої ротавірусної інфекції є неспецифічним патогенетичним, включає компенсацію зневоднення, підтримку гідратації на належному рівні[43]. За відсутності такого лікування, дитина може загинути внаслідок дегідратаційного шоку.[74] Залежно від тяжкості лікування складається або з оральної регідратації, протягом якої дитина отримує додаткову воду для пиття, яка містить необхідні кількості солей і сахарози[75], або з внутрішньовенного введення відповідних сольових розчинів та введення оральних сумішей через назогастральний зонд. Здійснюють контроль електролітів і глюкози в крові дитини.[70] Антибіотики не рекомендують.
Ротавірусна інфекція рідко спричинює ускладнення і для дитини при адекватному лікуванні та нагляді прогноз для життя позитивний.[76]
Профілактика[ред. | ред. код]
Оскільки поліпшення санітарних умов не знижує захворюваність на ротавірусну інфекцію, а рівень госпіталізації залишається високим, попри використання препаратів оральної регідратації, основним запобіжним заходом є вакцинація.[2] На світовому ринку дві ротавірусні вакцини проти ротавірусної інфекції вважаються безпечними та ефективними для дітей:[45] Rotarix від GlaxoSmithKline[77] і RotaTeq від Merck & Co.[78] Обидві вони приймаються орально і містять ослаблений живий вірус.[45]
Ротавірусні вакцини ліцензовані у понад 100 країнах, але тільки в 17 країнах введена рутинна вакцинація від ротавірусної інфекції.[79] Після введення рутинної вакцинації проти ротавірусної інфекції у США у 2006 році, «вплив на суспільне здоров'я ротавірусного гастроентериту швидко і різко скорочуються», попри нижчі рівні охоплення порівняно з іншою регулярною імунізацією дітей.[80] Клінічні випробування ротавірусної вакцини Rotarix у Південній Африці та Малаві, виявили, що вакцина сприяє значному зменшенню числа випадків тяжкої діареї, яку спричинює ротавірус.[81] Кокранівський огляд 2012 року 41 клінічного випробування, які охоплювали 186 263 учасників, дійшов висновку, що Rotarix і RotaTeq є ефективними вакцинами.[82] Інші ротавірусні вакцини перебувають на стадії розробки.[83] Всесвітня організація охорони здоров'я (ВООЗ) рекомендує внесення ротавірусної вакцини до усіх національних програм імунізації.[84] Частота і тяжкість ротавірусної інфекції значно знизилося в країнах, які виконали цю рекомендацію.[44][45]
"Rotavirus Vaccine Program" є співпрацею між PATH, ВООЗ і Центрами контролю і профілактики захворювань США і фінансується "GAVI Alliance". Програма спрямована на зниження дитячої захворюваності та смертності від діарейних хвороб шляхом забезпечення доступності вакцини проти ротавірусу для використання в країнах, які розвиваються.[85]
Ротавірусні хвороби у тварин[ред. | ред. код]
Ротавіруси уражають молодняк багатьох видів тварин і вони є однією з основних причин діареї у диких і свійських тварин по всьому світу.[24] Як патоген свійської худоби, особливо у малих телят і поросят, ротавіруси зумовлюють економічні втрати фермерів за рахунок витрат на лікування, пов'язаних з високою захворюваністю і смертністю.[86] Ці ротавіруси є потенційним резервуаром для генетичного обміну з ротавірусами людини.[86] Існують певні докази, що ротавіруси тварин можуть заразити людей, або шляхом прямої передачі вірусу, або шляхом внесення одного або декількох сегментів РНК до реасортименту з ланцюжками ротавірусів людини.[87][88]
Примітки[ред. | ред. код]
- ↑ а б в Dennehy PH (2000). Transmission of rotavirus and other enteric pathogens in the home. Pediatr. Infect. Dis. J. 19 (10 Suppl): S103—5. doi:10.1097/00006454-200010001-00003. PMID 11052397.
- ↑ а б Bernstein DI (March 2009). Rotavirus overview. The Pediatric Infectious Disease Journal. 28 (3 Suppl): S50—3. doi:10.1097/INF.0b013e3181967bee. PMID 19252423. Архів оригіналу за 11 травня 2013. Процитовано 25 серпня 2016.
- ↑ а б в Grimwood K, Lambert SB (February 2009). Rotavirus vaccines: opportunities and challenges. Human Vaccines. 5 (2): 57—69. doi:10.4161/hv.5.2.6924. PMID 18838873. Архів оригіналу за 15 вересня 2019. Процитовано 24 серпня 2016.
- ↑ ICTV Virus Taxonomy: 2009 Release. Архів оригіналу за 4 жовтня 2013. Процитовано 24 серпня 2016.
- ↑ Light JS, Hodes HL (1943). Studies on epidemic diarrhea of the new-born: Isolation of a Filtrable Agent Causing Diarrhea in Calves. Am. J. Public Health Nations Health. 33 (12): 1451—4. doi:10.2105/AJPH.33.12.1451. PMC 1527675. PMID 18015921.
- ↑ Mebus CA, Wyatt RG, Sharpee RL та ін. (1 серпня 1976). Diarrhea in gnotobiotic calves caused by the reovirus-like agent of human infantile gastroenteritis. Infect. Immun. 14 (2): 471—4. PMC 420908. PMID 184047. Архів оригіналу (PDF) за 29 вересня 2011. Процитовано 26 серпня 2016.
- ↑ Rubenstein D, Milne RG, Buckland R, Tyrrell DA (1971). The growth of the virus of epidemic diarrhoea of infant mice (EDIM) in organ cultures of intestinal epithelium. British journal of experimental pathology. 52 (4): 442—45. PMC 2072337. PMID 4998842.
- ↑ а б Woode GN, Bridger JC, Jones JM, Flewett TH, Davies HA, Davis HA, White GB (1 вересня 1976). Morphological and antigenic relationships between viruses (rotaviruses) from acute gastroenteritis in children, calves, piglets, mice, and foals. Infect. Immun. 14 (3): 804—10. PMC 420956. PMID 965097. Архів оригіналу (PDF) за 29 вересня 2011. Процитовано 26 серпня 2016.
- ↑ а б Bishop R (October 2009). Discovery of rotavirus: Implications for child health. Journal of Gastroenterology and Hepatology. 24 (Suppl 3): S81—5. doi:10.1111/j.1440-1746.2009.06076.x. PMID 19799704. Архів оригіналу за 15 вересня 2019. Процитовано 26 серпня 2016.
- ↑ а б Flewett TH, Woode GN (1978). The rotaviruses. Arch. Virol. 57 (1): 1—23. doi:10.1007/BF01315633. PMID 77663.
- ↑ Flewett TH, Bryden AS, Davies H, Woode GN, Bridger JC, Derrick JM (1974). Relation between viruses from acute gastroenteritis of children and newborn calves. Lancet. 2 (7872): 61—3. doi:10.1016/S0140-6736(74)91631-6. PMID 4137164.
- ↑ Matthews RE (1979). Third report of the International Committee on Taxonomy of Viruses. Classification and nomenclature of viruses. Intervirology. 12 (3–5): 129—296. doi:10.1159/000149081. PMID 43850.
- ↑ Beards GM, Brown DW (March 1988). The antigenic diversity of rotaviruses: significance to epidemiology and vaccine strategies. European Journal of Epidemiology. 4 (1): 1—11. doi:10.1007/BF00152685. PMID 2833405.
- ↑ Urasawa T, Urasawa S, Taniguchi K (1981). Sequential passages of human rotavirus in MA-104 cells. Microbiol. Immunol. 25 (10): 1025—35. doi:10.1111/j.1348-0421.1981.tb00109.x. PMID 6273696.
- ↑ Ward RL, Bernstein DI (January 2009). Rotarix: a rotavirus vaccine for the world. Clinical Infectious Diseases. 48 (2): 222—8. doi:10.1086/595702. PMID 19072246. Архів оригіналу за 4 червня 2020. Процитовано 26 серпня 2016.
- ↑ Rotavirus vaccine for the prevention of rotavirus gastroenteritis among children. Recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep. 48 (RR–2): 1—20. 1999. PMID 10219046.
- ↑ Kapikian AZ (2001). A rotavirus vaccine for prevention of severe diarrhoea of infants and young children: development, utilization and withdrawal. Novartis Found. Symp. Novartis Foundation Symposia. 238: 153—71, discussion 171–9. doi:10.1002/0470846534.ch10. ISBN 9780470846537. PMID 11444025.
- ↑ Bines JE (2005). Rotavirus vaccines and intussusception risk. Curr. Opin. Gastroenterol. 21 (1): 20—5. PMID 15687880. Архів оригіналу за 11 травня 2013. Процитовано 26 серпня 2016.
- ↑ Bines J (2006). Intussusception and rotavirus vaccines. Vaccine. 24 (18): 3772—6. doi:10.1016/j.vaccine.2005.07.031. PMID 16099078.
- ↑ Dennehy PH (2008). Rotavirus vaccines: an overview. Clin. Microbiol. Rev. 21 (1): 198—208. doi:10.1128/CMR.00029-07. PMC 2223838. PMID 18202442. Архів оригіналу за 28 вересня 2011. Процитовано 26 серпня 2016.
- ↑ Meeting of the immunization Strategic Advisory Group of Experts, April 2009—conclusions and recommendations. Relevé Épidémiologique Hebdomadaire / Section D'hygiène Du Secrétariat De La Société Des Nations = Weekly Epidemiological Record / Health Section of the Secretariat of the League of Nations. 84 (23): 220—36. June 2009. PMID 19499606.[1] [Архівовано 27 жовтня 2013 у Wayback Machine.]
- ↑ а б Rheingans RD, Heylen J, Giaquinto C (2006). Economics of rotavirus gastroenteritis and vaccination in Europe: what makes sense?. Pediatr. Infect. Dis. J. 25 (1 Suppl): S48—55. doi:10.1097/01.inf.0000197566.47750.3d. PMID 16397429.
- ↑ а б в г д Simpson E, Wittet S, Bonilla J, Gamazina K, Cooley L, Winkler JL (2007). Use of formative research in developing a knowledge translation approach to rotavirus vaccine introduction in developing countries. BMC Public Health. 7: 281. doi:10.1186/1471-2458-7-281. PMC 2173895. PMID 17919334. Архів оригіналу за 24 вересня 2015. Процитовано 25 серпня 2016.
{{cite journal}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ а б Edward J Dubovi; Nigel James MacLachlan (2010). Fenner's Veterinary Virology, Fourth Edition. Boston: Academic Press. с. 288. ISBN 0-12-375158-6.
- ↑ Leung AK, Kellner JD, Davies HD (2005). Rotavirus gastroenteritis. Adv. Ther. 22 (5): 476—87. doi:10.1007/BF02849868. PMID 16418157.
- ↑ а б в Tate JE, Burton AH, Boschi-Pinto C, Steele AD, Duque J, Parashar UD (February 2012). 2008 estimate of worldwide rotavirus-associated mortality in children younger than 5 years before the introduction of universal rotavirus vaccination programmes: a systematic review and meta-analysis. Lancet Infect Dis. 12 (2): 136—141. doi:10.1016/S1473-3099(11)70253-5. PMID 22030330.
- ↑ UNICEF/WHO (2009) «Diarrhoea: Why children are still dying and what can be done.» Retrieved 23 May 2010 (PDF). Архів оригіналу (PDF) за 19 жовтня 2013. Процитовано 24 серпня 2016.
- ↑ Centers for Disease Control and Prevention (CDC) (October 2009). Reduction in rotavirus after vaccine introduction—United States, 2000–2009. MMWR. Morbidity and Mortality Weekly Report. 58 (41): 1146—9. PMID 19847149. Архів оригіналу за 31 жовтня 2009. Процитовано 20 грудня 2009.
- ↑ а б Fischer TK, Viboud C, Parashar U та ін. (2007). Hospitalizations and deaths from diarrhea and rotavirus among children <5 years of age in the United States, 1993–2003. J. Infect. Dis. 195 (8): 1117—25. doi:10.1086/512863. PMID 17357047.
- ↑ Rodrigo C, Salman N, Tatochenko V, Mészner Z, Giaquinto C (May 2010). Recommendations for rotavirus vaccination: A worldwide perspective. Vaccine. 28 (31): 5100—8. doi:10.1016/j.vaccine.2010.04.108. PMID 20472032.
- ↑ Parashar UD, Gibson CJ, Bresse JS, Glass RI (2006). Rotavirus and severe childhood diarrhea. Emerging Infect. Dis. 12 (2): 304—6. doi:10.3201/eid1202.050006. PMC 3373114. PMID 16494759.
- ↑ Ryan MJ, Ramsay M, Brown D, Gay NJ, Farrington CP, Wall PG (1996). Hospital admissions attributable to rotavirus infection in England and Wales. J. Infect. Dis. 174 Suppl 1: S12—8. doi:10.1093/infdis/174.Supplement_1.S12. PMID 8752285.
- ↑ Levy K, Hubbard AE, Eisenberg JN (December 2009). Seasonality of rotavirus disease in the tropics: a systematic review and meta-analysis. International Journal of Epidemiology. 38 (6): 1487—96. doi:10.1093/ije/dyn260. PMC 2800782. PMID 19056806. Архів оригіналу за 15 вересня 2019. Процитовано 25 серпня 2016.
- ↑ Koopmans M, Brown D (1999). Seasonality and diversity of Group A rotaviruses in Europe. Acta Paediatrica Supplement. 88 (426): 14—9. doi:10.1111/j.1651-2227.1999.tb14320.x. PMID 10088906.
- ↑ Anderson EJ, Weber SG (February 2004). Rotavirus infection in adults. The Lancet Infectious Diseases. 4 (2): 91—9. doi:10.1016/S1473-3099(04)00928-4. PMID 14871633. Архів оригіналу за 10 червня 2018. Процитовано 25 серпня 2016.
- ↑ Bucardo F, Karlsson B, Nordgren J та ін. (2007). Mutated G4P[8] rotavirus associated with a nationwide outbreak of gastroenteritis in Nicaragua in 2005. J. Clin. Microbiol. 45 (3): 990—7. doi:10.1128/JCM.01992-06. PMC 1829148. PMID 17229854. Архів оригіналу за 27 вересня 2011. Процитовано 25 серпня 2016.
- ↑ Linhares AC, Pinheiro FP, Freitas RB, Gabbay YB, Shirley JA, Beards GM (1981). An outbreak of rotavirus diarrhea among a non-immune, isolated South American Indian community. Am. J. Epidemiol. 113 (6): 703—10. PMID 6263087.
- ↑ Hung T, Chen GM, Wang CG та ін. (1984). Waterborne outbreak of rotavirus diarrhea in adults in China caused by a novel rotavirus. Lancet. 1 (8387): 1139—42. doi:10.1016/S0140-6736(84)91391-6. PMID 6144874.
- ↑ Fang ZY, Ye Q, Ho MS та ін. (1989). Investigation of an outbreak of adult diarrhea rotavirus in China. J. Infect. Dis. 160 (6): 948—53. doi:10.1093/infdis/160.6.948. PMID 2555422.
- ↑ Kelkar SD, Zade JK (2004). Group B rotaviruses similar to strain CAL-1, have been circulating in Western India since 1993. Epidemiol. Infect. 132 (4): 745—9. doi:10.1017/S0950268804002171. PMC 2870156. PMID 15310177.
- ↑ Ahmed MU, Kobayashi N, Wakuda M, Sanekata T, Taniguchi K, Kader A, Naik TN, Ishino M, Alam MM, Kojima K, Mise K, Sumi A (2004). Genetic analysis of group B human rotaviruses detected in Bangladesh in 2000 and 2001. J. Med. Virol. 72 (1): 149—55. doi:10.1002/jmv.10546. PMID 14635024.
- ↑ Penaranda ME, Ho MS, Fang ZY та ін. (1 жовтня 1989). Seroepidemiology of adult diarrhea rotavirus in China, 1977 to 1987. J. Clin. Microbiol. 27 (10): 2180—3. PMC 266989. PMID 2479654. Архів оригіналу (PDF) за 27 вересня 2011. Процитовано 25 серпня 2016.
- ↑ а б Diggle L (2007). Rotavirus diarrhoea and future prospects for prevention. Br. J. Nurs. 16 (16): 970—4. PMID 18026034.
- ↑ а б Giaquinto C, Dominiak-Felden G, Van Damme P, Myint TT, Maldonado YA, Spoulou V, Mast TC, Staat MA (July 2011). Summary of effectiveness and impact of rotavirus vaccination with the oral pentavalent rotavirus vaccine: a systematic review of the experience in industrialized countries. Human Vaccines. 7 (7): 734—48. doi:10.4161/hv.7.7.15511. PMID 21734466. Архів оригіналу за 4 травня 2020. Процитовано 25 серпня 2016.
- ↑ а б в г Jiang V, Jiang B, Tate J, Parashar UD, Patel MM (July 2010). Performance of rotavirus vaccines in developed and developing countries. Human Vaccines. 6 (7): 532—42. doi:10.4161/hv.6.7.11278. PMC 3322519. PMID 20622508. Архів оригіналу за 4 червня 2020. Процитовано 25 серпня 2016.
- ↑ Rao VC, Seidel KM, Goyal SM, Metcalf TG, Melnick JL (1 серпня 1984). Isolation of enteroviruses from water, suspended solids, and sediments from Galveston Bay: survival of poliovirus and rotavirus adsorbed to sediments. Appl. Environ. Microbiol. 48 (2): 404—9. PMC 241526. PMID 6091548. Архів оригіналу (PDF) за 27 вересня 2011. Процитовано 24 серпня 2016.
- ↑ Greenberg HB, Estes MK (May 2009). Rotaviruses: from pathogenesis to vaccination. Gastroenterology. 136 (6): 1939—51. doi:10.1053/j.gastro.2009.02.076. PMC 3690811. PMID 19457420.
- ↑ Greenberg HB, Clark HF, Offit PA (1994). Rotavirus pathology and pathophysiology. Curr. Top. Microbiol. Immunol. 185: 255—83. PMID 8050281.
- ↑ Baker M, Prasad BV (2010). Rotavirus cell entry. Current Topics in Microbiology and Immunology. Current Topics in Microbiology and Immunology. 343: 121—48. doi:10.1007/82_2010_34. ISBN 978-3-642-13331-2. PMID 20397068.
- ↑ Jayaram H, Estes MK, Prasad BV (2004). Emerging themes in rotavirus cell entry, genome organization, transcription and replication. Virus Res. 101 (1): 67—81. doi:10.1016/j.virusres.2003.12.007. PMID 15010218.
- ↑ Patton JT, Vasquez-Del Carpio R, Spencer E (2004). Replication and transcription of the rotavirus genome. Curr. Pharm. Des. 10 (30): 3769—77. doi:10.2174/1381612043382620. PMID 15579070.
- ↑ Ruiz MC, Leon T, Diaz Y, Michelangeli F (2009). Molecular biology of rotavirus entry and replication. TheScientificWorldJournal. 9: 1476—97. doi:10.1100/tsw.2009.158. PMID 20024520.
{{cite journal}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ Kirkwood CD (September 2010). Genetic and antigenic diversity of human rotaviruses: potential impact on vaccination programs. The Journal of Infectious Diseases. 202 (Suppl): S43—8. doi:10.1086/653548. PMID 20684716.
- ↑ O'Ryan M (March 2009). The ever-changing landscape of rotavirus serotypes. The Pediatric Infectious Disease Journal. 28 (3 Suppl): S60—2. doi:10.1097/INF.0b013e3181967c29. PMID 19252426.
- ↑ Patton JT (January 2012). Rotavirus diversity and evolution in the post-vaccine world. Discovery Medicine. 13 (68): 85—97. PMC 3738915. PMID 22284787. Архів оригіналу за 23 вересня 2015. Процитовано 24 серпня 2016.
- ↑ Desselberger U, Wolleswinkel-van den Bosch J, Mrukowicz J, Rodrigo C, Giaquinto C, Vesikari T (2006). Rotavirus types in Europe and their significance for vaccination. Pediatr. Infect. Dis. J. 25 (1 Suppl.): S30—41. doi:10.1097/01.inf.0000197707.70835.f3. PMID 16397427. Архів оригіналу за 11 травня 2013. Процитовано 24 серпня 2016.
- ↑ Butz AM, Fosarelli P, Dick J, Cusack T, Yolken R (1993). Prevalence of rotavirus on high-risk fomites in day-care facilities. Pediatrics. 92 (2): 202—5. PMID 8393172.
- ↑ а б Bishop RF (1996). Natural history of human rotavirus infection. Arch. Virol. Suppl. 12: 119—28. PMID 9015109.
- ↑ Gregorini, L; Marco, J; Bernies, M; Cassagneau, B; Pomidossi, G; Anguissola, GB; Fajadet, J (15 квітня 1997). The alpha-1 adrenergic blocking agent urapidil counteracts postrotational atherectomy "elastic recoil" where nitrates have failed. The American journal of cardiology. 79 (8): 1100—3. doi:10.1016/S0002-9149(97)00053-2. PMID 9114772.
- ↑ Farnworth ER (June 2008). The evidence to support health claims for probiotics. The Journal of Nutrition. 138 (6): 1250S—4S. PMID 18492865. Архів оригіналу за 15 вересня 2019. Процитовано 24 серпня 2016.
- ↑ Ouwehand A, Vesterlund S (2003). Health aspects of probiotics. IDrugs. 6 (6): 573—80. PMID 12811680.
- ↑ Arya SC (1984). Rotaviral infection and intestinal lactase level. J. Infect.Dis. 150 (5): 791. doi:10.1093/infdis/150.5.791. PMID 6436397.
- ↑ Hochwald C, Kivela L (1999). Rotavirus vaccine, live, oral, tetravalent (RotaShield). Pediatr. Nurs. 25 (2): 203—4, 207. PMID 10532018.
- ↑ Maldonado YA, Yolken RH (1990). Rotavirus. Baillieres Clin. Gastroenterol. 4 (3): 609—25. doi:10.1016/0950-3528(90)90052-I. PMID 1962726.
- ↑ Glass RI, Parashar UD, Bresee JS, Turcios R, Fischer TK, Widdowson MA, Jiang B, Gentsch JR (July 2006). Rotavirus vaccines: current prospects and future challenges. Lancet. 368 (9532): 323—32. doi:10.1016/S0140-6736(06)68815-6. PMID 16860702.
- ↑ а б Goode, Jamie; Chadwick, Derek (2001). Gastroenteritis viruses. New York: Wiley. с. 14. ISBN 0-471-49663-4.
- ↑ Ward R (March 2009). Mechanisms of protection against rotavirus infection and disease. The Pediatric Infectious Disease Journal. 28 (3 Suppl): S57—9. doi:10.1097/INF.0b013e3181967c16. PMID 19252425.
- ↑ Ramsay M, Brown D (2000). Desselberger, U.; Gray, James (ред.). Rotaviruses: methods and protocols. Totowa, NJ: Humana Press. с. 217. ISBN 0-89603-736-3.
- ↑ Hrdy DB (1987). Epidemiology of rotaviral infection in adults. Rev. Infect. Dis. 9 (3): 461—9. doi:10.1093/clinids/9.3.461. PMID 3037675.
- ↑ а б Patel MM, Tate JE, Selvarangan R та ін. (2007). Routine laboratory testing data for surveillance of rotavirus hospitalizations to evaluate the impact of vaccination. Pediatr. Infect. Dis. J. 26 (10): 914—9. doi:10.1097/INF.0b013e31812e52fd. PMID 17901797.
- ↑ The Pediatric ROTavirus European CommitTee (PROTECT) (2006). The paediatric burden of rotavirus disease in Europe. Epidemiol. Infect. 134 (5): 908—16. doi:10.1017/S0950268806006091. PMC 2870494. PMID 16650331.
- ↑ Angel J, Franco MA, Greenberg HB (2009). Mahy WJ and Van Regenmortel MHV (ред.). Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. с. 278. ISBN 0-12-375147-0.
- ↑ Fischer TK, Gentsch JR (2004). Rotavirus typing methods and algorithms. Reviews in Medical Virology. 14 (2): 71—82. doi:10.1002/rmv.411. PMID 15027000.
- ↑ Alam NH, Ashraf H (2003). Treatment of infectious diarrhea in children. Paediatr. Drugs. 5 (3): 151—65. doi:10.2165/00128072-200305030-00002. PMID 12608880.
- ↑ Sachdev HP (1996). Oral rehydration therapy. Journal of the Indian Medical Association. 94 (8): 298—305. PMID 8855579.
- ↑ Ramig RF (August 2007). Systemic rotavirus infection. Expert Review of Anti-infective Therapy. 5 (4): 591—612. doi:10.1586/14787210.5.4.591. PMID 17678424.
- ↑ O'Ryan M (2007). Rotarix (RIX4414): an oral human rotavirus vaccine. Expert review of vaccines. 6 (1): 11—9. doi:10.1586/14760584.6.1.11. PMID 17280473.
- ↑ Matson DO (2006). The pentavalent rotavirus vaccine, RotaTeq. Seminars in paediatric infectious diseases. 17 (4): 195—9. doi:10.1053/j.spid.2006.08.005. PMID 17055370.
- ↑ Widdowson MA, Steele D, Vojdani J, Wecker J, Parashar U (November 2009). Global rotavirus surveillance: determining the need and measuring the impact of rotavirus vaccines. The Journal of Infectious Diseases. 200 (Suppl 1): S1—8. doi:10.1086/605061. PMID 19817589.
- ↑ Tate JE, Cortese MM, Payne DC, Curns AT, Yen C, Esposito DH, Cortes JE, Lopman BA, Patel MM, Gentsch JR, Parashar UD (January 2011). Uptake, impact, and effectiveness of rotavirus vaccination in the United States: review of the first 3 years of postlicensure data. The Pediatric Infectious Disease Journal. 30 (1 Suppl): S56—60. doi:10.1097/INF.0b013e3181fefdc0. PMID 21183842.
- ↑ Waggie Z, Hawkridge A, Hussey GD (September 2010). Review of rotavirus studies in Africa: 1976–2006. The Journal of Infectious Diseases. 202 (Suppl): S23—33. doi:10.1086/653554. PMID 20684708. Архів оригіналу за 15 вересня 2019. Процитовано 25 серпня 2016.
- ↑ Soares-Weiser K, Maclehose H, Bergman H та ін. (2012). Soares-Weiser, Karla (ред.). Vaccines for preventing rotavirus diarrhoea: vaccines in use. Cochrane Database Syst Rev. 11: CD008521. doi:10.1002/14651858.CD008521.pub3. PMID 23152260.
- ↑ Ward RL, Clark HF, Offit PA (September 2010). Influence of potential protective mechanisms on the development of live rotavirus vaccines. The Journal of Infectious Diseases. 202 (Suppl): S72—9. doi:10.1086/653549. PMID 20684721. Архів оригіналу за 15 вересня 2019. Процитовано 25 серпня 2016.
- ↑ Tate JE, Patel MM, Steele AD, Gentsch JR, Payne DC, Cortese MM, Nakagomi O, Cunliffe NA, Jiang B, Neuzil KM, de Oliveira LH, Glass RI, Parashar UD (April 2010). Global impact of rotavirus vaccines. Expert Review of Vaccines. 9 (4): 395—407. doi:10.1586/erv.10.17. PMID 20370550.
- ↑ Moszynski P (2011). GAVI rolls out vaccines against child killers to more countries. BMJ (Clinical Research Ed.). 343: d6217. doi:10.1136/bmj.d6217. PMID 21957215. Архів оригіналу за 15 вересня 2019. Процитовано 25 серпня 2016.
- ↑ а б Martella V, Bányai K, Matthijnssens J, Buonavoglia C, Ciarlet M (January 2010). Zoonotic aspects of rotaviruses. Veterinary Microbiology. 140 (3–4): 246—55. doi:10.1016/j.vetmic.2009.08.028. PMID 19781872.
- ↑ Müller H, Johne R (2007). Rotaviruses: diversity and zoonotic potential—a brief review. Berl. Munch. Tierarztl. Wochenschr. 120 (3–4): 108—12. PMID 17416132.
- ↑ Cook N, Bridger J, Kendall K, Gomara MI, El-Attar L, Gray J (2004). The zoonotic potential of rotavirus. J. Infect. 48 (4): 289—302. doi:10.1016/j.jinf.2004.01.018. PMID 15066329.
Посилання[ред. | ред. код]
- WHO Rotavirus web page [Архівовано 14 жовтня 2013 у Wayback Machine.]
- CDC About Rotavirus [Архівовано 19 серпня 2016 у Wayback Machine.]
- Viralzone: Rotavirus [Архівовано 13 червня 2010 у Wayback Machine.]
- Rotavirus resource library [Архівовано 23 грудня 2017 у Wayback Machine.]
- Ramig, RF (October 2004). Pathogenesis of intestinal and systemic rotavirus infection. Journal of Virology. Т. 78, № 19. с. 10213—20. doi:10.1128/JVI.78.19.10213-10220.2004. PMC 516399. PMID 15367586. Архів оригіналу за 22 серпня 2016. Процитовано 24 серпня 2016.