DHX58
Перейти до навігації
Перейти до пошуку
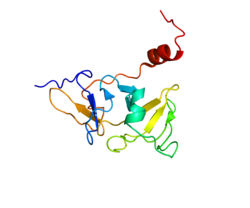
DHX58 (англ. DExH-box helicase 58) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 17-ї хромосоми.[3] Довжина поліпептидного ланцюга білка становить 678 амінокислот, а молекулярна маса — 76 613[4].
Послідовність амінокислот
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MELRSYQWEV | IMPALEGKNI | IIWLPTGAGK | TRAAAYVAKR | HLETVDGAKV | ||||
| VVLVNRVHLV | TQHGEEFRRM | LDGRWTVTTL | SGDMGPRAGF | GHLARCHDLL | ||||
| ICTAELLQMA | LTSPEEEEHV | ELTVFSLIVV | DECHHTHKDT | VYNVIMSQYL | ||||
| ELKLQRAQPL | PQVLGLTASP | GTGGASKLDG | AINHVLQLCA | NLDTWCIMSP | ||||
| QNCCPQLQEH | SQQPCKQYNL | CHRRSQDPFG | DLLKKLMDQI | HDHLEMPELS | ||||
| RKFGTQMYEQ | QVVKLSEAAA | LAGLQEQRVY | ALHLRRYNDA | LLIHDTVRAV | ||||
| DALAALQDFY | HREHVTKTQI | LCAERRLLAL | FDDRKNELAH | LATHGPENPK | ||||
| LEMLEKILQR | QFSSSNSPRG | IIFTRTRQSA | HSLLLWLQQQ | QGLQTVDIRA | ||||
| QLLIGAGNSS | QSTHMTQRDQ | QEVIQKFQDG | TLNLLVATSV | AEEGLDIPHC | ||||
| NVVVRYGLLT | NEISMVQARG | RARADQSVYA | FVATEGSREL | KRELINEALE | ||||
| TLMEQAVAAV | QKMDQAEYQA | KIRDLQQAAL | TKRAAQAAQR | ENQRQQFPVE | ||||
| HVQLLCINCM | VAVGHGSDLR | KVEGTHHVNV | NPNFSNYYNV | SRDPVVINKV | ||||
| FKDWKPGGVI | SCRNCGEVWG | LQMIYKSVKL | PVLKVRSMLL | ETPQGRIQAK | ||||
| KWSRVPFSVP | DFDFLQHCAE | NLSDLSLD |
Кодований геном білок за функціями належить до гідролаз, геліказ. Задіяний у таких біологічних процесах, як імунітет, вроджений імунітет, взаємодія хазяїн-вірус, противірусний захист. Білок має сайт для зв'язування з АТФ, нуклеотидами, іонами металів, іоном цинку, РНК. Локалізований у цитоплазмі.
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Komuro A., Horvath C.M. (2006). RNA- and virus-independent inhibition of antiviral signaling by RNA helicase LGP2. J. Virol. 80: 12332—12342. PMID 17020950 DOI:10.1128/JVI.01325-06
- Vitour D., Meurs E.F. (2007). Regulation of interferon production by RIG-I and LGP2: a lesson in self-control. Sci. STKE. 2007: PE20—PE20. PMID 17473309 DOI:10.1126/stke.3842007pe20
- Bamming D., Horvath C.M. (2009). Regulation of signal transduction by enzymatically inactive antiviral RNA helicase proteins MDA5, RIG-I, and LGP2. J. Biol. Chem. 284: 9700—9712. PMID 19211564 DOI:10.1074/jbc.M807365200
- Loo Y.M., Gale M. Jr. (2011). Immune signaling by RIG-I-like receptors. Immunity. 34: 680—692. PMID 21616437 DOI:10.1016/j.immuni.2011.05.003
- Broquet A.H., Hirata Y., McAllister C.S., Kagnoff M.F. (2011). RIG-I/MDA5/MAVS are required to signal a protective IFN response in rotavirus-infected intestinal epithelium. J. Immunol. 186: 1618—1626. PMID 21187438 DOI:10.4049/jimmunol.1002862
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:29517 (англ.) . Процитовано 12 вересня 2017.
- ↑ UniProt, Q96C10 (англ.) . Архів оригіналу за 7 вересня 2017. Процитовано 12 вересня 2017.
| Це незавершена стаття про білки. Ви можете допомогти проєкту, виправивши або дописавши її. |
| На цю статтю не посилаються інші статті Вікіпедії. Будь ласка розставте посилання відповідно до прийнятих рекомендацій. |