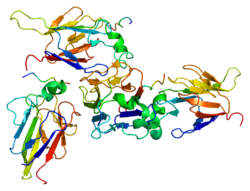
CHEK2
CHEK2 (англ. Checkpoint kinase 2) – білок, який кодується геном CHEK2, розташованим у людей на довгому плечі 22-ї хромосоми.[4] Довжина поліпептидного ланцюга білка становить 543 амінокислот, а молекулярна маса — 60 915[5].
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MSRESDVEAQ | QSHGSSACSQ | PHGSVTQSQG | SSSQSQGISS | SSTSTMPNSS | ||||
| QSSHSSSGTL | SSLETVSTQE | LYSIPEDQEP | EDQEPEEPTP | APWARLWALQ | ||||
| DGFANLECVN | DNYWFGRDKS | CEYCFDEPLL | KRTDKYRTYS | KKHFRIFREV | ||||
| GPKNSYIAYI | EDHSGNGTFV | NTELVGKGKR | RPLNNNSEIA | LSLSRNKVFV | ||||
| FFDLTVDDQS | VYPKALRDEY | IMSKTLGSGA | CGEVKLAFER | KTCKKVAIKI | ||||
| ISKRKFAIGS | AREADPALNV | ETEIEILKKL | NHPCIIKIKN | FFDAEDYYIV | ||||
| LELMEGGELF | DKVVGNKRLK | EATCKLYFYQ | MLLAVQYLHE | NGIIHRDLKP | ||||
| ENVLLSSQEE | DCLIKITDFG | HSKILGETSL | MRTLCGTPTY | LAPEVLVSVG | ||||
| TAGYNRAVDC | WSLGVILFIC | LSGYPPFSEH | RTQVSLKDQI | TSGKYNFIPE | ||||
| VWAEVSEKAL | DLVKKLLVVD | PKARFTTEEA | LRHPWLQDED | MKRKFQDLLS | ||||
| EENESTALPQ | VLAQPSTSRK | RPREGEAEGA | ETTKRPAVCA | AVL |
Цей білок за функціями належить до серин/треонінових протеїнкіназ, є гену чекпоінт-гомологом. Задіяний у таких біологічних процесах, як апоптоз, регуляція транскрипції, клітинний цикл, поділ клітини, репарація ДНК, мітоз, альтернативний сплайсинг.
Білок має сайт для зв'язування з АТФ, іоном магнію. Локалізований у ядрі.
Білок CHK2 — це протеїнкіназа, що активується при пошкодженнях ДНК та залучена до блокування клітинного циклу. CHK2 містать домен FHA, що активується у відповідь на пошкодження ДНК, завдяки швидкому фосфорилюванню. Активований протеїн інгібує фосфатазу CDC25C, завдяки чому попереджується початок мітозу. Крім того, CHK2 стабілізує пухлинний супресор p53, що впливає на блокування клітинного циклу на G1. Крім того, CHK2 взаємодіє та фосфорилює BRCA1, що в свою чергу бере участь у регуляції відновлення клітин після пошкодження ДНК.
Мутації в CHEK2 призводять до зниження рівня репарації ДНК при її пошкожденнях та зниження рівня апоптозу. Внаслідок цього, підвищується ризик розвитку злоякісних новоутворень (раку).
Мутації делеції на позиції 1100 гену CHEK2 асоційовані з підвищеним ризиком раку молочної залози, зокрема серед жіночого населення Європи.
CHEK2 взаємодіє з PLK1,[6] MDC1,[7] MSH2,[8][9] GINS2,[10] PLK3,[11] MUS81[12] та BRCA1.[13][14]
- Matsuoka S., Huang M., Elledge S.J. (1998). Linkage of ATM to cell cycle regulation by the Chk2 protein kinase. Science. 282: 1893—1897. PMID 9836640 DOI:10.1126/science.282.5395.1893
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Lee J.S., Collins K.M., Brown A.L., Lee C.H., Chung J.H. (2000). hCds1-mediated phosphorylation of BRCA1 regulates the DNA damage response. Nature. 404: 201—204. PMID 10724175 DOI:10.1038/35004614
- Lee C.H., Chung J.H. (2001). The hCds1 (Chk2)-FHA domain is essential for a chain of phosphorylation events on hCds1 that is induced by ionizing radiation. J. Biol. Chem. 276: 30537—30541. PMID 11390408 DOI:10.1074/jbc.M104414200
- Falck J., Mailand N., Syljuaasen R.G., Bartek J., Lukas J. (2001). The ATM-Chk2-Cdc25A checkpoint pathway guards against radioresistant DNA synthesis. Nature. 410: 842—847. PMID 11298456 DOI:10.1038/35071124
- Ahn J.Y., Li X., Davis H.L., Canman C.E. (2002). Phosphorylation of threonine 68 promotes oligomerization and autophosphorylation of the Chk2 protein kinase via the forkhead-associated domain. J. Biol. Chem. 277: 19389—19395. PMID 11901158 DOI:10.1074/jbc.M200822200
- ↑ Захворювання, генетично пов'язані з CHEK2 переглянути/редагувати посилання на ВікіДаних.
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:16627 (англ.) . Процитовано 26 квітня 2018.
- ↑ UniProt, O96017 (англ.) . Архів оригіналу за 10 травня 2018. Процитовано 26 квітня 2018.
- ↑ Tsvetkov, Lyuben; Xu Xingzhi, Li Jia, Stern David F (March 2003). Polo-like kinase 1 and Chk2 interact and co-localize to centrosomes and the midbody. J. Biol. Chem. United States. 278 (10): 8468—75. doi:10.1074/jbc.M211202200. ISSN 0021-9258. PMID 12493754.
{{cite journal}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) - ↑ Lou, Zhenkun; Minter-Dykhouse Katherine, Wu Xianglin, Chen Junjie (February 2003). MDC1 is coupled to activated CHK2 in mammalian DNA damage response pathways. Nature. England. 421 (6926): 957—61. doi:10.1038/nature01447. ISSN 0028-0836. PMID 12607004.
- ↑ Adamson, Aaron W; Beardsley Dillon I, Kim Wan-Ju, Gao Yajuan, Baskaran R, Brown Kevin D (March 2005). Methylator-induced, Mismatch Repair-dependent G2 Arrest Is Activated through Chk1 and Chk2. Mol. Biol. Cell. United States. 16 (3): 1513—26. doi:10.1091/mbc.E04-02-0089. ISSN 1059-1524. PMC 551512. PMID 15647386.
- ↑ Brown, Kevin D; Rathi Abhilasha, Kamath Ravindra, Beardsley Dillon I, Zhan Qimin, Mannino Jennifer L, Baskaran R (January 2003). The mismatch repair system is required for S-phase checkpoint activation. Nat. Genet. United States. 33 (1): 80—4. doi:10.1038/ng1052. ISSN 1061-4036. PMID 12447371.
- ↑ Matsuoka, Shuhei; Ballif Bryan A, Smogorzewska Agata, McDonald E Robert, Hurov Kristen E, Luo Ji, Bakalarski Corey E, Zhao Zhenming, Solimini Nicole, Lerenthal Yaniv, Shiloh Yosef, Gygi Steven P, Elledge Stephen J (May. 2007). ATM and ATR substrate analysis reveals extensive protein networks responsive to DNA damage. Science. United States. 316 (5828): 1160—6. doi:10.1126/science.1140321. PMID 17525332.
- ↑ Bahassi, El Mustapha; Conn Christopher W, Myer David L, Hennigan Robert F, McGowan Clare H, Sanchez Yolanda, Stambrook Peter J (September 2002). Mammalian Polo-like kinase 3 (Plk3) is a multifunctional protein involved in stress response pathways. Oncogene. England. 21 (43): 6633—40. doi:10.1038/sj.onc.1205850. ISSN 0950-9232. PMID 12242661.
- ↑ Chen, X B; Melchionna R, Denis C M, Gaillard P H, Blasina A, Van de Weyer I, Boddy M N, Russell P, Vialard J, McGowan C H (November 2001). Human Mus81-associated endonuclease cleaves Holliday junctions in vitro. Mol. Cell. United States. 8 (5): 1117—27. doi:10.1016/S1097-2765(01)00375-6. ISSN 1097-2765. PMID 11741546.
- ↑ Lee, J S; Collins K M, Brown A L, Lee C H, Chung J H (March 2000). hCds1-mediated phosphorylation of BRCA1 regulates the DNA damage response. Nature. ENGLAND. 404 (6774): 201—4. doi:10.1038/35004614. ISSN 0028-0836. PMID 10724175.
- ↑ Chabalier-Taste, Corinne; Racca Carine, Dozier Christine, Larminat Florence (December 2008). BRCA1 is regulated by Chk2 in response to spindle damage. Biochim. Biophys. Acta. Netherlands. 1783 (12): 2223—33. doi:10.1016/j.bbamcr.2008.08.006. ISSN 0006-3002. PMID 18804494.