Моноклональні антитіла
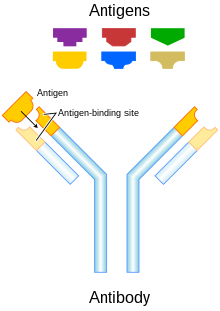
Моноклональні антитіла — це антитіла, які виробляються ідентичними імунними клітинами, які клоновані з однієї клітини-попередника (B-лімфоцита), які специфічні до одного антигену. Моноклональні антитіла можуть вироблятися проти будь-якого природного антигену (Найчастіше це білки, полісахариди, білкова оболонка вірусу, пухлинні або пошкоджені клітини, токсини), який можуть зв'язувати дані антитіла. Моноклональні антитіла можуть використовуватись як для виявлення специфічного антигену в організмі, так і для його зв'язування та його знешкодження. Найбільш широко моноклональні антитіла застосовуються в медицині для діагностики (зокрема, різних гематологічних захворювань), та для лікування різноманітних онкологічних, ревматологічних[1], деяких неврологічних захворювань (зокрема, розсіяного склерозу[2]) та пульмонологічних захворювань[3], а також у трансплантології для профілактики реакції відторгнення трансплантату. Назви усіх моноклональних антитіл, що застосовуються в медицині, мають закінчення «-маб» (скорочення, яке з англійської мови перекладається «monoclonal» (моноклональні) «antibodies» (антитіла)).
Історія відкриття[ред. | ред. код]
Дослідження, які розпочали вивчення механізму утворення антитіл, що мають високу специфічність до відповідних антигенів, розпочались ще у кінці ХІХ століття. Уперше сироватку із протитоксичними антитілами (проти токсину збудника дифтерії) застосували у 1894 році в Берліні під час епідемії дифтерії, і за успіхи в антитоксичній терапії ініціатор застосування цієї сироватки Еміль фон Берінг отримав у 1901 році Нобелівську премію з медицини. Перші спроби лікування злоякісних пухлин зроблені ще у 1895 році, коли Ерікур та Ріше робили спроби застосування екстракту остеогенної саркоми для лікування 50 хворих. Хоча результати застосування цього екстракту були досить обнадійливими, проте вони були короткочасними, та при їх застосуванні спостерігалась значна кількість побічних ефектів. На початку ХХ століття відомий німецький імунолог Пауль Ерліх висловлював думку про наявність так званої «чарівної кулі», тобто препарату, який сам би знаходив причину хвороби та знищував її. Подальше обґрунтування застосування моноклональних антитіл для лікування злоякісних пухлин знайшло в роботах Прессмана та Корнгол, опублікованих у 1953 році. У 60-х роках встановлено також структуру антитіл, у тому числі вивчено їх амінокислотну послідовність. Подальший розвиток ідея лікування моноклональними антитілами отримала в 70-х роках ХХ століття. У 1975 році Георг Келер та Сезар Мільштейн розробили технологію отримання особливих клітинних ліній, які представляли собою гібриди між нормальними клітинами селезінки миші, здатними до вироблення антитіл, та клітинами мишачої мієломи. Ці гібриди були двоядерними і зберігали здатність до мітозу. Ці клітинини назвали гібридомами. Структура вироблення такою клітиною антитіл залишалась незмінною, а антитіла, які вироблялися такою клітиною, назвали моноклональними. За розробку цієї технології Келер та Мільштайн у 1984 році отримали Нобелівську премію з медицини. У 1986 році до клінічного застосування для профілактики реакції відторгнення трансплантату при трансплантації нирки допущений перший препарат мишачих гібридизованих моноклональних антитіл — муромонаб. Проте пізніше у використанні таких антитіл у клінічній практиці виникли серйозні проблеми. Причиною цього стало те, що організм людини сприймав такі антитіла як повністю чужорідні, що спричинювало часті побічні реакції, аж до виникнення анафілактичного шоку; окрім того, такі антитіла не завжди мали достатню клінічну активність у зв'язку із утворенням в організмі людини антитіл до таких моноклональних мишачих антитіл. Для усунення цього недоліку в подальшому була розроблена технологія клонування генів, відповідальних за синтез імуноглобулінів, та розробка так званих «химерних» антитіл — гуманізованих антитіл, які є гібридами антитіл людини і миші. На першому етапі в таких антитілах константні регіони амінокислотної послідовності мали людське походження, а варіабельні регіони — мишаче походження. Прикладом такого моноклонального антитіла є ритуксимаб. Наступним етапом стала розробка таких гуманізованих антитіл, у яких лише незначні ділянки мають мишаче походження, а більша частина амінокислотної послідовності має людське походження. Прикладом такого моноклонального антитіла є алемтузумаб. Наступним етапом отримання моноклональних антитіл є синтез повністю людських антитіл, які не мають явищ гуманізації, та знижують імовірність імунних реакцій на введення такого лікарського засобу.
Виробництво моноклональних антитіл[ред. | ред. код]


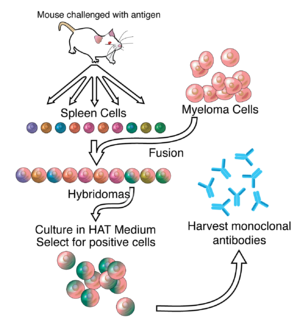
Отримання моноклональних антитіл включає у себе кілька етапів, зокрема, імунізацію тварин, одержання лімфоцитів, одержання гібридом та вирощування клону в промислових біотехнологічних масштабах.
На першому етапі лабораторним мишам проводиться імунізація шляхом ввення антигену, антитіла до якого мають виробляти клітини імунної системи миші. Після проведення циклу імунізації, який триває кілька тижнів, перевіряють, чи в мишей розвинулась імунна відповідь. Якщо імунна відповідь відбулась, то в тварин вилучають селезінку, промивають та подрібнюють її, отримані клітини селезінки змішують із суспензією спеціальних мієломних клітин, і цю суміш початково інкубують у 35 % розчині поліетиленгліколю, а пізніше переносять у середовище, у якому містяться гіпоксантин, аміноптерин та тимідин, оскільки в такому середовищі ростуть виключно клітини-гібридоми мієломи-селезінки. Після отримання гібридом їх на 10—14 день переносять із вказаного вище середовища до лунок пластикових планшетів, на якому їх далі вирощують на звичайному культуральному середовищі без додавання аміноптерину, тимідину і гіпоксантину. Після цього проводиться ідентифікація гібридних клітинних ліній, які виробляють специфічні антитіла шляхом імуноферментного аналізу. При отриманні клітин, які продукують необхідні антитіла, їх висівають із лунок на культуральне середовище, культивуючи їх у інші лунки, і шляхом клонування їх виробляють у кількості, достатній і для промислового виробництва. Іноді гібридоми культивують в організми мишей, вводячи їх у черевну порожнину тварини, і після того, як вони приживуться та розпочинають розмножуватися, їх отримують у великих кількостях із асцитичної рідини. Деякі моноклональні антитіла отримують у системі для експресії, яка створена на основі клітин яєчників китайського хом'ячка.[4]
Новітньою технологією в отриманні моноклональних антитіл, а саме чисто людських моноклональних антитіл, є метод фагового дисплею, який полягає у вбудовуванні гену, який кодує необхідний білок (у тому числі необхідні антитіла), у генотип бактеріофага, внаслідок чого він починає відтворювати цей білок на своїй оболонці, що дає можливість пізніше методом так званої білкової інженерії отримувати цей білок у необхідних кількостях.[5][6]
Застосування[ред. | ред. код]
Моноклональні антитіла застосовуються у діагностиці та лікуванні різноманітних захворювань, а також для проведення біохімічних досліджень.
Діагностика[ред. | ред. код]
Моноклональні антитіла використовують у діагностиці деяких захворювань під час дослідження методом вестерн-блот[7][8] Вони також можуть застосовуватися в імуногістохімічних дослідженнях[9], а також у дослідженнях методом імунофлюресценції.[10]
Лікування[ред. | ред. код]
Моноклональні антитіла застосовують у лікуванні як онкологічних, так і ревматологічних, пульмонологічних та неврологічних захворювань, є клінічних досвід застосування моноклональних антитіл у кардіології та при інфекційних захворюваннях.
Для лікування різноманітних онкологічних захворювань застосовуються ряд моноклональних антитіл, які специфічно зв'язуються з рецепторами відповідних пухлинних клітин. Для лікування онкологічних захворювань найрозповсюдженішими препаратами моноклональних антитіл є алемтузумаб, бевацизумаб, цетуксимаб, ритуксимаб, трастузумаб, панітумумаб, іпілімумаб, офатумумаб[11], а німотузумаб отримав статус орфанного препарату в Європейському Союзі для лікування гліоми в 2004 році.[12]
Для лікування ревматологічних захворювань, зокрема ревматоїдного артриту та ювенільного ревматоїдного артриту застосовуються інфліксімаб[13][14], адалімумаб[15][16] та тоцилізумаб.[17][18] Для лікування остеопорозу застосовується деносумаб.[19][20] Моноклональні антитіла застосовуються також для лікування інших системних захворювань, зокрема для лікування хвороби Крона та неспецифічного виразкового коліту застосовується препарат ведолізумаб.[21][22]
Для профілактики та лікування реакції відторгнення трансплантату в трансплантології застосовується базиліксимаб[23][24], раніше з цією метою також застосовувався даклізумаб.[25] Пізніше даклізумаб був схвалений для використання при розсіяному склерозі[26][27] Для лікування розсіяного склерозу застосовується також наталізумаб.[28][29]
У лікуванні бронхіальної астми застосовується препарат моноклональних антитіл омалізумаб.[30] Для застосування в кардіології розроблені моноклональні антитіла проти рецептора ліпопротеїнів низької щільності.[3] Для профілактики тромбозу стента при крізьшкірній коронарній ангіопластиці застосовується препарат моноклональних антитіл абціксимаб.[31]
У лікуванні ряду інфекційних захворювань також застосовуються препарати моноклональних антитіл. Зокрема. у лікуванні гепатиту C застосовується бавітуксимаб[32], палівізумаб використовується у лікуванні респіраторно-синцитіальної інфекції в дітей[31], є повідомлення про застосування препарату моноклональних антитіл під кодовою назвою ZMapp для лікування геморагічної гарячки Ебола[33][34][35], досліджуються препарати моноклональних антитіл севірумаб[36][37] та сувізумаб для лікування СНІДу.[38]
Біохімічні дослідження[ред. | ред. код]
Моноклональні антитіла застосовують для проведення імунопреципітації — виділення білка із складних сумішей, таких як клітинні лізати, сироватки та тканинні гомогенати, за допомогою специфічних до білка антитіл.[39]
Див. також[ред. | ред. код]
Примітки[ред. | ред. код]
- ↑ Моноклональные антитела: что это за препараты [Архівовано 28 листопада 2016 у Wayback Machine.] (рос.)
- ↑ Натализумаб (Тизабри) — новый препарат на рынке Украины для лечения рассеяного склероза [Архівовано 6 лютого 2017 у Wayback Machine.] (рос.)
- ↑ а б Инновационные лекарственные средства XXI века [Архівовано 3 жовтня 2017 у Wayback Machine.] (рос.)
- ↑ Бевацизумаб [Архівовано 30 травня 2018 у Wayback Machine.] (рос.)
- ↑ Kehoe JW, Kay BK (2005). Filamentous phage display in the new millennium. Chem. Rev. 105 (11): 4056—4072. doi:10.1021/cr000261r. (англ.)
- ↑ Smith GP, Petrenko VA (1997). Phage display. Chem. Rev. 97 (2): 391—410. doi:10.1021/cr960065d. (англ.)
- ↑ Towbin, H. et al. (1979): Electrophoretic transfer of proteins from polyacrylamide gels to nitrocellulose sheets: procedure and some applications. In: Proc. Natl. Acad. Sci. U. S. A. Bd. 76(9), S. 4350-4354. PMID 388439 PDF[недоступне посилання з червня 2019] (англ.)
- ↑ Corley RB. (2005). A Guide to Methods in the Biomedical Sciences. Springer. с. 11. ISBN 978-0-387-22844-0. Архів оригіналу за 2 травня 2016. Процитовано 3 червня 2017. (англ.)
- ↑ Ramos-Vara, JA (2005). Technical Aspects of Immunohistochemistry. Vet Pathol. 42 (4): 405—426. doi:10.1354/vp.42-4-405. PMID 16006601. Архів оригіналу за 25 травня 2009. Процитовано 3 червня 2017. (англ.)
- ↑ Fritschy, Jean-Marc; Härtig, Wolfgang (2001). Immunofluorescence. ELS. doi:10.1038/npg.els.0001174. ISBN 978-0-470-01590-2. Архів оригіналу за 2 липня 2017. Процитовано 3 червня 2017. (англ.)
- ↑ Takimoto CH, Calvo E. (Січень 2005) «Principles of Oncologic Pharmacotherapy» [Архівовано 22 липня 2017 у Wayback Machine.] in Pazdur R, Wagman LD, Camphausen KA, Hoskins WJ (Eds) Cancer Management [Архівовано 4 жовтня 2013 у Wayback Machine.] (англ.)
- ↑ Ramakrishnan, Melarkode S.; Anand Eswaraiah; Tania Crombet; Patricia Piedra; Giselle Saurez; Harish Iyer; A.S. Arvind (2009). Nimotuzumab, a promising therapeutic monoclonal for treatment of tumors of epithelial origin. mAbs. 1 (1): 41—48. doi:10.4161/mabs.1.1.7509. PMC 2715181. PMID 20046573. Архів оригіналу за 29 липня 2012. Процитовано 13 липня 2017. (англ.)
- ↑ Опыт лечения ревматоидного артрита препаратом Ремикейд (инфликсимаб) (РМЖ) [Архівовано 11 травня 2017 у Wayback Machine.] (рос.)
- ↑ Ювенильный артрит: возможности медикаментозного и немедикаментозного лечения на современном этапе [Архівовано 11 вересня 2017 у Wayback Machine.] (рос.)
- ↑ Адалимумаб в терапии раннего ревматоидного артрита [Архівовано 18 травня 2017 у Wayback Machine.] (рос.)
- ↑ Rau R (January 2002). Adalimumab (a fully human anti-tumour necrosis factor α monoclonal antibody) in the treatment of active rheumatoid arthritis: the initial results of five trials. Ann Rheum Dis. 61 (Suppl 2): ii70—3. doi:10.1136/ard.61.suppl_2.ii70. PMC 1766697. PMID 12379628. Архів оригіналу за 28 вересня 2011. Процитовано 3 червня 2017. (англ.)
- ↑ ТОЦИЛІЗУМАБ У ЛІКУВАННІ ЮВЕНІЛЬНОГО РЕВМАТОЇДНОГО АРТРИТУ. Архів оригіналу за 7 вересня 2017. Процитовано 3 червня 2017.
- ↑ ПРИМЕНЕНИЕ НОВОГО ГЕННО-ИНЖЕНЕРНОГО БИОЛОГИЧЕСКОГО ПРЕПАРАТА ТОЦИЛИЗУМАБ В ЛЕЧЕНИИ РЕВМАТОИДНОГО АРТРИТА [Архівовано 24 лютого 2017 у Wayback Machine.] (рос.)
- ↑ Деносумаб — первый генно-инженерный препарат для лечения остеопороза [Архівовано 26 березня 2020 у Wayback Machine.] (рос.)
- ↑ НОВАЯ ЦЕЛЬ ТАРГЕТНОЙ ТЕРАПИИ ОСТЕОПОРОЗА — ИНГИБИТОР RANKL ДЕНОСУМАБ [Архівовано 5 липня 2017 у Wayback Machine.] (рос.)
- ↑ Leon P McLean,Terez Shea-Donohue,Raymond K Cross (Вересень 2012). Vedolizumab for the treatment of ulcerative colitis and Crohn’s disease. Immunotherapy (англ.). 4 (9): 883—898.
- ↑ ENTYVIO- vedolizumab injection, powder, lyophilized, for solution (англ.). Архів оригіналу за 13 березня 2018. Процитовано 3 червня 2017.
- ↑ Basiliximab [Архівовано 26 серпня 2019 у Wayback Machine.] (англ.)
- ↑ Иммуносупрессанты: мнение отечественного эксперта [Архівовано 23 червня 2017 у Wayback Machine.] (рос.)
- ↑ Roche. 4 березня 1999 Roche Press Release: Zenapax (daclizumab), The First Humanized Monoclonal Antibody To Prevent Organ Rejection, Approved In The European Union [Архівовано 28 серпня 2021 у Wayback Machine.] (англ.)
- ↑ В Европе рекомендован к одобрению препарат Зинбрита (даклизумаб) для лечения рассеянного склероза [Архівовано 12 лютого 2017 у Wayback Machine.] (рос.)
- ↑ Lycke J. Monoclonal antibody therapies for the treatment of relapsing-remitting multiple sclerosis: differentiating mechanisms and clinical outcomes. Ther Adv Neurol Disord. 2015 Nov;8(6):274-93. Review. PMID 26600872 PMC 4643868 (англ.)
- ↑ Стратегии лечения рассеянного склероза: эффективность и безопасность [Архівовано 7 лютого 2017 у Wayback Machine.] (рос.)
- ↑ НОВЫЙ ВЗГЛЯД НА ЭФФЕКТИВНОСТЬ НАТАЛИЗУМАБА ПРИ РАССЕЯННОМ СКЛЕРОЗЕ (ДАННЫЕ ПРЕДВАРИТЕЛЬНЫХ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ И ИССЛЕДОВАНИЙ, ВЫПОЛНЕННЫХ ПОСЛЕ ВЫВОДА ПРЕПАРАТА НА РЫНОК) [Архівовано 6 лютого 2017 у Wayback Machine.] (рос.)
- ↑ Омализумаб [Архівовано 4 березня 2016 у Wayback Machine.] (англ.)
- ↑ а б Rang, H. P. (2003). Pharmacology. Edinburgh: Churchill Livingstone. с. 241, for the examples infliximab, basiliximab, abciximab, daclizumab, palivusamab, gemtuzumab, alemtuzumab and rituximab, and mechanism and mode. ISBN 0-443-07145-4. (англ.)
- ↑ Staff, Adis Insight. Bavituximab profile [Архівовано 19 червня 2017 у Wayback Machine.] (англ.)
- ↑ Near-final version. Reversion of advanced Ebola virus disease in nonhuman primates with ZMapp [Архівовано 31 серпня 2014 у Wayback Machine.] (англ.)
- ↑ Emory University Hospital Ebola team featured by NBC News [Архівовано 21 квітня 2017 у Wayback Machine.] (англ.)
- ↑ Лекарство против Эболы показало первые результаты. Архів оригіналу за 9 квітня 2016. Процитовано 3 червня 2017.
- ↑ Borucki, MJ; Spritzler, J; Asmuth, DM; Gnann, J; Hirsch, MS; Nokta, M; Aweeka, F; Nadler, PI та ін. (2004). A phase II, double-masked, randomized, placebo-controlled evaluation of a human monoclonal anti-Cytomegalovirus antibody (MSL-109) in combination with standard therapy versus standard therapy alone in the treatment of AIDS patients with Cytomegalovirus retinitis. Antiviral Research. 64 (2): 103—11. doi:10.1016/j.antiviral.2004.06.012. PMID 15498605. (англ.)
- ↑ ClinicalTrials.gov [Архівовано 5 березня 2016 у Wayback Machine.] (англ.)
- ↑ Proposed List number 102 of International Nonproprietary Names (PDF). WHO Drug Information. Geneva: World Health Organization. 23 (4): 344. 2009. ISSN 1010-9609. (англ.)
- ↑ Isolation of proteins and protein complexes by immunoprecipitation. [Архівовано 23 квітня 2017 у Wayback Machine.] (англ.)
Посилання[ред. | ред. код]
- Моноклональні антитіла — вічний двигун у медицині
- «Волшебные пули»: моноклональные антитела в онкологии [Архівовано 23 грудня 2016 у Wayback Machine.] (рос.)
- Моноклональные антитела — лекарства XXI века. (рос.)
- Моноклональні антитіла, їх одержання та використання в медичній практиці [Архівовано 25 грудня 2016 у Wayback Machine.]
- МОНОКЛОНАЛЬНІ АНТИТІЛА. ЩО ЦЕ ТАКЕ І ДЛЯ ЧОГО ВОНИ ПОТРІБНІ?
- Отримання моноклональних антитіл [Архівовано 23 травня 2017 у Wayback Machine.]
- Достижения фармацевтики: моноклональные антитела [Архівовано 27 грудня 2016 у Wayback Machine.] (рос.)
- Monoclonal Antibodies [Архівовано 10 червня 2017 у Wayback Machine.] (англ.)
| |||||||||||||||||||||||||
|