Ізобутилен
| Ця стаття не має шаблону-картки. Можливо, потрібен шаблон {{Речовина}}. |
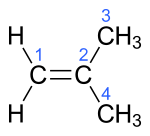

І́зобутиле́н (ізобутен, 2-метилпропен) — ненасичений вуглеводень ряду алкенів, з хімічною формулою (СH3)2C=CH2.
Ізобутилен був синтезований в 1868 році О. М. Бутлеровим шляхом дегідратації третинного бутилового спирту.
Фізичні властивості[ред. | ред. код]
Агрегатний стан: безбарвний газ;
Густина: 0,5942 г/см3
Молекулярна маса: 56,11;
Температура плавлення: -140,337 °C;
Температура кипіння: -6,896 °C;
Показник заломлення n25
D: 1,3814;
Критична температура: 144,75 °C;
Критичне тиск: 4,0003 МПа;
Критична густина: 0,235 г/см3;
Отримання[ред. | ред. код]
У промисловості ізобутилен отримують дегідруванням ізобутану на окисних каталізаторах (наприклад, Cr3O3 на Al2O3) при 500—600 °C, або дегідратацією ізобутилового спирту.
Хімічні властивості[ред. | ред. код]

Може приєднувати воду в присутності кислот (найчастіше, сульфатної) з утворенням трет-бутанолу. Реакція проходить поетапно: спочатку молекула приєднує протон, утворюючи трет-бутиловий карбокатіон. Потім приєднується молекула води, утворюючи оксонієвий катіон. Далі протон відривається, залишаючи трет-бутанол.
При нагріванні в кислому середовищі з фторидом бору приєднує спирти з утворенням трет-бутилових етерів.
Може алкілюватися ізобутаном у приcутності сульфатної кислоти з утворенням 2,2,4-триметилпентану. В цій реакції теж спочатку приєднується протон. Далі приєднується ще одна молекула ізобутилену, утворюючи димерний карбокатіон. Потім від молекули ізобутану відривається негативний іон гідрогену, перетворюючи її в карбокатіон, та приєднується до димерного карбокатіону, утворюючи 2,2,4-триметилпентан. Карбокатіон, що утворився, взаємодіє з новою молекулою ізобутилену, і процес повторюється.
Може окиснюватися під дією сильних окисників (перманганату калію, дихромату калію, нітратної кислоти) до кетонів та альдегідів, які, в свою чергу, можуть окиснитися до карбонових кислот.
Застосування[ред. | ред. код]
Здатність ізобутилену полімеризуватися і сополімеризуватися використовують у виробництві поліізобутилену і бутилкаучуку.
Ізобутилен застосовують також для алкілування ароматичних сполук та ізобутану з метою отримання ізооктану.
Джерела[ред. | ред. код]
- Ластухін Ю. О., Воронов С. А. Органічна хімія : підручник. — Вид. 3-тє, стереотипне. — Львів : Центр Європи, 2006. — ISBN 966-7022-19-6.
- Кузнецов Д. Г. Органическая химия: Учебное пособие. — СПб.: Издательство «Лань», 2016. — 556 с. ISBN 978-5-8114-1913-5
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

