Поширеність хімічних елементів
Поширеність хімічних елементів — міра кількості хімічних елементів відносно всіх інших елементів у даному середовищі. Поширеність вимірюється одним із трьох способів: масовою часткою (у комерційному контексті її також називають ваговою часткою), молярною часткою (часткою атомів за чисельним підрахунком) або об'ємною часткою. Об'ємна частка є загальноприйнятою мірою вмісту в змішаних газах, таких як планетарні атмосфери, і для ідеальних газів вона співпадає з молекулярною молярною часткою. Більшість значень вмісту в цій статті дано як масові частки.
Наприклад, вміст кисню в чистій воді можна виміряти двома способами: молярна частка становить 33 %, оскільки в молекулі H2O лише один атом з трьох є киснем, натомість масова частка становить 89 %, тому що з загальної молекулярної маси, рівної приблизно 18, на кисень припадає близько 16 одиниць. Як інший приклад, можна розглянути розповсюдженість водню та гелію як у Всесвіті в цілому, так і в атмосферах Сонця або газових планет: масова частка становить 74 % для водню та 23–25 % для гелію, в той час як атомна молярна частка водню становить 92 %, а гелію 8 %. У зовнішній атмосфері Юпітера, де водень двоатомний, а гелій — ні, молекулярна мольну частку (частку від загальної кількості молекул газу) і рівна їй об'ємна частка водню становить приблизно 86 %, а гелію 13 %[Note 1].
За розповсюдженостю у Всесвіті переважають водень та гелій, які утворилися під час Великого вибуху. Решта елементів, що становлять лише близько 2 % Всесвіту, були в основному створені надновими та деякими червоними гігантами. Літій, берилій і бор, незважаючи на їх низький атомний номер, є рідкісними, тому що, хоча вони й утворюються в результаті ядерного синтезу, вони руйнуються іншими реакціями в зорях[1][2]. Елементи від вуглецю до заліза відносно поширені у Всесвіті через легкість їх утворення в нуклеосинтезі у наднових. Елементи з вищим атомним номером, ніж залізо (елемент 26), стають все рідшими у Всесвіті, оскільки вони потребують все більшої енергії під час свого утворення. Крім того, елементи з парними атомними номерами, як правило, зустрічаються частіше, ніж їхні сусіди в періодичній таблиці, бо їхнє утворення є енергетично вигіднішим.
Для багатьох елементів їхня поширеність на Сонці та у зовнішніх планетах Сонячної системи подібна до поширеності у Всесвіті. Через сонячне нагрівання елементи Землі та внутрішніх кам'яних планет Сонячної системи були збіднені леткими елементами — воднем, гелієм, неоном, азотом та вуглецем (який випаровується у вигляді метану). У корі, мантії та ядрі Землі є ознаки розділення елементів за густиною. Більш легкі силікати алюмінію знаходяться в корі, з силікати магнію — в мантії, а металеві залізо та нікель складають ядро. Поширеність елементів у специфічних середовищах, таких як атмосфера, океани чи людське тіло, є насамперед продуктами хімічних реакцій у відповідних середовищах.
Всесвіт[ред. | ред. код]
| З | Елемент | Масова частка (ppm) |
|---|---|---|
| 1 | водень | 739 000 |
| 2 | гелій | 240 000 |
| 8 | кисень | 10 400 |
| 6 | вуглець | 4 600 |
| 10 | неон | 1 340 |
| 26 | залізо | 1 090 |
| 7 | азот | 960 |
| 14 | кремній | 650 |
| 12 | магній | 580 |
| 16 | сірка | 440 |
| Всього | 999,060 |
Елементи, тобто звичайна (баріонна) матерія, що складається з протонів, нейтронів і електронів, є лише невеликою частиною вмісту Всесвіту. Космологічні спостережні дані показують, що з маси Всесвіту (включно з масою, яку вносить енергія, E = mc 2 ⇔ m = E / c 2) лише 4,6 % припадає на видиму баріонну матерію, яка складає зорі, планети та живі істоти. Вважається, що решта складається з темної енергії (68 %) і темної матерії (27 %). Існування цих форм матерії та енергії випливає лише з теоретичних моделей і не має прямих спостережних підтверджень, і їх природа недостатньо зрозуміла.
Більшість баріонної матерії міститься в міжгалактичному газі, зорях і міжзоряних хмарах у формі атомів або іонів, хоча подекуди її можна знайти в вироджених формах в екстремальних астрофізичних умовах, таких як білі карлики і нейтронні зорі.
Водень є найпоширенішим елементом у Всесвіті, а гелій знаходиться на другому місці. Після цього порядок за поширеністю не відповідає атомному номеру: наприклад, на третьому місці стоїть кисень з атомний номером 8.
Поширеність різних ізотопів найлегших елементів добре передбачена стандартною космологічною моделлю. Вони здебільшого виникли в ході первинного нуклеосинтезу протягом кількох хвилин після Великого вибуху в процесі. За оцінками, водень і гелій становлять приблизно 74 % і 24 % усієї баріонної матерії у Всесвіті відповідно.
Важчі елементи, хоч і складають лише невелику частину Всесвіту, можуть значно впливати на астрономічні явища. В диску галактики Чумацький Шлях масова частка важчих за гелій елементів складає лише близько 2 %. Ці важчі елементи генеруються зоряними процесами[4][5][6]. В астрономії всі елементи, важчі за гелій, прийнято називати «металами», незалежно від того, чи є вони металами з фізичної чи хімічної точки зору. Таким чином, металічність галактики чи іншого об'єкта є ознакою минулої зоряної активності в ній.
Загалом, елементи до заліза утворюються великими зорями, які стають надновими, або меншими зорями на останніх стадіях їхньої еволюції. Один з ізотопів заліза, залізо-56, є особливо поширеним, оскільки він є найстабільнішим нуклідом (має найвищу енергію ядерного зв'язку на нуклон), і його можна легко утворити з альфа-частинок (як продуктом розпаду радіоактивного нікелю-56, що в кінцевому підсумку складається з 14 ядер гелію). Елементи, важчі за залізо, утворюються в ендотермічних процесах у великих зорях, і їхня кількість у Всесвіті (і на Землі) зазвичай зменшується зі збільшенням атомного номера.
У таблиці наведено десять найпоширеніших елементів у нашій Галактиці (за спектроскопічними оцінками), виміряні в мільйонних частках за масою[3]. Сусідні галактики, які еволюціонували схожими шляхами, мають схожу поширеність елементів, важчих за водень і гелій. Найвіддаленіші і тому найстаріші галактики мають поширеність елементів, ближчу до первісної.
Як показано в періодичній таблиці нижче, поширеність елементів відповідає їх походженню. Найпоширеніші водень і гелій є продуктами Великого вибуху. Наступні три елементи в періодичній таблиці (літій, берилій і бор) є рідкісними, незважаючи на їх низький атомний номер. Вони мали небагато часу для формування під час Великого вибуху і утворилися лише в невеликих кількостях. Вони продовжують утворюватися в результаті ядерного синтезу в старих зорях або в результаті розпаду важчих елементів у міжзоряному пилу, викликаного космічними променями. У наднових зорях вони утворюються в результаті ядерного синтезу, але потім руйнуються іншими реакціями[1].
Важчі елементи, починаючи з вуглецю, утворювалися у вмираючих або наднових зорях шляхом накопичення альфа-частинок (ядер гелію), що призводить, в першу чергу, до утворення елементів з парними атомними номерами (вони також більш стабільні). Менша поширеність у Всесвіті непарних елементів була емпірично помічена у 1914 році та носить назву правила Оддо-Гаркінса.
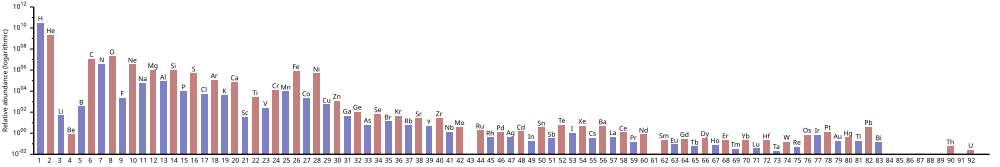
Наступний графік (зверніть увагу на логарифмічний масштаб) показує поширеність елементів у Сонячній системі.
| Нуклід | А | Масова частка в мільйонних частках | Частка атома в частках на мільйон |
|---|---|---|---|
| Водень-1 | 1 | 705 700 | 909 964 |
| Гелій-4 | 4 | 275 200 | 88,714 |
| Кисень-16 | 16 | 9,592 | 477 |
| Вуглець-12 | 12 | 3,032 | 326 |
| Азот-14 | 14 | 1,105 | 102 |
| Неон-20 | 20 | 1,548 | 100 |
| Інші нукліди: | 3616 | 172 | |
| Кремній-28 | 28 | 653 | 30 |
| Магній-24 | 24 | 513 | 28 |
| Залізо-56 | 56 | 1,169 | 27 |
| Сірка-32 | 32 | 396 | 16 |
| Гелій-3 | 3 | 35 | 15 |
| Водень-2 | 2 | 23 | 15 |
| Неон-22 | 22 | 208 | 12 |
| Магній-26 | 26 | 79 | 4 |
| Вуглець-13 | 13 | 37 | 4 |
| Магній-25 | 25 | 69 | 4 |
| Алюміній-27 | 27 | 58 | 3 |
| Аргон-36 | 36 | 77 | 3 |
| Кальцій-40 | 40 | 60 | 2 |
| Натрій-23 | 23 | 33 | 2 |
| Залізо-54 | 54 | 72 | 2 |
| Кремній-29 | 29 | 34 | 2 |
| Нікель-58 | 58 | 49 | 1 |
| Кремній-30 | 30 | 23 | 1 |
| Залізо-57 | 57 | 28 | 1 |
Зв'язок з енергією зв'язку ядра[ред. | ред. код]
Спостерігається певна кореляція між розповсюдженістю елементів у Всесвіті та кривою ядерної енергії зв'язку. Грубо кажучи, відносна стабільність різних атомних нуклідів сильно вплинула на розповсюдженість елементів, що утворилися під час Великого вибуху та під час розвитку Всесвіту після цього[8]. Стаття про нуклеосинтез пояснює, як певні процеси ядерного синтезу в зорях (наприклад, спалювання вуглецю тощо) створюють елементи, важчі за водень і гелій.
Правило Оддо-Гаркінса для більшої поширеності парних елементів теж корелює з їхньою більшою енергією зв'язку, яка пояснюється принципом Паулі[9] і, зокрема, описується формулою Вайцзекера[10].
Земля[ред. | ред. код]
Земля утворилася з тієї ж хмари матерії, що й Сонце, але планети набули різного складу під час формування та еволюції Сонячної системи. У свою чергу, природна історія Землі призвела до того, що окремі частини планети набули різної поширеності елементів.
Маса Землі становить приблизно 5,97 × 1024 кг. У вона складається здебільшого з заліза (32,1 %), кисню (30,1 %), кремнію (15,1 %), магнію (13,9 %), сірки (2,9 %), нікелю (1,8 %), кальцію (1,5 %) та алюмінію (1,4 %); решта 1,2 % складаються з малих кількостей інших елементів[11].
Склад Землі схожий на склад Сонячної системи, а головна відмінність полягає в тому, що в Землі значно менше летких елементів, — водню, гелію, неону та азоту, а також вуглецю, який був втрачений у вигляді летких вуглеводнів. Елементний склад Землі типовий для кам'яних внутрішніх планет, які утворилися в теплій частині протопланетного диску, де температура була достатньою для сублімації летючих сполук. Земля містить велику кількість кисню (другий за масовою часткою і перший за атомною молярною часткою), головним чином завдяки тому, що цей елемент утримується в силікатних мінералах, які мають дуже високу температуру плавлення.
| Атомний номер | Назва | Позначення | Масова частка (ppm) | Атомна частка (ppb)[12] |
|---|---|---|---|---|
| 8 | кисень | O | 297,000 | 482,000,000 |
| 12 | магній | Mg | 154,000 | 164,000,000 |
| 14 | кремній | Si | 161,000 | 150,000,000 |
| 26 | залізо | Fe | 319,000 | 148,000,000 |
| 13 | алюміній | Al | 15,900 | 15,300,000 |
| 20 | кальцій | Ca | 17,100 | 11,100,000 |
| 28 | нікель | Ni | 18,220 | 8,010,000 |
| 1 | водень | H | 260 | 6,700,000 |
| 16 | сірка | S | 6,350 | 5,150,000 |
| 24 | хром | Cr | 4,700 | 2,300,000 |
| 11 | натрій | Na | 1,800 | 2,000,000 |
| 6 | вуглець | C | 730 | 1,600,000 |
| 15 | фосфор | P | 1,210 | 1,020,000 |
| 25 | марганець | Mn | 1,700 | 800,000 |
| 22 | титан | Ti | 810 | 440,000 |
| 27 | кобальт | Co | 880 | 390,000 |
| 19 | калій | K | 160 | 110,000 |
| 17 | хлор | Cl | 76 | 56,000 |
| 23 | ванадій | V | 105 | 53,600 |
| 7 | азот | N | 25 | 46,000 |
| 29 | мідь | Cu | 60 | 25,000 |
| 30 | цинк | Zn | 40 | 16,000 |
| 9 | фтор | F | 10 | 14,000 |
| 21 | скандій | Sc | 11 | 6,300 |
| 3 | літій | Li | 1.10 | 4,100 |
| 38 | стронцій | Sr | 13 | 3,900 |
| 32 | германій | Ge | 7.00 | 2,500 |
| 40 | цирконій | Zr | 7.10 | 2,000 |
| 31 | галій | Ga | 3.00 | 1,000 |
| 34 | селен | Se | 2.70 | 890 |
| 56 | барій | Ba | 4.50 | 850 |
| 39 | ітрій | Y | 2.90 | 850 |
| 33 | арсен | As | 1.70 | 590 |
| 5 | бор | B | 0.20 | 480 |
| 42 | молібден | Mo | 1.70 | 460 |
| 44 | рутеній | Ru | 1.30 | 330 |
| 78 | платина | Pt | 1.90 | 250 |
| 46 | паладій | Pd | 1.00 | 240 |
| 58 | церій | Ce | 1.13 | 210 |
| 60 | неодім | Nd | 0.84 | 150 |
| 4 | берилій | Be | 0.05 | 140 |
| 41 | ніобій | Nb | 0.44 | 120 |
| 76 | осмій | Os | 0.90 | 120 |
| 77 | іридій | Ir | 0.90 | 120 |
| 37 | рубідій | Rb | 0.40 | 120 |
| 35 | бром | Br | 0.30 | 97 |
| 57 | лантан | La | 0.44 | 82 |
| 66 | диспрозій | Dy | 0.46 | 74 |
| 64 | гадоліній | Gd | 0.37 | 61 |
| 52 | телур | Te | 0.30 | 61 |
| 45 | родій | Rh | 0.24 | 61 |
| 50 | олово | Sn | 0.25 | 55 |
| 62 | самарій | Sm | 0.27 | 47 |
| 68 | ербій | Er | 0.30 | 47 |
| 70 | ітербій | Yb | 0.30 | 45 |
| 59 | празеодим | Pr | 0.17 | 31 |
| 82 | свинець | Pb | 0.23 | 29 |
| 72 | гафній | Hf | 0.19 | 28 |
| 74 | вольфрам | W | 0.17 | 24 |
| 79 | золото | Au | 0.16 | 21 |
| 48 | кадмій | Cd | 0.08 | 18 |
| 63 | європій | Eu | 0.10 | 17 |
| 67 | гольмій | Ho | 0.10 | 16 |
| 47 | серебро | Ag | 0.05 | 12 |
| 65 | тербій | Tb | 0.07 | 11 |
| 51 | стибій | Sb | 0.05 | 11 |
| 75 | реній | Re | 0.08 | 10 |
| 53 | йод | I | 0.05 | 10 |
| 69 | тулій | Tm | 0.05 | 7 |
| 55 | цезій | Cs | 0.04 | 7 |
| 71 | лютецій | Lu | 0.05 | 7 |
| 90 | торій | Th | 0.06 | 6 |
| 73 | тантал | Ta | 0.03 | 4 |
| 80 | ртуть | Hg | 0.02 | 3 |
| 92 | уран | U | 0.02 | 2 |
| 49 | індій | In | 0.01 | 2 |
| 81 | талій | Tl | 0.01 | 2 |
| 83 | бісмут | Bi | 0.01 | 1 |
Кора[ред. | ред. код]
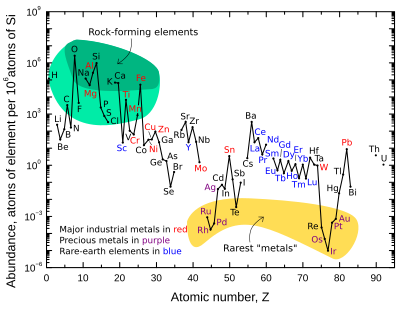
Масова частка дев'яти найпоширеніших елементів у земній корі становить приблизно: кисень 46 %, кремній 28 %, алюміній 8,3 %, залізо 5,6 %, кальцій 4,2 %, натрій 2,5 %, магній 2,4 %, калій 2,0 % і титан 0,61 %. Інші елементи складають менше 0,15 %.
Графік праворуч ілюструє відносну атомну концентрацію хімічних елементів у верхній частині континентальної земної кори — частині, відносно доступній для вимірювань і оцінок.
Деякі елементи, показані на графіку, включають до таких груп, які частково перекриваються:
- породоутворюючі елементи (головні елементи в зеленому полі, а другорядні в світло-зеленому полі);
- рідкоземельні елементи (лантаноїди (La–Lu), Sc і Y; позначені синім кольором);
- основні промислові метали (світове виробництво >~3×107 кг/рік; позначені червоним);
- дорогоцінні метали (позначені фіолетовим);
- дев'ять найрідкісніших «металів» — шість елементів платинової групи плюс Au, Re і Te (металоїд) — у жовтому полі. Вони рідко зустрічаються в земній корі через те, що розчиняються в залізі, і тому концентруються в ядрі Землі. Телуром земні силікати найсильніше збіднені у порівнянні з поширеністю в космосі, оскільки на додаток до того, що він концентрувався у вигляді щільних халькогенідів у ядрі, він був значною мірою втрачений з частинок в протопланетній туманності у вигляді летючого телуриду водню[13].
Є два розриви, на місці нестабільних елементів технецію (атомний номер 43) і прометію (атомний номер 61). Їхні найстабільніші ізотопи мають відносно короткий період напіврозпаду (~4 мільйони років і ~18 років відповідно), тому будь-які первинні атоми цих матеріалів вже давно розпалися, і зараз вони надзвичайно рідкісні. Вони виробляються в природі лише шляхом спонтанного поділу дуже важких радіоактивних елементів (наприклад, урану, торію або слідових кількостей плутонію, які містяться в уранових рудах), або шляхом взаємодії деяких інших елементів із космічними променями. І технецій, і прометій були ідентифіковані спектроскопічно в атмосферах зір, де вони утворюються в результаті процесів нуклеосинтезу.
На графіку розповсюдженості також є розриви на місці шести благородних газів, які рідкісні в земній корі, оскільки вони хімічно не зв'язані в горних породах і утворюються там лише ланцюжками розпаду радіоактивних елементів.
Вісім дуже рідкісних високорадіоактивних природних елементів (полоній, астат, францій, радій, актиній, протактиній, нептуній і плутоній) не включені, оскільки будь-який з цих елементів, які були присутні під час формування Землі, розпався багато років тому, і їхня кількість сьогодні незначна і утворюється лише в результаті радіоактивного розпаду урану та торію.
Кисень і кремній є найпоширенішими елементами земної кори. На Землі та на кам'янистих планетах загалом кремній і кисень набагато більш поширені, ніж у космосі. Причина в тому, що вони добре поєднуються один з одним, утворюючи нелеткі силікатні мінерали[13]. Інші поширені в космосі елементи, такі як водень, вуглець і азот, утворюють леткі сполуки, такі як аміак і метан, які легко википають у космос від тепла формування планет і/або сонячного світла.
Мантія[ред. | ред. код]
Масова частка семи найпоширеніших елементів у мантії Землі становить приблизно: кисень 44,3 %, магній 22,3 %, кремній 21,3 %, залізо 6,32 %, кальцій 2,48 %, алюміній 2,29 %, нікель 0,19 %[14].
Ядро[ред. | ред. код]
Вважається, що через сегрегацію маси ядро Землі в основному складається із заліза (88,8 %), з меншою кількістю нікелю (5,8 %), сірки (4,5 %) і менше 1 % мікроелементів[11].
Океан[ред. | ред. код]
Найпоширенішими елементами в океані за масовою часткою є кисень (85,84 %), водень (10,82 %), хлор (1,94 %), натрій (1,08 %), магній (0,13 %), сірка (0,09 %), кальцій (0,04 %), калій (0,04 %), бром (0,007 %), вуглець (0,003 %) і бор (0,0004 %).
Атмосфера[ред. | ред. код]
Порядок елементів за об'ємною часткою (що приблизно дорівнює молекулярній молірній частці) в атмосфері: азот (78,1 %), кисень (20,9 %)[15], аргон (0,96 %), потім (у невизначеному порядку) вуглець і водень оскільки водяна пара та вуглекислий газ, які представляють більшість цих двох елементів у повітрі, є змінними компонентами. Сірка, фосфор і всі інші елементи присутні в значно менших частках.
Тіло людини[ред. | ред. код]
| елемент | Частка (за масою) |
|---|---|
| Кисень | 65 |
| Вуглець | 18 |
| Водень | 10 |
| Азот | 3 |
| Кальцій | 1.5 |
| Фосфор | 1.2 |
| Калій | 0,2 |
| Сірка | 0,2 |
| Хлор | 0,2 |
| Натрій | 0,1 |
| Магній | 0,05 |
| Залізо | < 0,05 |
| Кобальт | < 0,05 |
| Мідь | < 0,05 |
| Цинк | < 0,05 |
| Йод | < 0,05 |
| Селен | < 0,01 |
За масою клітини людини на 65-90 % складаються з води (H2O), а значна частина решти складається з вуглецевмісних органічних молекул. Тому кисень становить більшу частину маси людського тіла, а наступним йде вуглець. Майже 99 % маси людського тіла складається з шести елементів: водню (H), вуглецю (C), азоту (N), кисню (O), кальцію (Ca) і фосфору (P). Наступні 0,75 % складаються з наступних п'яти елементів: калію (K), сірки (S), хлору (Cl), натрію (Na) і магнію (Mg). Лише про 17 елементів відомо, що вони необхідні для життя людини, ще один додатковий елемент (фтор) вважається корисним для міцності зубної емалі. Ще кілька мікроелементів можуть відігравати певну роль у здоров'ї ссавців. Бор і кремній необхідні для рослин, але мають невизначену роль у тварин. Алюміній і кремній, хоча і дуже поширені в земній корі, мають дуже низький вміст в організмі людини[16].
Нижче наведено таблицю Менделєєва з елементами харчування[17].
Список літератури[ред. | ред. код]
Примітки[ред. | ред. код]
- ↑ а б Vangioni-Flam, Elisabeth; Cassé, Michel (2012). Spite, Monique (ред.). Galaxy Evolution: Connecting the Distant Universe with the Local Fossil Record. Springer Science & Business Media. с. 77—86. ISBN 978-9401142137.
- ↑ Trimble, Virginia (1996). The Origin and Evolution of the Chemical Elements. У Malkan, Matthew A.; Zuckerman, Ben (ред.). The origin and evolution of the universe. Sudbury, Mass.: Jones and Bartlett Publishers. с. 101. ISBN 0-7637-0030-4.
- ↑ а б Croswell, Ken (February 1996). Alchemy of the Heavens. Anchor. ISBN 0-385-47214-5. Архів оригіналу за 13 травня 2011.
- ↑ Suess, Hans; Urey, Harold (1956). Abundances of the Elements. Reviews of Modern Physics. 28 (1): 53. Bibcode:1956RvMP...28...53S. doi:10.1103/RevModPhys.28.53.
- ↑ Cameron, A. G. W. (1973). Abundances of the elements in the solar system. Space Science Reviews. 15 (1): 121. Bibcode:1973SSRv...15..121C. doi:10.1007/BF00172440.
- ↑ Anders, E.; Ebihara, M. (1982). Solar-system abundances of the elements. Geochimica et Cosmochimica Acta. 46 (11): 2363. Bibcode:1982GeCoA..46.2363A. doi:10.1016/0016-7037(82)90208-3.
- ↑ Arnett, David (1996). Supernovae and Nucleosynthesis (вид. First). Princeton, New Jersey: Princeton University Press. с. 11. ISBN 0-691-01147-8. OCLC 33162440.
- ↑ Bell, Jerry A.; GenChem Editorial/Writing Team (2005). Chapter 3: Origin of Atoms. Chemistry: a project of the American Chemical Society. New York [u.a.]: Freeman. с. 191–193. ISBN 978-0-7167-3126-9.
Correlations between abundance and nuclear binding energy [Subsection title]
- ↑ Bell, Jerry A.; GenChem Editorial/Writing Team (2005). Chapter 3: Origin of Atoms. Chemistry: a project of the American Chemical Society. New York [u.a.]: Freeman. с. 192. ISBN 978-0-7167-3126-9.
The higher abundance of elements with even atomic numbers [Subsection title]
- ↑ Bailey, David. Semi-empirical Nuclear Mass Formula. PHY357: Strings & Binding Energy. University of Toronto. Архів оригіналу за 24 липня 2011. Процитовано 31 березня 2011.
- ↑ а б Morgan, J. W.; Anders, E. (1980). Chemical composition of Earth, Venus, and Mercury. Proceedings of the National Academy of Sciences. 77 (12): 6973—6977. Bibcode:1980PNAS...77.6973M. doi:10.1073/pnas.77.12.6973. PMC 350422. PMID 16592930.
- ↑ William F McDonough The composition of the Earth. quake.mit.edu, archived by the Internet Archive Wayback Machine.
- ↑ а б в Anderson, Don L.; ‘Chemical Composition of the Mantle’ in Theory of the Earth, pp. 147—175 ISBN 0865421234
- ↑ Wang, Haiyang S.; Lineweaver, Charles H.; Ireland, Trevor R. (1 січня 2018). The elemental abundances (with uncertainties) of the most Earth-like planet. Icarus (англ.). 299: 460—474. doi:10.1016/j.icarus.2017.08.024. ISSN 0019-1035.
{{cite journal}}:|hdl-access=вимагає|hdl=(довідка) - ↑ Zimmer, Carl (3 жовтня 2013). Earth's Oxygen: A Mystery Easy to Take for Granted. The New York Times. Архів оригіналу за 3 October 2013. Процитовано 3 жовтня 2013.
- ↑ Table data from Chang, Raymond (2007). Chemistry (вид. Ninth). McGraw-Hill. с. 52. ISBN 978-0-07-110595-8.
- ↑ Nielsen, Forrest H. (1998). Ultratrace minerals.. У Maurice E. Shils (ред.). Modern nutrition in health and disease. Baltimore: Lippincott Williams & Wilkins. с. 283—303. ISBN 978-0683307696.
Виноски[ред. | ред. код]
- ↑ Нижче зовнішньої атмосфери Юпітера об’ємні частки значно відрізняються від мольних часток через високі температури (іонізація та диспропорціонування) і високу густину, де закон ідеального газу незастосовний.
Позначення[ред. | ред. код]
- Rare Earth Elements—Critical Resources for High Technology | USGS Fact Sheet 087-02. geopubs.wr.usgs.gov.
- Imagine the Universe! Dictionary. 3 грудня 2003. Архів оригіналу за 3 December 2003.
Посилання[ред. | ред. код]
- Список елементів у порядку поширеності в земній корі (вірно лише для двадцяти найпоширеніших елементів)
- Поширеність елементів і нуклеосинтез
- WebElements.com Списки вмісту елементів у Всесвіті, Сонці, метеоритах, Землі, океані, річковій воді тощо.
| Періодична система хімічних елементів | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||||||||||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||||||||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||||||||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||||||||||||||||||||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||