Морська вода

Морська вода (англ. marine water, ocean water; нім. Meerwasser n, Seewasser n) — вода морів і океанів. Переважна кількість морської води знаходиться в Світовому океані (1,37 млрд км³). Має гірко-солоний смак, через значний вміст солей (хлорид натрію). Середня солоність морської води 35 ‰. Така вода замерзає при −2 °C, чим більша солоність, тим нижча така температура замерзання[1].
Фізичні характеристики[ред. | ред. код]
Густина морської води коливається в межах від 1020 до 1030 кг·м−3. Показник кислотності pH варіюється в межах від 7,5 до 8,4. Швидкість звуку в морській воді — близько 1500 м/с.
Число км³ морської води в даному інтервалі солоності[2]

Густина[ред. | ред. код]
Середні величини густини поверхневих вод морів[3]
| No. | Море | густина кг/м³ |
|---|---|---|
| 1 | Середземне море | 1020,90 |
| 2 | Чорне море | 1013,5 |
| 3 | Мармурове море | 1017,0 |
| 4 | Північне море | 1026,4 |
| 5 | Балтійське море | 1006,6 |
Прозорість[ред. | ред. код]
Відносна прозорість вод морів[3]
| No. | Море | Відносна прозорість, м |
|---|---|---|
| 1 | Баренцеве море південно-західна частина | до 45 м |
| 2 | Чорне море | близько 30 |
| 3 | Егейське море | до 50 |
| 4 | Середземне море біля африканського узбережжя | 40-45 |
| 5 | Балтійське море біля острова Борнхольм | 11-13 |
| 6 | Каспійське море південна частина | 11-13 |
| 7 | Північне море біля Англійського каналу | 6,5-11 |
| 8 | Адріатичне море | 30-40 |
Хімічний склад[ред. | ред. код]

| Компонент | Концентрація (моль/кг) |
| H2O | 53,6 |
| Na+ | 0,546 |
| Cl- | 0,469 |
| Mg2+ | 0,0528 |
| SO42- | 0,0283 |
| Ca2+ | 0,0103 |
| K+ | 0,0102 |
| CT | 0,00206 |
| Br- | 0,000844 |
| BT | 0,000416 |
| Sr2+ | 0,000091 |
| F- | 0,000068 |
Середня солоність морської води — 35 г/л (35 ‰). Це 0,6 молей·літр−1 (у припущенні, що вся сіль являє собою NaCl, що насправді не так). Хоча солоність води в океанах майже повсюдно близька до 35 ‰, однак вода в морях має нерівномірно розподілену солоність, в залежності від ступеня їх ізольованості від океану, припливу слабкомінералізованих поверхневих вод суші, кліматичних умов. Відзначається трохи менший вміст солей у полярних акваторіях і підвищений до 39-42 ‰ в тропічних. Найменш солоною є вода Фінскої затоки і північної частини Ботнічної затоки (близько 5 ‰), що входять в акваторію Балтійського моря. Найсолонішою є вода Червоного моря (42 ‰). Соляні озера, такі як Мертве море, можуть мати значно більший рівень вмісту солей (до 300 ‰).
Середній вміст солей у морській воді близько 35 ‰, температура замерзання 1,91 °С, густина 1020 кг/м³. Хімічний склад морської води постійний — 99,99 % за масою сольового складу припадає на Na+ — 10,7 ‰, K+ — 0,39 ‰, Ca2+ — 0,42 ‰, Mg2+ — 1,30 ‰, SO42− — 2,70 ‰, Cl− — 19,35 ‰, Br− — 0,06 ‰, CO32− — 0,07 ‰. При цьому 85 % солей у морській воді складає NaCl, у значних кількостях присутні: MgCl2, MgSO4, CaSO4, NaBr, а також розчинені гази та органічні речовини (1-5 мг/л).
Внаслідок високої концентрації хімічних компонентів і величезного їх сумарного вмісту у водах Світового океану, морська вода використовується для отримання багатьох хімічних сполук. Наприклад, у країнах жаркого клімату (КНР, Японія, Індія, Австралія, ін.) упарюванням за рахунок сонячного тепла отримують 30-40 % світового видобутку кухонної солі. В перспективі, з появою нових технологій, з морської води можливе вилучення ряду цінних корисних копалин. Морська вода містить в розчиненому вигляді практично всі елементи періодичної таблиці хімічних елементів.
Розподіл солей за глибиною загалом постійний, в нижніх горизонтах зростає вміст розчиненої вуглекислоти, внаслідок чого в глибинних ділянках осад карбонату кальцію розчиняється. Різка зміна складу води за глибиною спостерігається в Чорному морі за рахунок двох потоків через Босфор (верхнього, більш прісного, з Чорного моря і нижнього, солонішого, з Мармурового в Чорне море) і дії сульфатредукуючих бактерій, що приводить до накопичення сірководню (до 14 мг/л).
Розподіл солоності поверхневих водних мас Світового океану має певні закономірності. На екваторі солоність поверхневих вод знижена, вона підвищується до субтропічних широт і знов зменшується до полюсів, сягаючи значень у 35 ‰ в помірних широтах. Такий широтний розподіл порушуються морськими течіями: холодні течії виносять з приполярних зон до помірних широт воду з пониженою солоністю, навпаки, теплі течії несуть до помірних широт більш солону воду. На екваторі на місце вод, що були знесені морськими течіями, повільно підіймаються з глибини холодні води. В свою чергу вони, прогрівшись на поверхні, відходять до полярних широт, де, охолонувши, опускаються на дно — термохалінна циркуляція.[1]
Геохімічне пояснення[ред. | ред. код]
Хімічні елементи (за масою)
|
|---|
Наукове обґрунтування появи солоної води в морі було покладено роботами сера Едмонда Галлея в 1715 році. Він висунув гіпотезу, що сіль й інші мінерали вимивалися із ґрунту й доставлялися в море річками. Досягши океану, солі залишалися й поступово концентрувалися. Хеллі помітив, що більшість озер, що не мають водного зв'язку з океанами, мають солону воду. Теорія Хеллі почасти вірна. Доповнюючи її, варто згадати, що натрій вимивався із дна океанів на ранніх етапах їхнього формування. Присутність іншого елемента солі — хлору, пояснюється його вивільненням (у вигляді соляної кислоти) з надр Землі при виверженнях вулканів. Натрій і хлор поступово стали основою сольового складу морської води (85 % від всіх солей).
Інша гіпотеза середини ХХ століття геохіміка Олександра Виноградова. Згідно якої суміш пари і води з газами при дегазації мантії Землі, була вже в початковий період формування океану порівняно схожою з сучасною. Тому океанічна вода завжди мала певну солоність і не була прісною. У подальшому на склад вод океану впливало багато атмосферних і континентальних процесів. Близько 200 млн років тому, наприкінці палеозою (за даними досліджень складу проб, відібраних з давніх висохлих морів) хімічний склад води океану, в основному, сформувався і став близьким до сучасного.
Морська вода нормальна[ред. | ред. код]
Нормальна морська вода (рос. морская вода нормальная; англ. normal sea water, нім. normales Meerwasser n, normales Seewasser n) — спеціально приготовлена морська вода з солоністю 34-35 ‰ (г/дм³). Використовують для калібрування приладів, наукових досліджень. Готують штучно у лабораторії на основі проб, відібраних у Біскайській затоці Атлантичного океану. Нормальна морська вода містить солі NaCl, MgCl2, Na2SO4, CaCl2, KCl, NaHCO3, KBr, H3BO4, SCl2, NaF, які взято у певній пропорції. Необхідно вводити поправку на вміст кристалізаційної води в застосовуваних реактивах, якщо вона в них є.
Розподіл температур[ред. | ред. код]
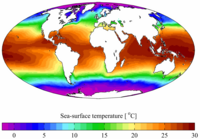
Температура разом із солоністю визначає щільність води. Чим нижча температура, тим більша щільність. Вода — одна з речовин, яка має найбільшу теплоємність 4200 кДж/кг. Тільки 10 метровий шар океанських вод містить тепла більше, ніж вся земна атмосфера. Саме велика теплоємність океану робить його головним акумулятором і регулятором температури географічної оболонки планети. На відміну від розподілу температур за глибиною, на поверхні океанів температури розподілені зонально. У екваторіальному поясі температура води становить 27-28°С протягом всього року. У тропіках західні частини океанів тепліші (20-25°С), тому що сюди підходять пасатні течії з екваторіальними водами. Східні частини океанів холодніші через холодні течії (15-20°С). Східні області океанів у помірному поясі обігріваються Північноатлантичною та Північнотихоокеанською течіями, західні області охолоджуються Лабрадорською та Курильською течіями. У помірних широтах південної півкулі температура змінюється зонально від 10°С близько 40° південної широти до 0° С на 60° південної широти і далі знижується до межі морських льодів. У полярних поясах температура води опускається до 2-3°С, не перетворюючись на лід через її солоність.
Розподіл солоності[ред. | ред. код]

Середня солоність океану змінюється на його поверхні незначно. У екваторіальній зоні солоність може знижуватися через випадання рясних дощів та велику хмарність до 32 ‰. У тропіках солоність води підвищена до 38 ‰. Це пов'язано з відсутністю хмарності та дією постійних вітрів, що викликають посилене випаровування води. Солоність помірних широт відповідає середній солоності океану. До полярних широт вона зменшується до 32 ‰, що обумовлено надходженням прісних вод з материків і таненням льодовиків.
Солоність внутрішніх морів особливо залежить від припливу річкових і океанічних вод. Наприклад, віддалені від Атлантичного океану Азовське і Чорне моря, у яких приплив річкових вод, мають значно нижчу солоність, ніж в океані (відповідно, 11 ‰ та 18 ‰). В той же час, у відділеному від Індійського океану Баб-ель-Мандебською протокою Червоному морі, в якого відсутній приплив річкових вод, солоність вища, ніж в океані (42 ‰). В окраїнних морях солоність води значно ближча до солоності води океану (якщо немає великого річкового припливу).
Зміна солоності з глибиною відрізняється великою розмаїтістю. Суттєві зміни відбуваються лише у верхньому шарі, до глибини 1500 м. Нижче цього горизонту коливання солоності надзвичайно малі. У деяких районах океанів солоність стає одноманітною зі значно вищих горизонтів. У полярних областях солоність сильно змінюється тільки лише глибини 200 м, а глибше вона практично незмінна.
Придатність для пиття[ред. | ред. код]
Морська вода непридатна для пиття через високий вміст солей, для виведення яких з організму потрібно води більше, ніж її випита кількість. Однак після опріснення морську воду можна пити.
Курйози[ред. | ред. код]
У Гонконзі морська вода широко використовується в зливальних системах туалетів. Більш ніж 90 % з них використають для змивання саме морську воду задля економії прісної води. Початок цій практиці було покладено в 1960-их й 1970-тих роках, коли скорочення запасів прісної води стало проблемою для жителів цієї британської колонії.
Див. також[ред. | ред. код]
Джерела[ред. | ред. код]
- ↑ а б (рос.) Подобедов Н. С. Общая физическая география и геоморфология. — М.: Недра, 1974. С. 312.
- ↑ «Океан сам по себе и для нас» — переклад з англійської Голосова. В. В. Редакція і післямова Сузюмова. А.А — Москва «Прогресс». Тираж 75000 1982 рік. Переклад книги «Oceanography» Ch.Drake, JImbrie, J Knauss, K.Turekian — Holt Rinehart Winston
- ↑ а б Зубков. О.Є Все о море /Під редакцією Дремлюга. В. В. — Київ:. Радянська школа., 1986. — 256ст. іл. Тираж 100000 екз.(рос.)
Література[ред. | ред. код]
- Мала гірнича енциклопедія : у 3 т. / за ред. В. С. Білецького. — Д. : Донбас, 2007. — Т. 2 : Л — Р. — 670 с. — ISBN 57740-0828-2.
- Хільчевський В. К. Гідрохімія океанів і морів — К.: ВПЦ «Київський університет», 2003.- 114 с.
- Хільчевський В. К., Дубняк С. С. Основи океанології. — К.: ВПЦ «Київський університет», 2008. — 255 с. [Архівовано 4 грудня 2017 у Wayback Machine.]
Посилання[ред. | ред. код]
| Вікісховище має мультимедійні дані за темою: Морська вода |
- (англ.) Water Temperature Map [Архівовано 6 травня 2015 у Wayback Machine.] — температура води Світового океану в реальному часі.
- (англ.) Tables and software for thermophysical properties of seawater. [Архівовано 30 липня 2010 у Wayback Machine.]
|