Свинець
Свине́ць, плю́мбум[1] (хімічний знак — , лат. plumbum), в нефаховій літературі плю́мбій[2] — хімічний елемент з атомним номером 82, що належить до 14-ї групи, 6-го періоду періодичної системи елементів.
Проста речовина свине́ць[3] (нефахове застаріле о́ливо[2][4][Заввага 1]) — важкий, м'який, ковкий, сірий метал.
Густина свинцю 11,34 г/см³; tплав 327,6 °С, tкип 1745 °С. Свинець хімічно малоактивний. На повітрі досить швидко покривається тонкою плівкою оксиду. Кристалічна ґратка кубічна гранецентрована.
Зазвичай свинець трапляється у вигляді руди галеніту, іноді у вигляді самородків; є кінцевим, стабільним продуктом розпаду урану. Свинець — найм'якший і найслабший з використовуваних металів із низькою точкою плавлення, поганий провідник електрики, стійкий до кислотної корозії, може бути отруйним, накопичується в організмі під час уживання води зі свинцевих труб, використання фарби на основі свинцю і бензину з його добавками. Є ефективним захистом проти радіації, використовується в гальванічних елементах, склі, кераміці і сплавах типу олова й у припої.
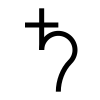
Українське слово «свинець» є похідним від прасл. *svinecь, від якого також походять назви цього металу у деяких слов'янських мовах: біл. свінец, рос. свинец, дав.-рус. і церк.-слов. свинҍць, словен. svinc (більшість слов'янських назв свинцю споріднені з українським словом «олово»). Праслов'янське *svinecь споріднене з лит. švinas («свинець») та латис. svins (так само), подальші зв'язки неясні[6]. Припускалася спорідненість з грец. κυανος («синя речовина»), яке порівнюють, у свою чергу, з хеттськ. kuuanna(n) («мідний купорос», «коштовний камінь»). Інша версія пов'язує *svinecь з ос. (ӕ)фсӕн («леміш», «залізо») та пушту ospina («залізо»)[7].
Слово «оливо» походить від прасл. *olovo («олово», «свинець»), похідними від якого є назви цього металу у більшості слов'янських мов: біл. волава, пол. ołów, хорв., чеськ. і словац. olovo, болг. і мак. олово, серб. олово/olovo.
Наукова назва свинцю — «плюмбум» — походить від лат. plumbum, яке давніми римлянами уживалося щодо двох металів: свинцю (plumbum nigrum — «чорний плюмбум») та олова (plumbum candidum — «білий плюмбум»).
Свинець відомий ще з бронзової доби. Поряд із стибієм та арсеном його використовували для виготовлення бронзи. Пізніше його замінили оловом. Ще стародавні вавилоняни виготовляли вази зі свинцю. Римляни використовували його для виготовлення посуду, водопровідних труб. Свинець був відомий також народам Месопотамії і Єгипті 6-7 тис. років до н. е.
Алхіміки вважали свинець сировиною для трансмутації (перетворення його на золото).

Металічний свинець отримують окиснювальним випаленням сульфідних руд з подальшим відновленням PbO до чорнового металу і рафінуванням останнього. У чорновому свинці міститься до 98 % Pb, в рафінованому 99,8-99,9 %. Свинець з 99,99 % Pb отримують електролізом.
Із галеніту свинець отримують у дві стадії:
- Прожарювання:
- 2 PbS + 3 O2 → 2 PbO + 2 SO2 ΔH0
r=−836 кДж/моль
- 2 PbS + 3 O2 → 2 PbO + 2 SO2 ΔH0
- Відновлення коксом:
- PbO + C → Pb + CO ΔH0
r=+107 кДж/моль - PbO + CO → Pb + CO2 ΔH0
r=−66 кДж/моль
- PbO + C → Pb + CO ΔH0
Утворюються свинцеві злитки з вмістом 95–97 % Pb, які потім очищують (рафінують) за допомогою переплавлення з флюсом, чи електролізом.
Більшість свинцевої руди містить дуже низький відсоток свинцю, який повинен бути більш концентрованим під час обробки.[8]
| Країна | Видобуток (тисячі тон) |
|---|---|
| 2300 | |
| 633 | |
| 385 | |
| 300 | |
| 240 | |
| 130 | |
| 90 | |
| 82 | |
| 76 | |
| 54 | |
| 45 | |
| 40 | |
| 40 | |
| 38 | |
| 33 | |
| Інші країни | 226 |
Кларк в земній корі 1,6×10−3 % за масою. Існує близько 180 мінералів свинцю, серед яких найбільш важливе значення мають галеніт PbS (86,6 % Pb), що зазвичай містить домішку Sb, Bi і Ag, джемсоніт Pb4FeSb6S14 (40,16 %), буланжерит Pb5Sb4S11 (55,42 %), бурноніт CuPbSbS3 (42,6 %); в зоні окиснення — церусит PbCO3 (77,6 %) і англезит PbSO4 (68,3 %). Свинець і цинк спільно з іншими металами (мідь, золото, срібло) утворюють поліметалічні руди. Відомі свинцево-цинкові руди з різним співвідношенням цих металів; рідше зустрічаються самостійні родовища цинкових або свинцевих руд.
Природній свинець складається з чотирьох різних ізотопів. З них 3 стабільні, а ще 1 має надзвичайно довгий період розпаду.
| Масове число | Частка у природному свинці | Період напіврозпаду |
|---|---|---|
| 204 | 1,4 % | >= 1,4×1017 років |
| 206 | 24,1 % | ∞ |
| 207 | 22,1 % | ∞ |
| 208 | 52,4 % | ∞ |
Загалом відомо 60 ізотопів свинцю з масовими числами від 178 до 220, 17 з яких — метастабільні. З нестабільних ізотопів, що не зустрічаються в природі, найбільші періоди напіврозпаду мають 205Pb (17,3 млн років) і 202Pb (52500 років)[10].
Використовується у виробництві акумуляторів.
Свинець відіграє важливу роль як компонент припійних сплавів. Із самого початку масового виробництва електроніки, олов'яно-свинцеві припої стали досить поширеними в електротехнічній та приладобудівній галузях завдяки своїй низькій вартості, зручності використання та гарним фізичним характеристикам.[11][12][13] Крім того, до 1980-х років вони були популярним матеріалом для формування з'єднань сантехнічної трубопровідної арматури в країнах Заходу. Разом зі зростанням уваги суспільства до питань екології, використання в припоях свинцю починає поступово обмежуватися. Зокрема, Євросоюз директивою «щодо обмеження вмісту шкідливих речовин» (RoHS) передбачає з 1 липня 2006 р. загальний перехід виробництв побутової електроніки на використання безсвинцевих припоїв.[14]
Сполуки свинцю токсичні, ГДК 0,01 мг/дм³.
Накопичення свинцю в організмі людини може викликати як свинцеві енцефалопатії, виродження периферичних нервів, венозний стаз, псевдомосклероз, серцеву гіпертонію, цироз печінки тощо.
- Платиніт
- Свинцево-цинкова промисловість
- Свинцево-цинкові руди
- Свинець аномальний
- Свинець звичайний
- Свинець первісний
- Свинець первозданний
- Свинець радіогенний
- Свинець рудний
- Свинець самородний
- Свинець (мінерал)
- Сплави свинцю
- Глосарій термінів з хімії // Й. Опейда, О. Швайка. Ін-т фізико-органічної хімії та вуглехімії ім. Л. М. Литвиненка НАН України, Донецький національний університет. — Донецьк: Вебер, 2008. — 758 с. — ISBN 978-966-335-206-0.
- Гірничий енциклопедичний словник : у 3 т / за ред. В. С. Білецького. — Д. : Східний видавничий дім, 2001—2004.
- Ф. А. Деркач. Хімія. — Л., 1968.
- Свинець // Універсальний словник-енциклопедія. — 4-те вид. — К. : Тека, 2006.
- ↑ На думку лексикографа Святослава Караванського, слово «оливо» у словнику неправильно витлумачене як «олово»[5]
- ↑ Національний стандарт України ДСТУ 2439:2018 «Хімічні елементи та прості речовини. Терміни та визначення основних понять, назви й символи». — [Чинний від 01.10.2019.] — К. : ДП «УкрНДНЦ», 2019. — С. 2.
- ↑ а б свине́ц [Архівовано 5 листопада 2021 у Wayback Machine.] // Ганіткевич М., Кінаш Б. Російсько-український словник з інженерних технологій: Понад 40 000 термінів / Технічний комітет стандартизації науково-технічної термінології Міністерства економ. розвитку і торгівлі та Міністерства освіти і науки, молоді та спорту України. — 2-е вид. — Львів: Вид-во Львівської політехніки, 2013. — 1021 с. — (Термінографічна серія СловоСвіт; № 9). — ISBN 978-617-607-385-7.
- ↑ Свинець // Словник української мови : в 11 т. — Київ : Наукова думка, 1970—1980.
- ↑ Оливо // Словник української мови : в 11 т. — Київ : Наукова думка, 1970—1980.
- ↑ Караванський, Святослав (1991). Пошук українського слова або боротьба за національне «я». Київ: Літературна Україна. с. 102.
- ↑ Этимологический словарь русского языка. — М.: Прогресс М. Р. Фасмер 1964—1973.
- ↑ Етимологічний словник української мови : в 7 т. / редкол.: О. С. Мельничук (гол. ред.) та ін. — К. : Наукова думка, 2006. — Т. 5 : Р — Т / укл.: Р. В. Болдирєв та ін. — 704 с. — ISBN 966-00-0785-X.
- ↑ Greenwood and Earnshaw, p. 369
- ↑ U.S. Geological Survey (2016). Lead (PDF) (Звіт). Архів оригіналу (PDF) за 13 грудня 2016. Процитовано 20 лютого 2016.
- ↑ Isotopes of the Element Lead [Архівовано 27 листопада 2020 у Wayback Machine.](англ.)
- ↑ Говард Г. Манко (1968). Пайка та припої. Матеріали, конструкції, технологія та методи розрахунку (російська) . Москва: Машиностроение. с. 42—43.
- ↑ ГОСТ 21930-76. Припої олов'яно-свинцеві в чушках. Технічні умови (російська) . Москва: Видавництво стандартів. 1989. Архів оригіналу за 5 листопада 2013. Процитовано 14 серпня 2013.
- ↑ Петрунін І.Є. (2003). Справочник по пайке [Довідник з пайки] (російська) . Москва: Машиностроение. с. 84. ISBN 5-217-03167-0.
- ↑ Медведєв А.М. (2007). Сборка и монтаж электронных устройств [Збірка та монтаж електронних пристроїв]. Мир электроники (російською) . Москва: Техносфера. с. 107. ISBN 978-5-94836-131-4.

