Формальдегід
| Формальдегід | |
|---|---|
 Формальдегід
|
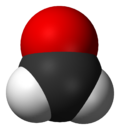 3D-модель молекули формальдегіду
|
 |
 |
| Назва за IUPAC | Метаналь |
| Систематична назва | Метаналь |
| Інші назви | Мурашиний альдегід, метилальдегід, метиленгліколь, метиленоксид |
| Ідентифікатори | |
| Номер CAS | 50-00-0 |
| PubChem | 712 |
| Номер EINECS | 200-001-8 |
| Номер EC | 200-001-8 |
| DrugBank | DB03843 |
| KEGG | D00017 |
| Назва MeSH | Formaldehyde |
| ChEBI | CHEBI:16842 |
| RTECS | LP8925000 |
| Код ATC | QP53AX19 |
| SMILES | C=O |
| InChI | 1S/CH2O/c1-2/h1H2 |
| Номер Бельштейна | 1209228 |
| Номер Гмеліна | 445 |
| 3DMet | B00018 |
| Властивості | |
| Молекулярна формула | СН2O |
| Молярна маса | 30,03 г/моль |
| Молекулярна маса | 30 а. о. м. |
| Зовнішній вигляд | Безбарвний газ |
| Запах | Різкий, характерний |
| Густина | 0,8153 г/см³ (-20 °C) |
| Тпл | −92 °C |
| Ткип | -19,2 °C |
| Розчинність (вода) | 400 г/дм³ |
| Кислотність (pKa) | 13,3 |
| Основність (pKb) | 0,7 |
| Дипольний момент | 2,33 |
| Структура | |
| Кристалічна структура | Плоска тригональна |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 |
-115,9 кДж/моль |
| Фармакологія | |
| Код ATC | QP53AX19 |
| DrugBank | DB03843 |
| Небезпеки | |
| ЛД50 | 100 мг/кг |
| NFPA 704 | |
| Температура спалаху | 64 °C |
| Температура самозаймання | 430 °C |
| Вибухові границі | 7%—73% |
| Пов'язані речовини | |
| Пов'язані речовини | Метанол, Мурашина кислота |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Формальдегід (метаналь, мурашиний альдегід) (від лат. formica — мурашка) — хімічна речовина з формулою H2CO, найпростіший із альдегідів, перший член гомологічного ряду аліфатичних альдегідів. Чистий мономерний формальдегід при звичайних умовах є безбарвним газом із характерним різким запахом. Досить добре розчинний у протонних розчинниках (вода, спирти). Сполука здатна утворюватися в природних умовах, зокрема при фотохімічному окисненні метану або метанолу, при атмосферному тиску і за відсутності каталізаторів[1].
Мономерний формальдегід має високу реакційну здатність. Його молекули легко реагують навіть одна з одною з утворенням великої кількості лінійних і циклічних полімерів (олігомерів).
Формальдегід широко застосовується у промисловості, зокрема для виробництва полімерних матеріалів, багатоатомних спиртів, ізопрену та інших продуктів. У медицині використовується як дезінфікуючий, консервуючий та дубильний засіб для анатомічних препаратів, а також для виробництва (уротропіну).
Формальдегід — це подразнюючий газ, що викликає дегенеративні процеси в паренхіматозних органах, сенсибілізує шкіру. При роботі з ним для індивідуального захисту слід застосовувати фільтрувальний промисловий протигаз марки А та герметичні захисні окуляри.
Роль у виникненні життя[ред. | ред. код]
Питання про місце формальдегіду у розвитку рослинного світу давно привертає увагу вчених. Легко помітити, що поряд з метаном, метанолом, синильною і мурашиною кислотами формальдегід належить до найпростіших органічних сполук. Різними дослідниками доведена можливість утворення формальдегіду в умовах, близьких до природних. Так, зареєстроване утворення формальдегіду при фотохімічному окисненні метану або метанолу, при атмосферному тиску і за відсутності каталізаторів[1]. Термодинамічно можливе отримання формальдегіду гідрогенізацією оксиду і діоксиду вуглецю. Добре відомо, що гідрогенізація легко відбувається за наявності металів, поширених в земній корі — хрому, міді та інших.
Величезним стрибком від первинної матерії до сполук, що утворюються рослинним шляхом, є, зокрема, реакції утворення багатоатомних альдегідоспиртів і цукрів. Ці реакції також можуть відбуватися під впливом ультрафіолетового випромінювання або при помірному нагріванні.
На думку багатьох фахівців, перехід діоксид вуглецю → формальдегід → цукри може реалізуватися у природних умовах як на Землі, так і в космосі[2]. Формальдегід легко вступає у взаємодію з іншими елементарними сполуками — аміаком, воднем, синильною кислотою, оксидом вуглецю. Всі ці речовини вже давно виявлені в космічному просторі засобами астрофізики, причому існують далекоглядні гіпотези про можливі маршрути утворення на їх основі біологічно активних речовин[3].
Фізичні властивості[ред. | ред. код]
Незважаючи на просту будову і хімічний склад молекул формальдегіду модифікації цієї сполуки, що зустрічаються на практиці, відрізняються великим різноманіттям. Це пов'язано насамперед з високою реакційною здатністю мономерного формальдегіду, молекули якого легко реагують одна з одною з утворенням великої кількості лінійних і циклічних полімерів (олігомерів). Всі ці модифікації мають одну і ту ж брутто-формулу (CH2O)n і відрізняються тільки значенням n. Наприклад, при розчиненні формальдегіду у воді у невеликих кількостях утворюються триоксан і тетраоксан, при спонтанній полімеризації газоподібного або рідкого полімерного формальдегіду утворюється твердий, але механічно неміцний поліоксиметилен, при охолодженні водних розчинів формальдегіду виділяється параформ[ru] у вигляді безбарвного або білуватого осаду.
Чистий мономерний формальдегід при звичайних умовах є безбарвним газом із характерним різким запахом. Саме наявності невеликих кількостей мономеру зобов'язані своїм запахом розчини формальдегіду, наприклад формалін, і навіть численні полімерні модифікації, зокрема, параформ[ru].
При контакті з холодною поверхнею або в присутності слідів вологи газоподібний формальдегід утворює твердий білий полімер, однак при низьких парціальних тисках мономерного формальдегіду суміші останнього з іншими речовинами, зокрема з водою і спиртами, в паровій фазі цілком стабільні (гомогенні) в широкому діапазоні тисків і температур.
Формальдегід досить добре розчинний у протонних розчинниках (вода, спирти). Це пов'язано з протіканням в них реакції полімеризації і сольватації.
При високій температурі суміші газоподібного формальдегіду з повітрям або киснем здатні самозайматися. Температура самозаймання в сумішах з повітрям становить 430 °С[4]. У певних умовах горіння переходить у детонацію, причому обидва явища виникають після деякого періоду.
За відсутності кисню формальдегід стійкий при температурі до 350-400 °С. При більш високих температурах відбувається інтенсивний крекінг[1][5]. Розпад формальдегіду різко прискорюється під впливом фотохімічного ефекту. Так, ультрафіолетове випромінювання викликає розпад вже при 100-300 °С[1]:
При швидкому і глибокому охолодженні чистий газоподібний формальдегід перетворюється в рідину. При атмосферному тиску точка кипіння складає -19,2 °С.
Рідкий формальдегід ще менш стійкий, ніж газоподібний, і досить швидко полімеризується, хоча при -(40-60) °С може зберігатися прозорим кілька діб. При найменшому нагріванні або при попаданні вологи, відбувається дуже швидка полімеризація. Рідкий формальдегід добре змішується з більшістю розчинників, наприклад з толуеном, діетиловим ефіром, хлороформом, етилацетатом і етаналем, причому з останнім утворюються суміші, близькі до ідеальних. При -118 °С рідкий формальдегід твердне. Властивості твердого мономерного формальдегіду вивчені мало, проте добре відомо, що цей продукт оборотно може бути знову перетворений на рідину а, отже, принципово відрізняється від полімеру.
Одержання[ред. | ред. код]
Окисна конверсія метанолу[ред. | ред. код]
Окисна конверсія метанолу в присутності розпеченої міді (сітка, спіралі, трубки) належить до найстаріших хімічних процесів. Як сировину довго застосовували метанол лісохімічного походження. У 20-х роках XX століття багатьма дослідниками було показано, що срібло та його сплави є ефективнішими каталізаторами ніж мідь. Надалі срібні каталізатори повністю витіснили мідні. Окисна конверсія метанолу на сріблі проводиться при співвідношенні метанол:повітря вище верхньої межі вибухової концентрації, тобто при великому надлишку метанолу відносно кисню. Утворення формальдегіду відбувається у результаті проходження паралельних реакцій простої і окисної дегідрогенізації метанолу:
У випадку використання як каталізатора срібла на носії метанол, що містить 20-25 % води, випаровують в струмені повітря[4]. Пароповітряну суміш перегрівають до 110 °С і подають у верхню частину реактора. При пуску системи шар каталізатора в реакторі розігрівається до 250-300 °С за допомогою спеціальних електропідігрівачів, а після «запалювання» шару температура каталізатора підтримується на заданому рівні за рахунок тепла реакції. Пройшовши з високою швидкістю через шар каталізатора, реакційна суміш охолоджується, а газоподібні продукти реакції надходять в абсорбер, де з них добувають формальдегід і непрореагований метанол.
Технологічна схема установок, де як каталізатор застосовується металічне срібло, практично ідентична[6].
Одержання на оксидних каталізаторах[ред. | ред. код]
Як каталізатор в процесі найчастіше використовують суміш оксидів заліза (III) і молібдену (VI) з атомним співвідношенням молібдену до заліза від 1,7 до 2,5. Готують каталізатор співосадженням підходящої солі заліза(III), наприклад хлориду або нітрату[ru], з молібдатом амонію[ru]. При нагріванні і прогартовуванні вихідна суміш перетворюється на твердий розчин оксиду молібдену(VI) у молібдаті заліза[en]. Атоми молібдену знаходяться всередині оксигенних тетраедрів і октаедрів.
Окиснення метанолу на оксидних каталізаторах відбувається за окисно-відновним механізмом:
Деякі вчені вважають, що в окисно-відновному процесі беруть участь також іони заліза[7][8].
Окиснення природного газу і нижчих алканів[ред. | ред. код]
З точки зору доступності і дешевизни сировини, а також простоти технології, отримання формальдегіду прямим окисненням природного газу, що складається, в основному, з метану, киснем повітря заслуговує уваги, оскільки синтез через метанол здійснюється через більшу кількістю етапів. Однак на практиці одержання формальдегіду окисненням метану супроводжується цілою низкою труднощів, найважливіші з яких пов'язані з недостатньою стійкістю формальдегіду в умовах реакції. Відомо, що некаталізоване (неініційоване) окиснення метану з помітною швидкістю відбувається при температурі вище 600 °С (під вакуумом вище 540 °С[9]). Водночас термічний розклад формальдегіду спостерігається вже при 400 °С[1]. Крім того, утворений формальдегід у присутності кисню легко піддається подальшому окисненню. Через ці причини на практиці окиснення метану, навіть у присутності ініціаторів проводять при малих значеннях конверсії, причому і в цих умовах селективність утворення формальдегіду невисока.
Окиснення вуглеводнів С2—С4 у порівнянні з окисненням метану має багато спільного хоча і характеризується деякими специфічними особливостями. Як і у випадку метану, процес проводять в області вище верхньої межі вибухових концентрацій вуглеводнів. При окисненні вуглеводнів С3—С5 в рідкій фазі одержуються переважно карбонові кислоти, а формальдегід практично не утворюється.
Хімічні властивості[ред. | ред. код]

Функції і активність формальдегіду в хімічних перетвореннях випливають із будови його молекули. Якщо поглянути на її структуру то можна відзначити такі особливості:
- наявність вуглець—оксигенового σ-π-зв'язку. Молекула формальдегіду є ніби окремо існуючою карбонільною групою, вільні валентності у С-атома якої заради стабільності витрачені на зв'язок з двома атомами водню. Хімічні властивості формальдегіду в основному визначаються специфікою цієї групи;
- висока поляризованість, навіть в ізольованому стані, пов'язана з відсутністю замісників, що сприяють делокалізації зарядів;
- простота будови і компактність молекули. Багато перетворень, характерних для складних органічних сполук, для формальдегіду нетипові. Однак для нього практично не існує просторових перешкод.
Перетворення у водних і спиртових розчинах[ред. | ред. код]
Відомо, що в протонних полярних розчинниках (вода, спирти) формальдегід знаходиться в хімічно зв'язаному стані, причому в результаті взаємодії з розчинником утворюється велика родина асоціатів, що знаходяться у рівновазі один з одним.
Розчиняючись у воді, мономерний формальдегід гідратується з утворенням метиленгліколю.
Швидкість реакції вельми велика, а її продукт — метиленгліколь нестійкий.
Першим актом взаємодії формальдегіду зі спиртами є утворення аналогічного до метиленгліколю моносольвату — геміформалю відповідного спирту.
Геміформаль може реагувати далі в двох напрямках, приєднуючи або ще одну молекулу формальдегіду, або спирту.
Реакція Канніццаро[ред. | ред. код]
До числа найцікавіших інтраперетворень формальдегіду належить реакція диспропорціонування з утворенням метанолу та мурашиної кислоти
або
Уперше диспропорціонування альдегідів у присутності їдких лугів вивчав Канніццаро в 1853 році. Пізніше було виявлено, що дана реакція відбувається також під впливом кислот, солей і оксидів, а також взагалі без каталізаторів. Є спостереження, що реакція прискорюється також під дією іонізуючого або світлового випромінювання[1].
З практичної точки зору велике значення має так звана перехресна реакція Канніццаро, тобто взаємодія формальдегіду з молекулою іншого альдегіду (або кетону). Останній у цьому випадку ніби гідрується (відновлюється) до відповідного спирту, а формальдегід перетворюється на мурашину кислоту. На практиці (при отриманні багатоатомних спиртів) перехресна реакція проводиться в лужному середовищі, так що її продуктами є спирт і форміат[ru] лужного металу, наприклад:
Одержання уротропіну[ред. | ред. код]
Формальдегід енергійно реагує з аміаком і деякими його похідними з утворенням гексаметилентетраміну (уротропіну):
Реакція відбувається цілком нормально уже при кімнатній температурі, причому реагенти можуть застосовуватися як у вигляді розчинів, так і в пароподібному стані, в лужному або кислому середовищі. На цій реакції оснований прийом ліквідації наслідків розгерметизації апаратури формалінових виробництв (розлив, загазованість і т. д.) обробкою аміаком або аміачною водою.
Реакція Манніха[ред. | ред. код]
Реакція Манніха — це тримолекулярна взаємодія формальдегіду одночасно з основним і кислим реагентами[10]. Як основний зазвичай застосовують диметиламін[ru], рідше — аміак або метиламін, а як кислий — сполуки, що містять активні протони: спирти, кетони, ціановодень, алкени і т. д.[1][11]
Реакція Бутлерова[ред. | ред. код]
За певних умов молекули формальдегіду здатні взаємодіяти одна з одною з утворенням системи зв'язків -C-C-, тобто з нарощуванням вуглецевого ланцюга. Як правило, це призводить до утворення багатоатомних спиртів, кетонів та альдегідів. Хоча в молекулі формальдегіду відсутній α-вуглецевий атом і звична для багатьох інших альдегідів інтрамолекулярна конденсація в даному випадку неможлива, механізм утворення перерахованих продуктів подібний до альдольної конденсації. Розглянута реакція може відбуватися як каталітичним, так і чисто термічним шляхом.
Вперше утворення цукроподібних продуктів спостерігав Бутлеров, додаючи до киплячого водного розчину формальдегіду барієвий або кальцієвий луг. Після випаровування води у вакуумі і екстрагування залишку спиртом, він отримав сиропоподібну рідину, яку назвали метилінітом (за аналогією з маннітом}})[12].
Ця реакція є досить повільною. Проте вона продовжується аж до утворення 1,1-диметилол-1,3-гідрокси-2-пропанону.
Каталітичною дією в реакції Бутлерова володіють і гідроксиди деяких нелужних металів. Так, при нагріванні розчину формальдегіду з оксидом свинцю можна отримати формозу (суміш синтетичних цукрів) з виходом 70 %[1]. Аналогічний ефект здійснює додавання дрібно меленого олова, свинцю і цинку.
Одержання циклічних формалей[ред. | ред. код]
При взаємодії формальдегіду з гліколями і багатоатомними спиртами утворюються циклічні формалі. Ці речовини, як правило, є добрими розчинниками. Однак найбільший інтерес циклічні формалі представляють як кополімерні добавки до поліформальдегіду, у зв'язку з чим ці речовини виробляють у промислових масштабах[13].
Діоксолан[ru] (глікольформаль) утворюються при дії формальдегіду на етиленгліколь при нагріванні в кислому середовищі:
Вихідний формальдегід можна застосовувати як у вигляді водного розчину, так і у вигляді параформу[ru]. Як каталізатори рекомендується застосовувати кислоти Льюїса (наприклад, ZnCl2, FeCl3).
Окиснення[ред. | ред. код]
У газоподібному стані при підвищеній температурі формальдегід легко окиснюється чистим киснем або повітрям.
У водному розчині при температурі до 100 °С швидкість взаємодії формальдегіду з киснем надзвичайно мала. Однак у присутності деяких металів, наприклад губчастої платини, формальдегід вже при кімнатній температурі швидко перетворюється на діоксид вуглецю.
Напрямок реакції окиснення формальдегіду в розчині змінюється при застосуванні таких окислювальних агентів, як озон, пероксид водню, йод і т. д. Дією озону в м'яких умовах формальдегід можна перетворити на мурашину кислоту. Взаємодія формальдегіду з пероксидом водню прискорюються в присутності лугів і кислот. У лужному середовищі формальдегід гладко реагує з пероксидом водню з утворенням форміату натрію[ru] і водню:
У лужному середовищі відновдює також оксиди і гідроксиди срібла, золота, міді, ртуті, бісмуту і нікелю до металів, наприклад:
Реакція Блана[ред. | ред. код]
При дії формальдегіду і галогеноводню на ароматичні вуглеводні останні вступають в реакцію галогенометилювання:
Це перетворення, що отримало назву реакції Блана, є зручним методом одержання сполук, в яких атом галогену знаходиться не в ароматичному ядрі, а в бічному ланцюзі[14]. Реакція Блана відбувається при помірному нагріванні, причому формальдегід може знаходитися як у водному розчині, так і у вигляді параформу[ru]. Як каталізатор застосовують мінеральні та кислоти Льюїса, зокрема хлорид цинку.
Методи визначення[ред. | ред. код]
Якісне визначення[ред. | ред. код]
Реакція з хромотроповою кислотою (метод Егріва)[ред. | ред. код]
При нагріванні розведеного водного розчину формальдегіду з хромотроповою кислотою (1,8-дигідроксинафталін-3,6-дисульфокислотою) за наявності міцної сірчаної кислоти розчин набуває фіолетового забарвлення, за інтенсивністю якою судять про кількість формальдегіду[1][15].
Метод Деніже[ред. | ред. код]
В основі методу лежить кольорова реакція між формальдегідом і фуксинбісульфітним реактивом Шиффа[ru][16]. У наступний період в рецептуру приготування реактиву були внесені зміни, у зв'язку з чим він отримав назву «модифікованого реагенту Шиффа»[1].
Полярографічний метод[ред. | ред. код]
Це один із найнадійніших і найточніших способів визначення малих кількостей формальдегіду у водних і водно-органічних середовищах. Він полягає в тому, що деякі речовини здатні відновлюватися на крапельному ртутному електроді, причому відновлення відбувається при строго індивідуальній напрузі, яка називається потенціалом напівхвилі[17]. У середині 30-х років XX століття було відкрито, що формальдегід полярографічно активний, потенціал його напівхвилі (при використанні каломельного електрода порівняння) дорівнює -1,63 В[1]. За висотою хвилі на полярограмі судять про вміст формальдегіду в розчині. Етаналь і вищі альдегіди відновлюються при більш високих потенціалах, метанол, етанол та інші спирти визначенню не заважають.
Як фон застосовують розчини нейтральних солей KCl або лугів LiOH, KOH, NaOH. Так як луги навіть при помірній температурі викликають хімічні перетворення формальдегіду, рекомендується знімати полярограму відразу ж після змішування проби з фоном.
Кількісний аналіз[ред. | ред. код]
Гідроксиламіновий метод[ред. | ред. код]
Суть методу — взаємодія формальдегіду з гідрохлоридом гідроксиламіну з утворенням формальдоксиму і вільної соляної кислоти:
Приладно-методичне оформлення аналізу залежить від способу визначення виділеної соляної кислоти або оксиму і пов'язане, в основному, з наявністю тих чи інших домішок, що впливають на похибку. У найпростішій модифікації метод полягає в прямому алкілметричному визначенні соляної кислоти[1][18].
Сульфітний метод[ред. | ред. код]
В основі методу — реакція формальдегіду із сульфітом натрію, в результаті якої утворюється ніби продукт приєднання гідросульфіту натрію[ru] до формальдегіду і вільний луг:
або
У тому випадку, якщо вихідний розчин сульфіту має кислу реакцію, титрування ведуть розчином їдкого натру до появи блідо-блакитного забарвлення. Нейтральний розчин сульфіту натрію переливають у колбу з наважкою, перемішують протягом 2 хвилин і титрують розчином соляної кислоти.
Йодометричний метод[ред. | ред. код]
Це один з найстарших способів кількісного визначення формальдегіду. Найбільш ефективно цей метод застосовується для знаходження невеликих кількостей формальдегіду у водних розчинах, що не містять домішок інших органічних речовин. Остання обставина випливає з самої природи методу, основаного на окисненні формальдегіду солями гіпойодитної кислоти[ru], оскільки окиснюватися в таких умовах може багато інших сполук. Визначення складається із наступних стадій[1][18]:
- утворення гіпойодиту калію
- перетворення KIO у суміш йодиду і йодату калію
- виділення йоду при підкисленні розчину суміші солей
- титрування вільного йоду розчином тіосульфату натрію
Метод застосування перекису водню[ред. | ред. код]
Метод оснований на окисненні формальдегіду:
При дії пероксиду водню формальдегід перетворюється на мурашину кислоту, яка відразу нейтралізується попередньо доданими надлишком лугу. За кількістю непрореагованого лугу (титрування розчином соляної або сірчаної кислот з індикатором бромтимоловий синій[ru]) вираховується вміст формальдегіду у вихідному розчині. Очевидно, що методу притаманний той же недолік, що й попередньому: у присутності пероксиду водню окиснюються сполуки різних класів, а отже, аналізований розчин не повинен містити жодних домішок.
Дімедоновий (метоновий) метод[ред. | ред. код]
Метод застосовується як для якісного, так і для кількісного визначення формальдегіду[1][16][18]. Дімедон[en] (метон, 5,5-діметилдигідрорезорцин, 5,5-диметил-1 ,2-циклогександіон, діметол) є таутомерною сполукою і існує у вигляді суміші трьох форм — енольної, кетонної та змішаної. Дімедон кількісно реагує з формальдегідом в нейтральних, лужних і слабокислих середовищах (вода, етанол) з утворенням метиленбісметону. Останній проявляє себе як одноосновна кислота, розчиняється в лугах і його можна відтитрувати спиртовими розчинами основ.
Хроматографія[ред. | ред. код]
Застосування хроматографічних методів ускладнюється у випадках, коли речовини характеризуються здатністю до взаємодії з електростатично неоднорідним сорбційним полем твердих носіїв, особливо високою реакційною здатністю і т. д. Всіма цими властивостями, на жаль, відрізняється і формальдегід, і супутні йому речовини — вода, метанол і особливо мурашина кислота. Для усунення методичних труднощів з визначенням формальдегіду останній в деяких випадках переводять в інші сполуки, зручніші для хроматографування. Однак повністю усунути всі перешкоди при проведенні аналізу поки не вдається. Основним недоліком методу залишається недостатня відтворюваність як площ, так і форми піків. Результати аналізу сильніше, ніж для інших сумішей, залежать від розміру проби, співвідношення компонентів, передісторії колонки і т. д. Тому газохроматографічне визначення формальдегіду найчастіше практикується для контролю роботи дослідних установок, склад потоків в яких змінюється порівняно мало.
Застосування[ред. | ред. код]
Виробництво полімерних матеріалів[ред. | ред. код]
Виробництво полімерних і поліконденсаційних продуктів безперечно є найважливішим напрямком використання формальдегіду. При одержанні цих матеріалів формальдегід може застосовуватися або безпосередньо у вигляді мономеру (кополімеру), або як сировина для синтезу полімерного продукту.
Традиційно одним з найбільш масових споживачів формальдегіду є виробництво пластичних мас і смол. Розрізняють такі типи цих матеріалів на основі формальдегіду: фенолоформальдегідні (продукт конденсації з фенолом), амідоформальдегідні (конденсація з карбамідом або меламіном), поліформальдегідні і т. д.
З урахуванням призначення виробу, що випускається, широко практикується введення в рецептуру невеликих добавок різних реагентів, які додають основному продукту ті чи інші експлуатаційні властивості — спиртів, кислот, ефірів, амінів і т. д. Тому справжній механізм утворення багатьох матеріалів вельми складний і не завжди повністю вивчений. Специфічні і різноманітні також технологія і апаратурне оформлення синтезу полімерних смол і пластмас, через що це виробництво, по суті, виділяється в самостійну галузь промисловості.
Фенолоформальдегідні смоли[ред. | ред. код]
Одержання фенолформальдегідних смол і пластмас на їх основі (фенопластів) належить до найстаріших виробництв такого роду. Перші установки з одержання смол на основі лісохімічного формальдегіду та коксохімічного фенолу були створені на початку 1900-х років. Смоли використовувалися для одержання клеїв і лаків, а також литих виробів. У 20—30-х роках XX століття фенолоформальдегідні смоли і фенопласти отримали виключно широке поширення в найрізноманітніших галузях виробництва більшості розвинених країн — у лакофарбовій, будівельній, електротехнічній та інших. За останні роки асортимент пластичних матеріалів значно розширився.
Фенолоформальдегідні смоли діляться на дві групи: термопластичні (новолачні) і термореактивні (резольні). До першої групи належать смоли, які після термообробки залишаються пластичними і розчинними в полярних розчинниках (спирти, кетони). Смоли другої групи при нагріванні втрачають пластичні властивості і перетворюються на твердий полімер, практично нерозчинний у звичайних розчинниках.
Амідоформальдегідні смоли[ред. | ред. код]
Для одержання смол і пластмас найбільшого значення набули реакції формальдегіду з карбамідом (сечовиною) і меламіном (триамінотриазином), в результаті яких одержують так звані амідоформальдегідні смоли. Ці смоли в рідкому стані використовуються для просочення будівельних матеріалів, приготування лаків, фарб, клеїв, а у застиглому — для одержання амінопластів, пінопластів і т. ін. Амідоформальдегідні смоли характеризуються порівняно невеликою молекулярною масою і повинні розглядатися як олігомери.
Поліформальдегід[ред. | ред. код]
Основним елементом пластичних матеріалів на основі формальдегіду є нерозгалужені лінійні поліметиленові (поліацетальні) структури: -CH2OCH2OCH2-.
Молекулярна маса промислових зразків поліформальдегіду в середньому становить 30 000-50 000 (до 100 000). Розрізняють дві основні модифікації поліформальдегіду: гомополімер, що складається в основному з формальдегіду, і кополімер, що містить невелику кількість зв'язків -C-C- (зазвичай не більше 3-5 %), за рахунок кополімеризації з такими мономерами, як оксиран, Діоксолан[ru], похідні альдегіду, ізоціанова кислота і т. д. Обидва типи полімеру є термопластичними матеріалами, що володіють високим ступенем кристалізації. Поліформальдегідні пластмаси характеризуються високою механічною міцністю, стійкістю до повзучості і стирання, хімічною інертністю і низьким водопоглинанням, практичною відсутністю усадки і т. д. Ці властивості роблять поліформальдегід пластмасою конструкційного типу, що витримує динамічні навантаження і успішно замінює багато металів і сплавів. Різні модифікації поліформальдегіду випускаються за кордоном під торговими назвами дельрін, хостаформ С, целконг, поліфайд, дуракон та ін[19].
Триоксан[ред. | ред. код]
Триоксан належить до найпростіших олігомерів формальдегіду. Хоча він, будучи циклічним тримером, не володіє властивостями високополімерних матеріалів, його одержання тісно пов'язане з виробництвом поліформальдегіду і зазвичай існує в рамках останнього. Триоксан є вихідною сировиною для одержання поліформальдегіду.
Параформ[ред. | ред. код]
Параформ[ru] — це пухка, аморфна речовина, яка, крім того, недостатньо стабільна. Через ці особливості параформ не має самостійного застосування як полімерний матеріал. Основним його призначенням є використання в різних синтезах, в які з якихось причин небажано вводити великі кількості води.
Інші полімерні матеріали[ред. | ред. код]
Крім перерахованих найбільших виробництв полімерних матеріалів, є ще кілька важливих і перспективних напрямів використання формальдегіду в даній галузі. До них належить одержання полівінілформалю, що застосовується у виробництві електроізоляційних лаків, клеїв для склеювання металів, монопластів і т. д. Полівінілформалі випускають у вигляді твердих порошків або гранул.
Важливий напрямок використання формальдегіду в полімерній хімії — синтез полісульфідних каучуків. Найбільш поширені з них рідкі полісульфідні каучуки — тіоколи. Особливістю рідких тіоколів є їх здатність до затвердіння при звичайній температурі, в результаті чого утворюються вироби з властивостями вулканізованих гум. Це дозволяє поєднувати процес затвердіння з формуванням готових виробів, проводячи його безпосередньо в розливних посудинах, прес-формах і т. д. Полісульфідні каучуки характеризуються високою стабільністю, стійкістю до окиснювачів і розчинників.
Виробництво багатоатомних спиртів[ред. | ред. код]
Синтез багатоатомних спиртів досить простий і не вимагає застосування особливо дефіцитних реагентів чи матеріалів. У той же час наявність в молекулі четвертинного С-атома надає спиртам високої термостабільності, а також стійкості до випромінювань, дії кислот і лугів і т. д.
Технологія одержання багатоатомних спиртів ґрунтується на конденсації формальдегіду з будь-яким іншим найпростішим аліфатичним альдегідом — оцтовим, пропіоновим, масляним та ін.
Оскільки альдольна конденсація найбільш інтенсивно відбувається в лужному середовищі, як каталізатори на практиці застосовують їдкі луги, аміни, аніоніти і т. д.
Для відновлення спиртоальдегіду до відповідного багатоатомного спирту є два основні шляхи:
- каталітична гідрогенізація воднем
- застосування як відновлювального агента формальдегіду
В останньому випадку утворення багатоатомних спиртів може відбуватися безпосередньо в реакційному середовищі синтезу спиртоальдегіду під дією тих же лужних агентів. Однак витрата останніх різко зростає, оскільки в наведеній реакції лужний агент стехіометрично витрачається на зв'язування мурашиної кислоти з утворенням відповідних форміатів[ru].
Взаємодією формальдегіду з ацетиленом або оксидом вуглецю можна одержати відповідно 1,4-бутандіол[en] або етиленгліколь.
Пентаеритрит[ред. | ред. код]
У порівнянні з іншими багатоатомними спиртами пентаеритрит[ru] (пентаеритритол, 2,2-метокси-1 ,3-пропандіол, тетраметилолметан) є найбільш масовим продуктом. Сировиною для його одержання є оцтовий альдегід і технічний формалін. На першому етапі, в результаті приєднання трьох молекул формальдегіду до молекули етаналю утворюється триметилолоцтовий альдегід (пентаеритроза). Далі пентаеритрозу відновлюють формальдегідом із застосуванням каталізатора — гідроксиду кальцію:
Неопентилгліколь[ред. | ред. код]
Неопентилгліколь[en] (2,2-диметил-1,3-пропандіол, 2,2-диметилолпропан) застосовується для синтезу поліефірних смол і волокон, поліуретанів і консистентних мастил. Крім формальдегіду, у синтезі неопентилгліколю застосовується ізомасляний альдегід. Останній утворюється у великих масштабах як побічний продукт при виробництві масляного альдегіду гідроформілюванням пропілену.
Вперше виробництво неопентилгліколю було організовано в 1957 році фірмою Eastman Chemical Products[en] в США[20].
Перший етап синтезу неопентилгліколю — утворення пенталдолю (гідрокситриметилацетальдегіду, 3-гідрокси-2,2-диметилпропіонового альдегіду, оксипівалевого альдегіду)[20][21][22][23]. Якщо проводити реакцію при надлишку формальдегіду і лужного агенту, наприклад гідроксиду кальцію, то пенталдоль в цьому ж реакційному середовищі перетворюється на неопентилгліколь.
Етріол[ред. | ред. код]
У складі 1,1,1-триметилолалканів етріол (триметилолпропан, 2,2-дигідроксиметил-1-бутанол) є найбільш поширеним. Його виробництво базується на масляному альдегіді.
Перші роботи, що стосувалися, синтезу етріолу були проведені в Німеччині на початку 30-х років. Дослідна установка була запущена у 1937 році, ймовірно з метою одержання вибухових речовин типу тринітрогліцерину. Згодом виробництво етріолу було освоєне у багатьох країнах[4][21].
Етріол утворюється в результаті приєднання двох молекул формальдегіду до α-вуглецевого атому бутаналю. Ця реакція відбувається у дві стадії. Спочатку утворюється 2-метилол-1-бутаналь:
Приєднуючи ще одну молекулу формальдегіду, 2-метилол-1-бутаналь перетворюється на 2,2-диметил-1-бутаналь:
Як лужні агенти можуть застосовуватися їдкі луги, аніоніти та інші речовини основного характеру[21].
Подальше перетворення 2,2-диметилол-1-бутаналю в етріол також може відбуватися двома шляхами
- прямою гідрогенізацією[24]
- перехресною реакцією Канніццаро
Найбільшого поширення набув другий варіант. У цьому випадку і утворення, і відновлення одержаного альдегіду послідовно відбувається в одному і тому ж реакторі.
Метріол, триметилоізобутан, триметилолпентан[ред. | ред. код]
Дослідне виробництво метріолу (1,1,1-триметилолетану, 2-метил-2-гідроксиметил-1 ,3-пропандіолу, пентагліцерину) було створене в Німеччині в 1938 році. Як і етріол, метріол, ймовірно, спочатку використовувався для одержання вибухових речовин.
Механізм і умови синтезу метріолу багато в чому схожі з процесами одержання інших багатоатомних спиртів, особливо з одержанням етріолу. На першому етапі за наявності лужного агента відбувається послідовне приєднання двох молекул формальдегіду до молекули пропіонового альдегіду з утворенням 2,2-диметилолпропаналю:
Як каталізатори можуть застосовуватися їдкі луги, карбонати лужних металів, третинні аміни, аніонообмінні смоли і т. д.
Другий етап — відновлення 2,2-диметилолпропану за рахунок перехресної реакції Канніццаро. У цьому випадку лужний агент береться в надлишку і метріол утворюється в реакційному середовищі конденсації формальдегіду і пропіонового альдегіду, як послідовна ланка сумарного перетворення:
Метріол використовується у виробництві алкідних смол і синтетичних мастил. Фталеві смоли на основі метріолу характеризуються підвищеною твердістю і еластичністю порівняно з гліфталевими[4]. Водорозчинні полімери метріолу застосовуються в поліграфії.
Триметилолізобутан і триметилолпентан синтезуються відповідно на основі ізовалеріанового і гексилового альдегідів. Синтез цих спиртів здійснюється за конденсаційно-відновлювальною схемою в одну стадію[25]. Брутто-реакція виражається так:
Ці речовини — гомологи метріолу і етріолу, проте за наявності довшого вуглеводневого ланцюга, характеризуються і деякими новими властивостями, зокрема більш високою полярністю і поверхневою активністю.
1,4-Бутандіол, етиленгліколь[ред. | ред. код]
На основі 1,4-бутандіолу[en] синтезують поліефірні волокна типу терилену, поліуретану, тетрагідрофурану, динітрилу адіпінової кислоти і т. д. В основі його одержання лежить взаємодія формальдегіду з ацетиленом за наявності ацетилідів металів[1]. У ході реакції спочатку утворюється пропаргіловий спирт, який, приєднуючи другу молекулу формальдегіду, перетворюється на 1,4-бутіндіол:
На другій стадії 1,4-бутіндіол каталітично гідрогенізують:
Етиленгліколь є продуктом, виробництво і споживання якого у багато разів перевищує відповідні показники для всіх багатоатомних спиртів, разом узятих. Існує метод одержання етиленгліколю з формальдегіду, який був витіснений більш конкурентоспроможним методом гідратації оксирану. Цей процес складався з декількох стадій. Спочатку формальдегід гідрокарбоксилювали:
Утворена гліколева кислота на другому етапі етерифікується метанолом:
Останній етап — гідрогенізація метилгліколяту.
Конденсація формальдегіду з алкенами[ред. | ред. код]
Виробництво ізопрену[ред. | ред. код]
Одним із методів синтезу ізопрену є його одержання з ізобутилену і формальдегіду:
Проміжною стадією процесу є утворення 4,4-диметил-1,3-діоксану та його каталітичний розклад. За схемою виробництва ізопрену діоксановим методом як сировина застосовується фракція C4 дегідрогенізації ізобутану або піролізу прямогонних бензинів, а також технічний формалін.
Більше 95 % ізопрену використовується для одержання ізопренових каучуків. Також ізопрен застосовують у виробництві бутилкаучука, ізопрен-стирольних термопластів, транс-поліізопрену, парфумерних та лікарських засобів.
Присадки[ред. | ред. код]
Виробництво присадок до мастильних матеріалів і палив відрізняється надзвичайно широким асортиментом. Основною причиною цього є їх багатоцільовий характер. Так, серед популярних присадок до мастил розрізняють антиокислювальні, миючі, протизносні, в'язкісні, депресорні, протипінні і т. д.[26]. Останнім часом широкого поширення набули присадки багатофункціональної дії.
Роль формальдегіду як реагенту в синтезах присадок зводиться до таких функцій:
- додання поверхнево-активних властивостей внаслідок метоксилювання або метиламінування основного реагенту;
- додання властивостей полімерного (олігомерного) матеріалу за рахунок з'єднання молекул основного реагенту містковими зв'язками -CH2-O-, які переходять у зв'язки -CH2-}.
Більшість присадок — це висококиплячі речовини з низькою леткістю. Технологія синтезу присадок мало відрізняється від процесів одержання фенолформальдегідних або амідоформальдегідних смол.
Алкілпіридини[ред. | ред. код]
Співконденсацією двох карбонілвмісних сполук (формальдегід, етаналь, ацетон і т. ін.) з аміаком одержують клас сполук під назвою алкілзаміщені піридини. Монометилпіридини отримали назву піколіни[en], диметилпіридини — лутідінів, триметилпіридини — колідінів. На практиці зустрічаються і чотиризаміщені піридини. Окрему групу розглянутого класу складають алкілвінілпіридини, які крім алкільної містять також вінільну групу -CH=CH2. Алкілпіридини застосовуються як кополімерні добавки при виробництві синтетичних каучуків, для одержання латексів, гербіцидів, вітамінів, комплексоутворюючих реагентів.
У медицині[ред. | ред. код]

При взаємодії формальдегіду з аміаком утворюється гексаметилентетрамін (уротропін). Ця сполука застосовується для лікування запальних захворювань сечових шляхів. Терапевтичний ефект базується на дезінфікуючій дії формальдегіду, який виділяється при кислотному гідролізі уротропіну. В лужному середовищі уротропін стійкий, тому при лужній реакції сечі хворого уротропін не здійснює лікувальної дії.
Формальдегід застосовується в синтезах і інших медичних препаратів, зокрема анальгіну і пірамідону (амідопірину). Кінцеві стадії одержання цих сполук — метилювання аміногрупи, здійснюють формальдегідом за наявності бісульфіту натрію[ru] і формальдегідом в мурашиній кислоті.
Формальдегід застосовують як дезінфікуючий, консервуючий та дубильний засіб для анатомічних препаратів.
Формалін[ред. | ред. код]
Практично увесь товарний формальдегід випускається у вигляді водно-метанольних розчинів. Найбільшого поширення набув продукт, що містить 35-37 % формальдегіду і 6-11 % метанолу — формалін. Рецептура формаліну сформувалася історично, під впливом наступних факторів. По-перше, метанол і вода супроводжують формальдегід на стадії його отримання найпоширенішим методом (метанол — сировина, вода — побічний продукт і абсорбент). По-друге, розчин зазначеного складу при позитивних температурах цілком стійкий до випадання полімеру і може зберігатися або транспортуватися протягом невизначено довгого часу. По-третє, у вигляді водно-метанольного розчину формальдегід може застосовуватися в більшості виробничих синтезів, а також при безпосередньому використанні. І по-четверте, саме формалін утворюється при окисній конверсії метанолу в присутності металевих каталізаторів на стадії абсорбції контактного газу. Жодних додаткових операцій із додавання продукту товарних властивостей (концентрування, очищення і т. д.), як правило, не потрібно.
Важливий показник якості формаліну — вміст мурашиної кислоти. Це пов'язано з інтересами виробництв, що застосовують формальдегід для синтезів в лужних середовищах. При великому вмісті мурашиної кислоти формалін проходить стадію аніонітного очищення.
Роль метанолу, як і інших спиртів, у стабілізації водних розчинів, полягає у блокуванні кінцевих груп полімерних молекул і в запобіганні утворення нерозчинних поліоксиметиленів надто великої молекулярної маси.
Світовий ринок[ред. | ред. код]

Станом на 2006 рік у всьому світі вироблялося близько 8 млн формальдегіду (у перерахунку на 100 %) на рік (21,5 млн тонн — в перерахунку на 37%-ний формалін)[27]. Загальносвітові потужності складали 8,8 млн тонн. Таким чином, середнє завантаження потужностей близьке до 90 %. На виробництво формальдегіду в усьому світі витрачається близько 35,7 % метанолу.
За даними Академії Кон'юнктури Промислових Ринків в США і Канаді розташовано трохи менше третини потужностей з виробництва формальдегіду. Майже стільки ж знаходиться в Європі. У Японії і Південної Кореї розташовано 5 % від сукупного обсягу потужностей.[27]
Виробничі потужності в Європі[ред. | ред. код]
| Компанія | Країна, де розміщені виробничі потужності | Потужність у перерахунку на 100%-ний вміст формальдегіду, тис. тонн[27] |
|---|---|---|
| Dynea | Брюссель, Бельгія | 30 |
| Нідерланди | 150 | |
| Фінляндія | 70 | |
| Hexion (Borden) | Велика Британія | 33 |
| Іспанія | - | |
| Krems Chemie | Австрія | 65 |
| Degussa | Німеччина | 122 |
| Kunstharzchemie | Австрія | 6 |
| Ostereichische Hiag | Австрія | 46 |
| Lambiotte & Cie | Бельгія | 22 |
| Mepa | Бельгія | 11 |
| Nordalim | Данія | 43 |
| Dyno | Фінляндія | 22 |
| Норвегія | 26 | |
| Велика Британія | 44 | |
| Casco | Франція | 20 |
| Elf Atochem | Франція (2) | 75 |
| Німеччина (2) | 180 | |
| Norsolor Hoechst | Франція | 12 |
| Protex | Франція | 4 |
| Bakelite | Німеччина | 18 |
| BASF | Німеччина (2) | 450 |
| Bayer | Німеччина | 100 |
| Casella | Німеччина | 9 |
| GAF-Huls Chemie | Німеччина | 70 |
| Pleiderer Holzwerk | Німеччина | 13 |
| RWE-DEA | Німеччина | 8 |
| Ticoma Polymer | Німеччина | 66 |
| Hadjilucas | Греція | 8 |
| Chemie Linz | Італія | 144 |
| Chimica Pomponesco | Італія | 60 |
| Fabbrica Adhesivi | Італія | 60 |
| Sadenpan Chemica | Італія | 80 |
| Caldic Europort | Нідерланди | 15 |
| Bresfor | Португалія | 22 |
| Sonae | Португалія | 15 |
| Sotima | Португалія | 7 |
| Derivados Forestales | Барселона, Іспанія | 50 |
| Валенсія, Іспанія | 130 | |
| Туртоза, Іспанія | 40 | |
| Айкар, Іспанія | - | |
| Foresa | Іспанія | 37 |
| Poliaco | Іспанія | 24 |
| Casco Nobel | Швеція (2) | 61 |
| Perstorp | Швеція | 63 |
| Spanplattenwerk | Швейцарія | 6 |
| BP Chemicals | Велика Британія | 22 |
| Blagden Chemicals | Велика Британія | 22 |
| Kronospan | Велика Британія | 15 |
| Strathclyde Chemical | Велика Британія | 3 |
| Synthite | Велика Британія | 41 |
| Lothian | Велика Британія | 1 |
Фізіологічна дія[ред. | ред. код]
Подразнюючий газ, викликає дегенеративні процеси в паренхіматозних органах, сенсибілізує шкіру. Є повідомлення про сильну дію на центральну нервову систему, особливо на таламус. Однак таку дію пов'язують не з прямим впливом формальдегіду, а з наявністю в технічному формаліні домішок метилового спирту, а також розпадом формальдегіду в організмі на мурашину кислоту і метиловий спирт, який вибірково вражає таламус і сітківку ока.
Загальна токсична дія формальдегіду і параформальдегіду схожа, але на шкіру формальдегід впливає сильніше.
Триоксиметилен не подразнює слизові оболонки, за запахом нагадує хлороформ.
Вільний формальдегід інактивує ряд ферментів в органах і тканинах, пригнічує синтез нуклеїнових кислот, порушує обмін вітаміну С, має мутагенні властивості[28][29]
Гостре отруєння[ред. | ред. код]
Тварини[ред. | ред. код]
У білих мишей при 0,02-0,06 мг/л і вище відразу фіксується подразнення слизових оболонок. У наступні дні — виснаження, важке дихання. При 0,4 мг/л гинуло 88 % піддослідних тварин. У загиблих були виявлені геморагічна бронхопневмонія, дифузний бронхіт, а в серці, головному мозку, печінці, нирках, надниркових залозах, гіпофізі і шлунково-кишковому тракті — осередки крововиливів і некрозів.
При одноразовому введенні в шлунок для мишей ЛД50 становить 385 мг/кг, для щурів — 424 мг/кг[30].
У кішок при 0,02-0,06 мг/л виникала слинотеча, виділення рідини з носа, почастішання дихання, 0,14-0,2 мг/л до кінця першої хвилини викликає сильне слиновиділення, різке занепокоєння, через 3-5 хвилин виділення пінистої рідини з носа, задишка, іноді блювання. У наступні дні серозні гнійні риніти, кашель, помітне виснаження. При вдиханні 0,4 мг/л після 2-годинної експозиції гинули всі піддослідні тварини (в середньому на третю добу). При розтині виявляли трахеїт і пневмонію.
У дослідах на плодовій мусі виявлена мутагенна активність формальдегіду[31].
При одноразовому введенні в шлунок параформальдегіду мишам ЛД50 становить 0,5 г/кг, а при введенні поліформальдегіду щурам ЛД50 = 5,0 г/кг. Обидві сполуки викликали однакову картину отруєння, яка характеризувалася загальним збудженням, утрудненням дихання, тремтінням всього тіла. У печінці та нирках спостерігалися тяжкі циркуляторні і дистрофічні розлади.
Людина[ред. | ред. код]
Для гострого отруєння характерне подразнення слизових оболонок очей і верхніх дихальних шляхів: сльозотеча, біль в очах, паршіння в горлі, нежить, чхання і кашель, біль і відчуття тиску в грудях, задишка, ядуха. Одночасно, наростає загальна слабкість, пітливість, головний біль; іноді виникає запаморочення, відчуття страху, хитка хода, судоми, гіперемія шкіри обличчя, слизової оболонки носа, носові кровотечі. У нічний час кашель і задишка посилюються. У першу добу відзначається еозинофілія[32]. Поріг сприйняття запаху, за різними даними, 0,00007-0,0004 мг/л[33][34].
Описано декілька смертельних випадків після прийому внутрішньо 100-200 мл 5 % розчину формаліну при картині частого блювання, різкого болю в горлі, коматозного стану. Смерть після шлункової кровотечі наставала через 5–6 годин або на 4 добу. Розтин засвідчив фіксацію формаліном стравоходу, шлунка, кишечника, підшлункової залози, нижньої частини печінки та селезінки[35].
Хронічне отруєння[ред. | ред. код]
Тварини[ред. | ред. код]
У мишей, які вдихали 0,05-0,2 мг/л формальдегіду 3 рази на тиждень по 1 годині протягом 35 тижнів, в епітелії трахей і бронхів було виявлено базальноклітинну гіперплазію і метаплазію[ru]. Морські свинки в умовах хронічного впливу гинули. Розтин показував різкі зміни у слизових оболонках дихальних шляхів і дистрофію печінки та нирок. Сенсибілізація морських свинок зареєстрована при вмісті формальдегіду у крові 3,3-4,4 мг% і його концентрації у повітрі 0,005 мг/л[28].
Людина[ред. | ред. код]
У людей, які працювали з технічним формальдегідом, що містив також 14-16 % метилового спирту, спостерігалися випадки отруєння. Вони виражалися в розладах травлення, тремтінні, розладах зору. На підприємствах, де концентрація формальдегіду досягала 0,02-0,07 мг/л, у робітників відзначалися відсутність апетиту, схуднення, слабкість, стійкі головні болі, серцебиття, безсоння і т. д.[36].
Хронічне отруєння формальдегідом може проявлятися у розладах чутливості до тактильних, больових і температурних подразнень (альгезії і гіпералгезії[ru]), які часто обмежуються однією стороною тіла або навіть окремими ділянками; в розладах потовиділення (підвищена пітливість однієї, частіше правої, половини тіла), в неоднаковості температури обох половин тіла і т. д. Одна з частих і важких форм професійного захворювання — астма від формальдегіду, яка може залишатися у хворих і після переходу на іншу роботу[37].
Дія на шкіру і слизові оболонки[ред. | ред. код]
Тварини[ред. | ред. код]
При нанесенні на шкіру живота кролика на 2 години формалін виникає поверхневий некроз з і тривалим загоєнням. Після занурення вуха кролика у формалін на 30 хвилин відзначено тільки почервоніння з подальшим лущенням. Введення декількох крапель формаліну в око кішки спричиняє різкі сльозотечу, слинотечу та виділення рідини з носа, які, проте, швидко проходять.
Людина[ред. | ред. код]
Формалін іноді викликає захворювання нігтів (розм'якшення, ламкість, болючість), болі в кінцях пальців, пухирчасті висипи на шкірі, кропивницю по всьому тілу, зменшення потовиділення на дотичних з ним ділянках шкіри. Такі захворювання можуть викликати навіть дуже розведені розчини формальдегіду (до 0,015 %). Зазвичай процес має симетричний характер, поширюючись тильною поверхнею кистей і передпліч. Відзначається сверблячка, легка гіперемія і інфільтрація, надалі — висипання[38]. Почервоніння і інфільтрація можуть супроводжуватися утворенням наривів з поверхневим некрозом або приводити до утворення твердих вузликових потовщень і розтріскування затверділих поверхонь.
Після шкірних уражень, викликаних дією формальдегіду і смол, залишається підвищена чутливість. Захворювання може наступити і після багатьох років роботи з формальдегідом. Не виключена можливість загальної отруйної дії в результаті всмоктування формальдегіду через шкіру.
Легка подразнююча дія на слизові оболонки очей і дихальних шляхів у робітників спостерігалася в приміщеннях, де концентрація формальдегіду була від 0,001 до 0,0095 мг/л. 0,025 мг/л викликає сильне подразнення слизових оболонок[39].
Поведінка в організмі[ред. | ред. код]
Формальдегід швидко і повністю всмоктується за будь-якого шляху надходження в організм. Через 12 годин після введення в шлунок найбільшу кількість виявлено в кістковому мозку[40]. Формальдегід окиснюється в мурашину кислоту, одночасно утворюється і метиловий спирт. Ця реакція відбувається в печінці. Формальдегід також активно реагує з аміногрупами білків та амінокислот, з метильними групами холіну і метіоніну[41]. 40 % міченого формальдегіду протягом 12 годин видихається, нирками за цей час видаляється 10 %, кишечником 1 %. Значна кількість видихається у вигляді [42].
Невідкладна терапія[ред. | ред. код]
При отруєнні шляхом вдихання необхідно винести потерпілого на свіже повітря. Потім організувати інгаляцію водяною парою з додаванням кількох крапель нашатирного спирту (нейтралізує надлишок формальдегіду з утворенням уротропіну). За показаннями: інгаляції кисню, серцеві ліки, стимулятори дихання, заспокійливі засоби (настоянка валеріани, бром) .
При подразненні слизових оболонок дихальних шляхів — лужні або олійні інгаляції. При подразненні очей — промивання водою або фізіологічним розчином, холодні примочки.
При отруєнні через рот — негайне промивання шлунка 3 % розчином карбонату або ацетату натрію, але краще 3 % розчином карбонату амонію[ru]. Після цього внутрішньо необхідно прийняти 15 % розчин ацетату амонію[ru] (столовими ложками), також великі дози сечовини (понад 2,0-4,0 г через кожні 2-3 години — до 15-40 г на день), сирі яйця, білкову воду, молоко, сольові проносні, клізми.
При попаданні на шкіру — негайне промивання водою, краще 5 % розчином нашатирного спирту.
Можливий контакт у побуті[ред. | ред. код]
Формальдегід використовується при виготовленні фанери, пресованої деревини і клею. Він зазвичай виділяється при використанні шаф, килимів і меблів з ДСП. Формальдегід регулярно потрапляє в домашнє повітря з пластикових пакетів для продуктів, він виявляється при тестуванні навіть у деяких серветках і паперових рушниках. Формальдегід також вивільняється при палінні цигарок і під час роботи приладів на пальному. У гаражах і в будинках з прибудованим гаражем формальдегід надходить у повітря з вихлопної труби автомобіля[43].
Індивідуальний захист[ред. | ред. код]
Для індивідуального захисту слід застосовувати фільтрувальний промисловий протигаз марки А, герметичні захисні окуляри. В умовах дуже високих концентрацій — ізолюючі шлангові або інші протигази. При роботі з фенолоформальдегідними смолами для захисту шкіри рекомендують застосовувати мазь.
Див. також[ред. | ред. код]
| Вікісховище має мультимедійні дані за темою: Формальдегід |
Примітки[ред. | ред. код]
- ↑ а б в г д е ж и к л м н п р с Walker J. К — Formaldehyde. 3d ed. New York — London, Reinhold Corp., 1964. (англ.)
- ↑ Крылов О. В. и др. — Космическая биология и медицина, 1970, т. 1, с. 6. (рос.)
- ↑ Опарин А. И. — Вопросы философии, 1979, № 4, с. 41. (рос.)
- ↑ а б в г Справочник нефтехнмика/Под ред. С. К. Огородникова. Л.: Химия, 1978. Т. 2. (рос.)
- ↑ Медведев С. С., Робинзон Е. А. — Труды Ин-та физ. химии им. Карпова, 1925, № 4, с. 117—125. (рос.)
- ↑ Klimkiewicz R. — Wiadomości Chemiczne, 1977, v. 31, № 12, p. 713—728. (пол.)
- ↑ Trifiro Е. е. а. — Journal of Catalysis, 1971, v. 27, р. 324. (англ.)
- ↑ Novakova J. е. а. — Journal of Catalysis, 1971, v. 21, № 2, р. 143—148. (англ.)
- ↑ Налбандян А. Б. и др. — Известия АН СССР. Серия химических наук, 1955, № 5, с. 789—799. (рос.)
- ↑ Reichert В. Die Mannich-Reaktion, Berlin: Springer, 1959. (нім.)
- ↑ Сайкс П. Механизмы реакций в органической химии: Пер. с 3-го изд./Под ред. Я. М. Варшавского. М.: Химия. 1973. гл. 8. (рос.)
- ↑ Бутлеров А. М. Сочинения, М.: Изд-во АН СССР, 1953. Т. 1, с. 63. (рос.)
- ↑ Ениколопян H. С., Вольфсон С. А. Химия и технология формальдегида. М.: Химия, 1968. (рос.)
- ↑ Вацуро К. В., Мищенко Г. Л. Именные реакции в органической химии. М.: Химия, 1976, с. 61. (рос.)
- ↑ Полюдек-Фабини Р., Бейрих Т. Органический анализ: Пер. с нем. Л.: Химия, 1981, с. 119. (рос.)
- ↑ а б Губен-Вейль. Методы органической химии. М.: Госхимиздат, 1963, с. 431, 458. (рос.)
- ↑ Крюкова Т. А. и др. Полярографический анализ. М.: Госхимиздат, 1959, с. 434. (рос.)
- ↑ а б в Эшворт М. Р. Ф. Титрометрические методы анализа: Пер. с англ./Под ред. А. Л. Крешкова. М.: Химия, 1972. Кн. 1, 2. (рос.)
- ↑ Еникополян Н. С., Вольфсон С. А. Химия и технология формальдегида. М.: Химия, 1968. (рос.)
- ↑ а б Справочник нефтехимика/Под рад. С. К. Огородникова. Л.: Химия, 1978. Т. 2. (рос.)
- ↑ а б в Рудковский Д. М. и др. Многоатомные спирты. Л.: Химия, 1972. 168 с. (рос.)
- ↑ Cornils B., Felchtinger H. — Chemiker-Zeitung, 1976, Bd. 100, № 12, S. 502—504. (нім.)
- ↑ Высоцкий М. П. и др. — Химическая промышленность, 1977, № 2, с. 18—20. (рос.)
- ↑ Патент ЧССР 161450, 1975. (чес.)
- ↑ Патент США 3959406, 1976. (англ.)
- ↑ Кулиев А. М. Химия и технология присадок к маслам и топливам. М.: Химия, 1972. (рос.)
- ↑ а б в Мировой рынок формальдегида
- ↑ а б Дуева Л. А. Гигиена труда, 1966, № 11, с. 39–43. (рос.)
- ↑ Гофмеклер В. А. Гигиена и санитария, 1968, № 3, с. 12—16. (рос.)
- ↑ Померанцева О. Материалы к практической конференции врачей, Куйбышев, 1970, с. 421. (рос.)
- ↑ Раппопорт И. А. Влияние химических факторов в онтогенезе, Москва, 1966, с. 7–12. (рос.)
- ↑ Данілін В. А., Мещеряков В. П. Гигиена труда, 1968, № 7, с. 45–46. (рос.)
- ↑ Сгибиев А. К. Гигиена труда, 1968, № 7, с. 20–25. (рос.)
- ↑ Фельдман Ю. Г., Боиашевская Т. И. Гигиена н санитария, 1971, № 5, с. 6–11. (рос.)
- ↑ Simon A. Archives of Toxicology, 1966, Bd. 21, № 5, S. 279—283. (англ.)
- ↑ Камчатнов В. М., Гаязова С. С. Гигиена и санитария, 1971, № 2, с. 100—101. (рос.)
- ↑ Noceto J. B., Lafont H. Arch, malad. profession, 1962, v. 23, № 4–5, p. 314. (англ.)
- ↑ Андреев А. В. Гигиена труда, 1962, № 11, с. 59–60.
- ↑ Schuck E. A. et al. Archives of Environmental Health, 1966, v. 13, № 5. p. 570—575. (англ.)
- ↑ Buss J. et al. Archives of Experimental Pathology and Pharmacology, 1964, Bd. 247, № 5, S. 380—381. (англ.)
- ↑ Москвичева И. В. и др. Вопросы медицинской химии, 1967, т. 13, № 4, с. 398—404. (рос.)
- ↑ Brock N. W. Biochemical Pharmacology, 1964, v. 13, № 8, p. 1137—1142. (англ.)
- ↑ Воздух, которым мы дышим…
Джерела[ред. | ред. код]
- Посібник з хімії для вступників до вузів // Г. П. Хомченко. Київ: «Вища школа», 1970.
- Митронов О. П., Глікін М. А., Кочергін О. М., Мудрий О. П., Ставраті В. І., Зубко Л. П., Кулешов М. П., Громихаліна С. О. Спосіб одержання формальдегіду. — 2003.
- Небесний Р. В., Івасів В. В., Жизневський В. М., Шибанов С. В. Спосіб отримання каталізатора газофазної конденсації насичених карбонових кислот з формальдегідом. — 2010.
- Огородгиков С. К. Формальдегид. — Ленинград : Химия, 1984. — 280 с. (рос.)
- Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей / Под. ред. Лазарев Н. В. и Левиной Э. Н. — Ленинград : Химия, 1976. — Т. 1. — С. 505-509. — 49000 прим. (рос.)
- Химическая энциклопедия / Под. ред. Зефиров Н. С. — Москва : Большая российская энциклопедия, 1998. — Т. 5. — С. 115. (рос.)
- Walker J. F., Коржев П. П. Формальдегид. — Государственное научно-техническое издательство химической литературы, 1957. — 608 с. (рос.)
- Адрианов Р. А., Пономарев Ю. Е. Пенопласты на основе фенолформальдегидных полимеров. — Ростов : Издательство Ростовского университета, 1987. — 80 с. (рос.)
- Walker J. К. Formaldehyde. — 3. — New York—London : Reinhold Corporation, 1964. (англ.)
Посилання[ред. | ред. код]
- Ситнік К.М. Фармацевтична енциклопедія.
- Орган екологічної сертифікації та маркування. Архів оригіналу за 6 січня 2014.
- Про формальдегід на сайті BabyGreen. (рос.)
- Формальдегид (Е240). (рос.)
- Мировой рынок формальдегида. (рос.)
| |||||||||||||||||||
|
|
Ця стаття належить до добрих статей української Вікіпедії. |



















































