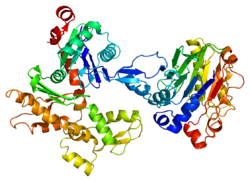
Бета-актин
Перейти до навігації
Перейти до пошуку
Бета-актин (англ. Actin beta) – білок, який кодується геном ACTB, розташованим у людей на короткому плечі 7-ї хромосоми. [4] Довжина поліпептидного ланцюга білка становить 375 амінокислот, а молекулярна маса — 41 737[5].
Послідовність амінокислот
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MDDDIAALVV | DNGSGMCKAG | FAGDDAPRAV | FPSIVGRPRH | QGVMVGMGQK | ||||
| DSYVGDEAQS | KRGILTLKYP | IEHGIVTNWD | DMEKIWHHTF | YNELRVAPEE | ||||
| HPVLLTEAPL | NPKANREKMT | QIMFETFNTP | AMYVAIQAVL | SLYASGRTTG | ||||
| IVMDSGDGVT | HTVPIYEGYA | LPHAILRLDL | AGRDLTDYLM | KILTERGYSF | ||||
| TTTAEREIVR | DIKEKLCYVA | LDFEQEMATA | ASSSSLEKSY | ELPDGQVITI | ||||
| GNERFRCPEA | LFQPSFLGME | SCGIHETTFN | SIMKCDVDIR | KDLYANTVLS | ||||
| GGTTMYPGIA | DRMQKEITAL | APSTMKIKII | APPERKYSVW | IGGSILASLS | ||||
| TFQQMWISKQ | EYDESGPSIV | HRKCF |
Білок має сайт для зв'язування з АТФ, нуклеотидами. Локалізований у цитоплазмі, цитоскелеті.
Література[ред. | ред. код]
- Ponte P., Ng S.Y., Engel J., Gunning P., Kedes L. (1984). Evolutionary conservation in the untranslated regions of actin mRNAs: DNA sequence of a human beta-actin cDNA. Nucleic Acids Res. 12: 1687—1696. PMID 6322116 DOI:10.1093/nar/12.3.1687
- Nakajima-Iijima S., Hamada H., Reddy P., Kakunaga T. (1985). Molecular structure of the human cytoplasmic beta-actin gene: interspecies homology of sequences in the introns. Proc. Natl. Acad. Sci. U.S.A. 82: 6133—6137. PMID 2994062 DOI:10.1073/pnas.82.18.6133
- Ohmori H., Toyama S., Toyama S. (1992). Direct proof that the primary site of action of cytochalasin on cell motility processes is actin. J. Cell Biol. 116: 933—941. PMID 1734024 DOI:10.1083/jcb.116.4.933
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Hanukoglu I., Tanese N., Fuchs E. (1983). Complementary DNA sequence of a human cytoplasmic actin. Interspecies divergence of 3' non-coding regions. J. Mol. Biol. 163: 673—678. PMID 6842590 DOI:10.1016/0022-2836(83)90117-1
- Stueven T., Hartmann E., Goerlich D. (2003). Exportin 6: a novel nuclear export receptor that is specific for profilin.actin complexes. EMBO J. 22: 5928—5940. PMID 14592989 DOI:10.1093/emboj/cdg565
Примітки[ред. | ред. код]
- ↑ Захворювання, генетично пов'язані з Бета-актин переглянути/редагувати посилання на ВікіДаних.
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:132 (англ.) . Архів оригіналу за 23 липня 2017. Процитовано 30 січня 2017.
- ↑ UniProt, P60709 (англ.) . Архів оригіналу за 28 грудня 2016. Процитовано 30 січня 2017.
Див. також[ред. | ред. код]
| Це незавершена стаття про білки. Ви можете допомогти проєкту, виправивши або дописавши її. |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||